
【题目】化合物H是一种抗血栓药物,其合成路线流程图如下:
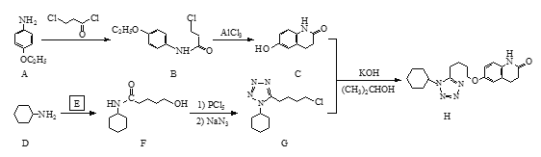
(1)B中的含氧官能团名称为_________________(写两种)。
(2)C + G → H 的反应类型为________________。
(3)环状分子E 的分子式为C5H8O2 ,写出E的结构简式:______________________。
(4)写出同时满足下列条件的C的一种同分异构体的结构简式____________________。
①含有苯环和一种含氧官能团,能与FeCl3溶液发生显色反应;
②分子中有叁键,有一个手性碳原子,有5种不同化学环境的氢。
(5)已知: ![]() ;
;![]() 。
。
写出以![]() 和
和![]() 为原料制备
为原料制备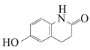 的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。__________________
的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。__________________
【答案】酰胺键,醚键 取代反应 ![]()
 或
或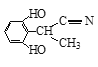
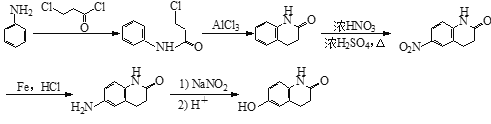
【解析】
A发生取代反应生成B,B发生取代反应生成C,环状分子E的分子式为C5H8O2,根据DF结构简式知E为![]() ,CG发生取代反应生成H;
,CG发生取代反应生成H;
(5)以![]() 和
和![]() 为原料制备
为原料制备![]() ,苯胺两次发生取代反应,然后和浓硝酸发生取代反应,再发生还原反应、最后发生取代反应得到目标产物;
,苯胺两次发生取代反应,然后和浓硝酸发生取代反应,再发生还原反应、最后发生取代反应得到目标产物;
或苯胺先发生取代反应、再和浓硝酸发生取代反应、再发生取代反应、还原反应、最后发生取代反应得到目标产物。
(1)B中的含氧官能团名称为酰胺键、醚键,
故答案为:酰胺键、醚键;
(2)C+G→H的反应类型为取代反应,还生成HCl分子,故答案为:取代反应;
(3)E的结构简式:![]() ,
,
故答案为:![]() ;
;
(4)C的同分异构体符合下列条件:
①含有苯环和一种含氧官能团,能与FeCl3溶液发生显色反应,说明含有酚羟基且含有2个酚羟基;
②分子中有叁键,有一个手性碳原子,有5种不同化学环境的氢,
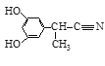
则符合条件的结构简式为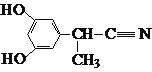 或
或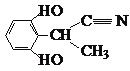 ,
,
故答案为: 或
或 ;
;
(5)以![]() 和
和![]() 为原料制备
为原料制备![]() ,苯胺两次发生取代反应,然后和浓硝酸发生取代反应,再发生还原反应、最后发生取代反应得到目标产物;
,苯胺两次发生取代反应,然后和浓硝酸发生取代反应,再发生还原反应、最后发生取代反应得到目标产物;
或苯胺先发生取代反应、再和浓硝酸发生取代反应、再发生取代反应、还原反应、最后发生取代反应得到目标产物,其合成路线为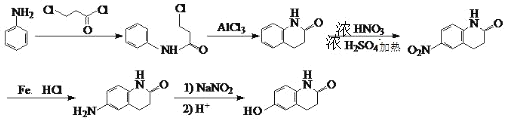 或
或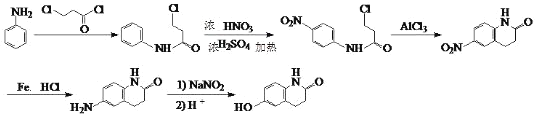 ,
,
故答案为: 或
或 。
。


 精英口算卡系列答案
精英口算卡系列答案科目:高中化学 来源: 题型:
【题目】已知H+可以写成H3O+,从某些性质看,NH3和H2O,![]() 和H3O+,OH-和
和H3O+,OH-和![]() ,N3-和O2-两两相似,据此判断下列反应式(反应条件忽略)正确的是( )
,N3-和O2-两两相似,据此判断下列反应式(反应条件忽略)正确的是( )
①2Na+2NH3=2NaNH2+H2↑
②CaO+2NH4Cl=CaCl2+2NH3↑+H2O
③3Mg(NH2)2=Mg3N2+4NH3↑
④NH4Cl+NaNH2=NaCl+2NH3↑
A.①B.②④C.全部D.①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究金属与硝酸的反应,实验如下。
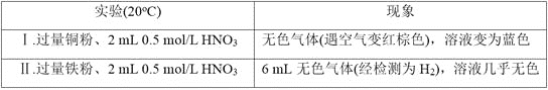
(1)Ⅰ中的无色气体是_________。
(2)Ⅱ中生成H2的离子方程式是______________。
(3)研究Ⅱ中的氧化剂
①甲同学认为该浓度的硝酸中H+的氧化性大于![]() ,所以
,所以![]() 没有发生反应。乙同学依据Ⅰ和Ⅱ证明了甲的说法不正确,其实验证据是____________。
没有发生反应。乙同学依据Ⅰ和Ⅱ证明了甲的说法不正确,其实验证据是____________。
②乙同学通过分析,推测出![]() 也能被还原,依据是_____________,进而他通过实验证实该溶液中含有
也能被还原,依据是_____________,进而他通过实验证实该溶液中含有![]() ,其实验操作是____________。
,其实验操作是____________。
(4)根据实验,金属与硝酸反应时,影响硝酸还原产物不同的因素有__________;试推测还可能有哪些因素影响_________(列举1条)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.1 mol CO2与0.3 mol C在恒压密闭容器中发生反应:CO2(g) + C(s)2CO(g)。平衡时,体系中各气体的体积分数与温度的关系如图。已知:用气体分压表示的化学平衡常数KP = ![]() ;气体分压(P分) = 气体总压(P总) ×体积分数。下列说法正确的是
;气体分压(P分) = 气体总压(P总) ×体积分数。下列说法正确的是
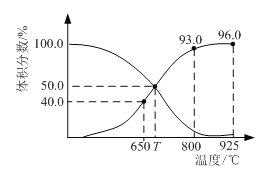
A.650℃时,CO2的平衡转化率为25%
B.800℃达平衡时,若充入气体He,v正 < v逆
C.T ℃达平衡时,若充入等体积的CO2和CO时,v正 > v逆
D.925℃时,用平衡气体分压表示的化学平衡常数KP = 23.04P总
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某反应的微观示意图如图所示,下列说法错误的是
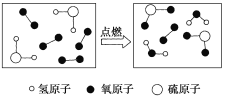
A.反应物中有单质
B.生成物均是氧化物
C.反应前是混合物,反应后是纯净物
D.化学方程式是2H2S+3O2![]() 2SO2+2H2O
2SO2+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应H2SO4既表现氧化性,又表现出酸性的是
A.Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
B.Zn+ H2SO4==ZnSO4+H2↑
C.C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2O
D.CuO+ H2SO4=CuSO4 +2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】制备钙掺杂纳米Fe3O4,并模拟吸附废水中磷元素的主要实验流程如下:

已知:①CaO2能氧化溶液中的FeCl2,反应生成Fe(OH)3和Fe3+。
②掺杂的Ca2+嵌入Fe3O4中,洗涤时不损失,吸附时不形成Ca3(PO4)2等沉淀。
③溶液的pH对吸附剂表面所带电荷有影响。pH越高,表面所带负电荷越多; pH越低,表面所带正电荷越多。
(1)向FeCl2、FeCl3混合溶液中滴加NaOH溶液,一定条件下反应生成Fe3O4,其离子方程式为___________。
(2)步骤Ⅱ调节pH至11,共沉淀需在70℃条件下进行,适宜的加热方式为________。为提高共沉淀效果,还可采取的措施为_______________。
(3)磷元素的吸附效果、H3PO4水溶液中含磷物种分布分数与pH的关系分别如图1和图2所示。

①步骤Ⅳ用KH2PO4溶液模拟废水,测得酸性条件下(pH > 2)对磷元素吸附量较大,原因是:pH越低,吸附剂表面所带正电荷越多,有利于吸附阴离子;___________________
②步骤Ⅴ将吸附剂取出,用碱液解吸回收磷。结合表中数据,分析钙掺杂纳米Fe3O4吸附剂与其他类型吸附剂相比的优势有:________。
不同类型吸附剂对磷酸盐吸附能力比较
吸附剂 | 本产品 | 纯Fe3O4 | 陶瓷材质 |
吸附量/mg·g-1 | 24.1 | 5.0 | 12.5 |
(4)请设计从步骤Ⅱ反应结束后的烧瓶中获取钙掺杂纳米Fe3O4产品的实验方案:用磁铁将沉淀物和溶液分离,______________,用筛网筛分得到产品 (实验中须使用的试剂和仪器有:蒸馏水、无水乙醇、pH计、研钵、烘箱)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“瘦肉精”是一种能减少脂肪增加瘦肉的药品,有很危险的副作用,轻则导致心律不齐,重则导致心脏病。下列关于两种常见瘦肉精的说法不正确的是
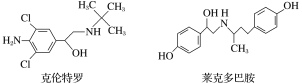
A.克伦特罗分子的分子式为C12H19ON2Cl2
B.克伦特罗能发生加成、氧化、消去等反应
C.克伦特罗和莱克多巴胺可以用FeCl3溶液鉴别
D.莱克多巴胺与足量NaOH溶液反应,生成物的化学式为C18H20NO3Na3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com