
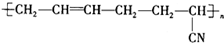 具有优良的耐油耐高温性能,合成丁腈橡胶的原料是( )
具有优良的耐油耐高温性能,合成丁腈橡胶的原料是( )| A. | ③⑥ | B. | ②③ | C. | ①③ | D. | ④⑤ |
分析 首先要根据高聚物的结构简式判断高聚物是加聚产物还是缩聚产物,然后根据推断单体的方法作出判断;丁腈橡胶为加聚反应产物,加聚产物的单体推断方法为:
(1)凡链节的主链上只有两个碳原子(无其它原子)的高聚物,其合成单体必为一种,将两半链闭合即可;
(2)凡链节主链上只有四个碳原子(无其它原子)且链节无双键的高聚物,其单体必为两种,在正中间画线断开,然后将四个半键闭合即可;
(3)凡链节主链上只有碳原子并存在碳碳双键结构的高聚物,其规律是“见双键,四个碳,无双键,两个碳”画线断开,然后将半键闭合,即将单双键互换.
解答 解:该高聚物链节主链不含杂原子,属于加聚反应生成的高聚物,链节主链上存在碳碳双键结构,有6个碳原子,其单体必为两种,按如图所示断开 ,在将双键中的1个C-C打开,然后将半键闭合即可的该高聚物单体为:①CH2=CH-CH=CH2、③CH2=CH-CN,
,在将双键中的1个C-C打开,然后将半键闭合即可的该高聚物单体为:①CH2=CH-CH=CH2、③CH2=CH-CN,
故选C.
点评 本题考查了加聚反应原理及高分子化合物单体的求算,题目难度中等,注意掌握加聚反应的概念及反应原理,明确高分子化合物单体的求算方法.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | ①②④⑤ | B. | ②③⑤⑥ | C. | ③④⑥ | D. | ①③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
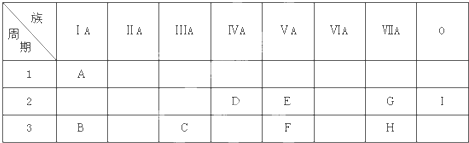
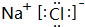 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 大烧杯上没有盖硬纸板 | |
| B. | 用环形铜丝搅拌棒代替环形玻璃搅拌棒 | |
| C. | 用相同浓度和体积的硝酸代替稀盐酸溶液进行实验 | |
| D. | 用1gNaOH固体代替50mL0.5mol/L的NaOH溶液进行实验 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有大量AlO2-的溶液中:K+、Al3+、Br-、HCO3-可共存 | |
| B. | CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)=2 CO(g)+O2(g)反应的△H=+566.0kJ/mol | |
| C. | 将SO2通入Ca(ClO)2溶液中:Ca2++2ClO-+SO2+H2O=CaSO3↓+2 HClO | |
| D. | 在某钠盐溶液中含有等物质的量的Cl-、I-、SO32-、CO32-、NO3-、SiO32-中的一种或多种,当加入过量的盐酸产生气泡,溶液颜色变深但仍澄清,阴离子种数减少3种,则原溶液中一定有CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 8n | B. | 14n | C. | 18n | D. | 44n |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com