
����Ŀ����֪ij�¶��£�Ksp��AgCl��=1.56��10��10 �� Ksp��Ag2CrO4��=1��10��12 �� ���й��ڸ��¶��µ�������ȷ���ǣ� ��
A.���Ȼ���������Һ�м����Ȼ�����Һ��Ksp��AgCl����С
B.����AgCl��Һ�뱥��Ag2CrO4��Һ��ȣ�ǰ�ߵ�c��Ag+����
C.����0.0008molL��1��K2CrO4��Һ�м�������0.002 molL��1��AgNO3��Һ����CrO42������ȫ����
D.����0.001molL��1AgNO3��Һ����Ũ�Ⱦ�Ϊ0.001 molL��1��KCl��K2CrO4�����Һ�У����Ȳ���AgCl����
���𰸡�D
���������⣺A���¶Ȳ�����Ksp���䣬��A���� B������AgCl��Һ��c2��Ag+��=Ksp��AgCl��=1.56��10��10 �� ����Ag2CrO4��Һ�� ![]() =Ksp��Ag2CrO4��=1��10��12 �� ��Ȼ���ߵ�c��Ag+����B����
=Ksp��Ag2CrO4��=1��10��12 �� ��Ȼ���ߵ�c��Ag+����B����
C��CrO42������ȫ������c��CrO42��������10��5molL��1 �� ��ʱc��Ag+���� ![]() =3.2��10��4molL��1 �� ��Ӧ��0.0008molL��1��K2CrO4��Һ�м������[3.2��10��4+2��0.0004��10��5��]��2=2.2��10��3molL��1 �� ��C����
=3.2��10��4molL��1 �� ��Ӧ��0.0008molL��1��K2CrO4��Һ�м������[3.2��10��4+2��0.0004��10��5��]��2=2.2��10��3molL��1 �� ��C����
D������AgCl��Һ��c��Ag+���ȱ���Ag2CrO4��Һ��c��Ag+��С������ͬŨ�ȵ�KCl��K2CrO4�����Һ�е���AgNO3��Һ��������AgCl��������D��ȷ��
��ѡD��
A��AgCl��Kspֻ���¶��йأ������ӵ�Ũ���йأ�
B������AgCl��Һ��c2��Ag+��=Ksp��AgCl��=1.56��10��10 �� ����Ag2CrO4��Һ�� ![]() =Ksp��Ag2CrO4��=1��10��12 �� �ɴ˷������
=Ksp��Ag2CrO4��=1��10��12 �� �ɴ˷������
C���������߷�Ӧ��Ȼ�����ʣ�������ӣ�����ܶȻ���CrO42�����ӵ�Ũ����1.0��10��5mol/L�Ƚϣ�
D������Ksp��AgCl����Ksp��Ag2CrO4������Cl����CrO42����ʼ����ʱc��Ag+�����Ƕ��٣�


 �·Ƿ��̸����100��ϵ�д�
�·Ƿ��̸����100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��Ϊ��ѧ��ѧ�ij��������Ҿ�����ͬһ��Ԫ�أ�����֮���ת����ϵ����ͼ��ʾ(��Ӧ���������������Ѿ���ȥ)��
A![]() B
B![]() C
C![]() D��
D��
��1����A������DΪǿ���:
��C�Ļ�ѧʽΪ______.
��C��D��Ӧ�Ļ�ѧ����ʽΪ__________________��1molC��ȫ��Ӧת�Ƶ��ӵ����ʵ���Ϊ_____________��
��2����AΪ���壬��ʹʪ��ĺ�ɫʯ����ֽ������DΪǿ�ᣬ��
��д��A��B �Ļ�ѧ����ʽ:_______________��
����Ҫ�ռ�B���壬�����ռ�װ���к��ʵ���(�����)______________��

��1.92gͭͶ��һ����D��Ũ��Һ�У�ͭ��ȫ�ܽ⣬���ռ���672mL����(��״��)����Ӧ������D �����ʵ���Ϊ____����ʢ�д����������������ˮ�У�ͨ���״����һ�������O2��ǡ��ʹ������ȫ����ˮ�У���ͨ��O2�����Ϊ____ (��״��)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������������һ���������ܼ�������������ܼ���ʵ�����Ʊ�������������ķ�Ӧԭ����ʵ��װ�ü�����������£�3CH3COOH+ ![]()
![]()
![]() +3H2O
+3H2O
���� | ��� | �ܶ�/gcm��3 | �е�/�� | ˮ�� |
���� | 92 | 1.2636 | 290 | �� |
���� | 60 | 1.0492 | 118 | �� |
����������� | 218 | 1.1596 | 258 | ���� |

ʵ�鲽�裺
����1����500mL��Ӧ���м���200g�����ᣬ92g���ͺ�100mL���������������������Ӳ��¶ȼƿڼ���3mLŨ����������Ȳ�����1h��ֹͣ���ȣ�
����2����5%̼������Һϴ�ӣ�����ˮϴ�ӣ���������ˮ�Ȼ��ƣ�
����3���Ƚ��г�ѹ�����ռ�75��85����֣�
����4������ѹ����ٽ��м�ѹ�����ռ�128��131��/933Pa��֣����յò�Ʒ176g��
��1������1�ȿ����������Ũ�����Ŀ�����������������Ŀ����
��2����5%̼������Һϴ�ӵ���ҪĿ����������ˮ�Ȼ��Ƶ�Ŀ����
��3������ü�ѹ��������ó�ѹ������ԭ����
��4������ʵ�����Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CMA������ơ�����þ����Ļ����Ǹ��ٹ�·����ɫ��ѩ�����������ʷ�Һ����ľ��Һ����Ҫ�ɷ����ᣬ�Լ������ļ״������ӡ����͵����ʣ�������ʯ����Ҫ�ɷ�MgCO3CaCO3 �� ��SiO2�����ʣ���Ϊԭ������CMA��ʵ��������ͼ1�� 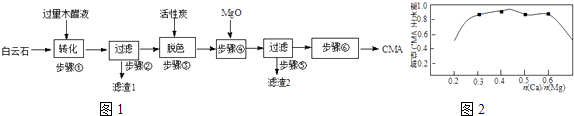
��1������ٷ����ķ�Ӧ���ӷ���ʽΪ ��
��2���������������1����Ҫ�ɷ�Ϊ��д��ѧʽ���������������Һ���ʺ�ɫ����ɫ����ľ��Һ�к�����������ɫ�Ľ����й��⣬������ɫ����һ��Ҫԭ���� ��
��3����֪CMA�иơ�þ�����ʵ���֮�����ˮ�ʣ�����ѩЧ�������ȣ���ϵ��ͼ2��ʾ������ܵ�Ŀ�ij�����n��Ca����n��Mg��ԼΪ��ѡ�1��2��3��7��2��3���⣬��һĿ���� ��
��4������ް����IJ����������ˡ�ϴ�Ӽ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ�����������ʵ���Ũ�Ⱦ�Ϊ0.2 molL-1��NaOH��Һ��ϡH2SO4��500mL��
�ṩ���Լ��ǣ�NaOH�����98%��ŨH2SO4���ܶ�Ϊ1.84 g/cm3��������ˮ��
��1��Ӧ��������ƽ����NaOH__________g��Ӧ��10mL��Ͳ��ȡŨH2SO4____________mL��
��2������������Һʱ����Ҫ��������__________��
��3��������������Һʵ���У����в���������ƫ�͵���_________________������ţ�
A�����ձ����ܽ����ʽ���ʱ������������Һ
B��û��������ˮϴ�ձ�2��3�Σ�����ϴҺ��������ƿ��
C������ʱ����������ƿ�̶����Կ��Ƽ�ˮ��
D����������Һ������ƿת�Ƶ��Լ�ƿʱ������������
E����Ũ�������ձ���ϡ�ͺ���ת�ƽ�����ƿ���к������ò���
F������ƿ��������ˮϴ����û�к��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ���Ҵ�ȼ�ϵ�ص�ʵ��װ��ͼ�������й�˵��һ����ȷ���ǣ� �� 
A.���ô�װ�ø������϶��ϲ�������N�缫�������缫��M�缫�������缫
B.�׳��и����ĵ缫��ӦʽΪ��CH3CH2OH��12e��+3H2O=2CO2+12H+
C.�׳�KOH��Һ�о���0.05mol����ʱ���������ҳ��е�M�缫��������5.04g
D.M�缫�ϵĵ缫��ӦʽΪ��Ag++e��=Ag
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�����ܱ������������淴Ӧ��Z������+W������X��g��+Y��������H����t1ʱ�̷�Ӧ�ﵽƽ�⣬��t2ʱ����С���������t3ʱ���ٴδﵽƽ��״̬��δ�ٸı������������й�˵������ȷ���ǣ� �� 
A.Z��W�ڸ�������������һ����Ϊ��̬
B.t1��t2ʱ�����t3ʱ�̺���ʱ��η�Ӧ��ϵ�������ƽ��Ħ�������������Ҳ���ܲ���
C.���ڸ��¶��´˷�Ӧƽ�ⳣ������ʽΪK=c��X������t1��t2ʱ�����t3ʱ�̺��XŨ�Ȳ����
D.���÷�Ӧֻ��ij�¶�T�����Է����У���÷�Ӧ��ƽ�ⳣ��K���¶����߶���С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����RNH2+R��CH2Cl ![]() RNHCH2R��+HCl��R��R����������� �ڱ���ͬϵ���ܱ���������������磺
RNHCH2R��+HCl��R��R����������� �ڱ���ͬϵ���ܱ���������������磺 ![]()
![]()
![]()
�� ![]()
![]()
![]() �������������ԣ��ױ�������������C����ȡ�����飨����ʹ�����м�����ϳ�·����ͼ��ʾ��
�������������ԣ��ױ�������������C����ȡ�����飨����ʹ�����м�����ϳ�·����ͼ��ʾ��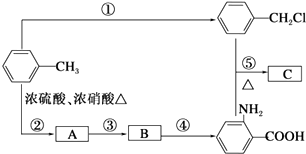
��ش��������⣺
��1��B���ʵĽṹ��ʽ�� ��
��2��д����Ӧ�١��ڵĻ�ѧ����ʽ�� ����
�� ��
��3����Ӧ�١����У�����ȡ����Ӧ�������Ӧ��ţ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵���в���ȷ����
A. NH3��Һ��
B. Cu��������Ũ������������ϡ���ᣬ������Ļ�ԭ����Ϊ����������
C. Cu�ڼ��ȵ�������������Ũ����
D. �������м���Ũ���ᣬ��������ɫ��Ϊ��ɫ������Ũ�������ˮ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com