
【题目】“大象牙膏”的实验操作是向30%的过氧化氢溶液中加入少量二氧化锰和表面活性剂,现象如图. 
(1)主要反应的化学方程式是 .
(2)过氧化氢被称为绿色氧化剂,原因是(填序号). a.过氧化氢具有强氧化性
b.过氧化氢的还原产物是水
c.过量的过氧化氢能自行分解
(3)制取过氧化氢的过程如图: ![]()
①用氧化钡制取过氧化钡的反应属于反应(填序号).
a.化合 b.分解 c.氧化还原
②用过氧化钡制取过氧化氢的化学方程式是 .
(4)以重晶石为原料制取过氧化氢,制得的过氧化氢浓度低且能耗高.有人提出下列制取过氧化氢的方案,从原理上分析合理的是(填序号). a.在一定条件下,O2氧化H2O
b.在一定条件下,H2还原H2O
c.在一定条件下,O2氧化H2 .
【答案】
(1)2H2O2═2H2O+O2↑
(2)bc
(3)ac; H2SO4+BaO2═BaSO4+H2O2
(4)ac
【解析】解:(1)过氧化氢在二氧化锰作催化剂作用下反应生成水和氧气,反应方程式为:2H2O2═2H2O+O2↑,所以答案是:2H2O2═2H2O+O2↑;(2)过氧化氢的还原产物是水,而且过量的过氧化氢能自行分解生成氧气和水,所以过氧化氢常被称为绿色氧化剂,所以答案是:bc;(3)①用氧化钡制取过氧化钡,首先发生氧化反应,然后发生复分解反应,所以答案是:ac;
②过氧化钡制取过氧化氢的化学方程式是H2SO4+BaO2═BaSO4+H2O2,所以答案是:H2SO4+BaO2═BaSO4+H2O2;(4)a.在一定条件下,O2氧化H2O,变成﹣1价的氧,故符合;
b.H2O中的氧是﹣2价,不能被还原,故不符合;
c.在一定条件下,O2氧化H2,生成过氧化氢,故符合;故选:ac.


 每课必练系列答案
每课必练系列答案科目:高中化学 来源: 题型:
【题目】我国“复兴号”高速列车的运行速度达到350 km·h-1。高速列车制造要使用轻质金属材料。下列可以作为轻质金属材料的是( )
A. 铝合金B. 铁合金
C. 碳素纤维D. 硅纤维
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图是一些含氯产品. 
(1)储氯钢瓶中应贴的标签为 . a.易燃品 b.爆炸品 c.有毒品
(2)漂白粉的有效成分是(填化学式),其与空气中的反应可得到具有漂白能力的次氯酸.
(3)“84”消毒液的有效成分是次氯酸钠,“84”消毒液与除垢剂(有效成分为盐酸)混合使用会产生黄绿色、有刺激性气味的气体,该反应的离子方程式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是小王在医院做的血常规检查报告单的部分内容.小王应注意补充的微量元素是( )
序号 | 项目 | 结果 | 正常范围 | 单位 |
1 | 红细胞计数 | 2.3 | 3.5~5 | ×1012/L |
2 | 血红蛋白 | 75 | 110~150 | g/L |
3 | 血小板计数 | 205.0 | 100~300 | ×109/L |
A.硒
B.锌
C.铁
D.碘
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以含Fe2O3、FeO、SiO2、Al2O3的混合物为原料,设计两种制备铁红(Fe2O3)的方案,部分产物已略去. [方案1]![]()
[方案2]![]()
(1)溶液A所含的阳离子有 .
(2)加入双氧水的作用是 .
(3)固体C的成分是(填化学式).
(4)试剂x可以选择(填序号). a.NaOH溶液 b.氨水 c.二氧化碳 d.稀H2SO4
(5)用试剂x浸取原料发生的离子方程式是、 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁、钴(Co)、镍(Ni)是同族元素,都是较活泼的金属,它们的化合物在工业上有重要的应用.
(1)草酸钴(CoCO)是一种难溶于水的浅粉红色粉末,通常用硫酸钴溶液和草酸铵溶液反应制得,写出该反应的离子方程式:
(2)现将含0.5mol FeCl3的溶液和含0.5mol KSCN的溶液混合,混合后溶液体积为1L,已知溶液存在平衡:Fe3++SCN﹣Fe(SCN)2+(忽略其它过程).平衡浓度c[Fe(SCN)2+]与温度T的关系如图1所示:则该反应△H0(填“>”或“<”),温度为T1时,反应在5秒钟时达到平衡,平衡时c[Fe(SCN)2+]=0.45mol/L,求达到平衡时的平均反应速率
v(SCN﹣)=molL﹣1S﹣1 , 该温度下的Fe3+的平衡转化率为 , 该温度下反应的平衡常数为 . 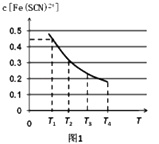
(3)已知某溶液中,Co2+、Ni2+的浓度分别为0.60mol/L和1.2mol/L,取一定量的该溶液,向其中滴加NaOH溶液,当Co(OH)2开始沉淀时,溶液中 ![]() 的值等于 . (取两位有效数字)
的值等于 . (取两位有效数字)
(已知Ksp[Co(OH)2]=6.0×10﹣15 , Ksp[Ni(OH)2]=2.0×10﹣15)
(4)工业上还可用通过电解浓NaOH溶液制备Na2FeO4 , 其工作原理如图2所示,则阳极的电极反应式为 . 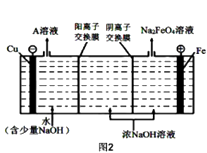
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】偏四氯乙烷是一种常见化工原料,以偏四氯乙烷和烯烃(C5H10)为原料合成某种六元环酯(C7H10O4)的合成路线如下: ![]()
已知:一个碳原子上连接2个﹣OH不稳定,容易脱水变成 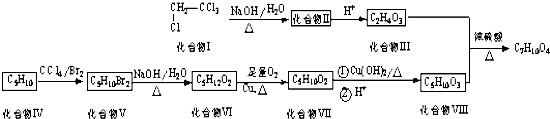
(1)化合物II中能与能与金属钠反应的官能团名称为 .
(2)化合物IV合成化合物V的反应类型为 , 化合物V合成化合物VI反应类型为 .
(3)写出由化合物VI合成化合物VII的反应方程式 .
(4)有机物R是化合物IV的同分异构体,R能使溴水褪色,且其核磁共振氢谱中有4组峰,有机物R的结构简式为 , 该六元环酯(C7H10O4)的结构简式为
(5)参照上合成路线,设计以有机物Cl2CH2﹣CH2Cl2和乙二醇为原料合成聚乙二酸乙二醇酯的合成路线.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1,2一二氯乙烯有如图两种结构. 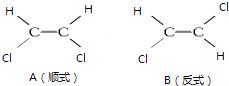
试回答下列问题:
(1)A、B分子中所含化学键类型(填“相同”或“不同”,下同),分子极性;
(2)A、B两种分子在CCl4中溶解度较大的是;
(3)将A、B加入Br2的CCl4溶液中,可得物质C,则C的结构简式为 , C物质(填“有”或“无”)手性异构体.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物X是一种医药中间体,其结构简式如图所示.下列有关化合物X的说法正确的是( ) 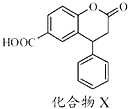
A.分子式为C16H14O4
B.1mol化合物X在一定条件下最多加成6molH2
C.分子中有三种官能团,酸性条件下水解后官能团还是三种
D.1mol化合物X最多能与2molNaOH反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com