
科目:高中化学 来源:2016届湖北省高三上学期10月调考理综化学试卷(解析版) 题型:选择题
为精确测定工业纯碱中碳酸钠的质量分数(含少量NaCl),准确称量W0 g样品进行实验,下列实验方法所对应的实验方案和测量数据最合理(除W0外)的是
实验方法 | 实验方案 | 测量数据 | |
A. | 滴定法 | 将样品配成100 mL溶液,取10 mL,加入甲基橙,用 标准盐酸滴定 | 消耗盐酸的体积 |
B. | 量气法 | 将样品与盐酸反应,生成的气体全部被碱石灰吸收 | 碱石灰增重 |
C. | 重量法 | 样品放入烧瓶中,置于天平上,加入足量盐酸 | 减轻的质量 |
D. | 量气法 | 将样品与盐酸反应,气体通过排水量气装置量气 | 排水体积 |
查看答案和解析>>
科目:高中化学 来源:2016届上海市高三上学期摸底测试化学试卷(解析版) 题型:填空题
填空题(共9分)下表中列出了五种短周期元素A、B、C、D、E的信息,请推断后作答:
元素 | 有关信息 |
A | 元素主要化合价为-2,原子半径为0.074nm |
B | 所在主族序数与所在周期序数之差为4,同周期主族元素中原子半径最小 |
C | 原子半径为0.102nm,其单质在A的单质中燃烧,发出明亮的蓝紫色火焰 |
D | 最高价氧化物对应水化物,能按1:1电离出电子数相等(10个电子)的阴阳离子 |
E | 原子半径为0.075nm,最高价氧化物对应水化物与其氢化物组成一种盐X |
1.写出A、E两种元素符号 、 。
2.画出B原子的核外电子排布式: ;写出D元素最高价氧化物对应水化物的电子式: 。
29.盐X水溶液显 (选填“酸”、“碱”或“中”)性,用离子方程式解释其原因: 。
30.D2CA3的溶液与B的单质能发生氧化还原反应,其反应的离子方程式为 。
31.已知E元素的某种氢化物Y与A2的摩尔质量相同,Y在常温下为液态,Y的化学式为 ,Y所含的化学键为 。
(a)极性键 (b)非极性键 (c)离子键
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高一上第二次月考化学试卷(解析版) 题型:计算题
取一定量Na2CO3和Na2SO4的混合物溶液分成两等份,一份与过量盐酸反应,生成2.016 L CO2(标准状况下),另一份加入足量的Ba(OH)2溶液,得到沉淀的质量为20.06 g。试计算原混合物中Na2CO3和Na2SO4的物质的量分别为多少?(写计算过程)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川树德中学高一上10月阶段测化学试卷(解析版) 题型:填空题
(14 分)(1)某同学用托盘天平称量烧杯的质量,天平平衡后的状态如图 1 所示。由图中可以看出,该同学在操作时的一个错误是_________________,烧杯的实际质量为_______________g。
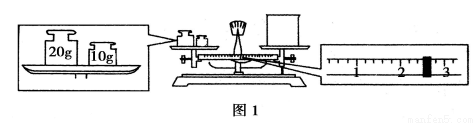
(2)需配制210 mL 0.2 mol·L-1 NaCl溶液,该同学转移溶液的示意图如图2所示。指出实验中存在的错误_______________________。
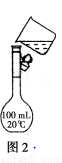
(3)用质量分数为 98%、密度为 1.84 g·cm-3的浓硫酸配制100 mL 0.1 mol·L-1的稀硫酸。
①应用量筒量取浓硫酸______________mL;
②配制硫酸时需用到的仪器有____________________________;(除量筒外,写出其余四种)
③下列操作使所配制溶液的物质的量浓度偏高的是____________(填序号)。
A.称量时用了生锈的砝码
B.将 NaOH 放在纸张上称量
C.定容时俯视刻度线
D.往容量瓶中转移时,有少量液体溅出
E.未洗涤溶解 NaOH 的烧杯
F.定容时仰视刻度线
G.容量瓶未干燥即用来配制溶液
H.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二上第二次月考化学试卷(解析版) 题型:选择题
常温下,若溶液中由水电离产生的c(OH-)=1×10-14mol·L-1,满足此条件的溶液中一定可以大量共存的离子组是
A.Al3+ Na+ NO3- Cl- B.K+ Na+ Cl- NO3-
C.K+ Na+ Cl- AlO2- D.K+ NH4+ SO42- NO3-
查看答案和解析>>
科目:高中化学 来源:2016届辽宁省高三10月月考化学试卷(解析版) 题型:选择题
火法炼铜首先要焙烧黄铜矿,其反应为:2CuFeS2+O2→Cu2S+2FeS+SO2 ,下列说法正确的是
A、每转移l.2 mol电子,有0.2mol硫被氧化
B、CuFeS2仅作还原剂,硫元素被氧化
C、每生成1molCu2S,有4mol硫被氧化
D、SO2只是氧化产物
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二上第一次月考化学试卷(解析版) 题型:选择题
中和滴定是一种操作简单、准确度高的定量分析方法。实际工作中也可利用物质间的氧化还原反应、沉淀反应进行类似的滴定分析,这些滴定分析均需要通过指示剂来确定滴定终点,下列对几种具体的滴定分析(待测液置于锥形瓶内)中所用指示剂及滴定终点时的溶液颜色的判断不正确的是
A.用标准酸性KMnO4溶液滴定Na2SO3溶液以测定其浓度:KMnO4——紫红色
B.利用“Ag++SCN-===AgSCN↓”原理,可用标准KSCN溶液测定AgNO3溶液浓度:Fe(SCN)3——红色
C.利用“2Fe3++2I-===I2+2Fe2+”,用FeCl3溶液测量KI样品中KI的百分含量:淀粉——蓝色
D.利用OH-+H+===H2O来测量某盐酸的浓度时:酚酞——浅红色
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三上学期10月月考化学试卷(解析版) 题型:选择题
下列实验中,对应的现象以及结论都正确且两者具有因果关系的是
选项 | 实验操作 | 现象 | 结论 |
A | 将稀硝酸加入过量铁粉中,充分反应后滴加KSCN溶液 | 有气体生成,溶液呈血红色 | 稀硝酸将Fe氧化为Fe3+ |
B | 分别加热Na2CO3和NaHCO3固体 | 试管内壁都有水珠 | 两种物质均受热分解 |
C | 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热 | 铝不能熔化 |
|
D | 将KI和FeCl3溶液在试管中混合后,加入CCl4,震荡,静置 | 下层溶液显紫红色 | 氧化性:Fe3+>I2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com