
(1)已知:重铬酸根离子(Cr2O72—)是橙红色的,铬酸根离子(CrO42-)是黄色的,重铬酸钾溶于水发生反应:
Cr2O72-+H2O  2CrO42-+2H+,溶液为橙黄色,向溶液中滴加少量
2CrO42-+2H+,溶液为橙黄色,向溶液中滴加少量
6mol/L的硫酸,溶液呈 色,原因是
。
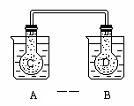 (2)如图所示,在常况下容器 A 中盛有 500mL 蒸馏水,
(2)如图所示,在常况下容器 A 中盛有 500mL 蒸馏水,
在容器 B 中盛有 500ml 1mol/L的盐酸,在烧瓶 C 和
D 中充满二氧化氮气体,并用导管将它们连通。向 A
容器中加入 50g 硝酸铵晶体,小心搅拌,使其迅速溶解;
向B中加入 10g 苛性钠固体,小心搅拌也使其迅速溶解,随着A、B中固体物质的溶解,烧瓶 C 和 D 中气体的颜色变化是 。
① 不变 ② 烧瓶 C 中颜色变深,D 中变浅
③ 烧瓶D中变深, C中变浅 ④ 两个烧瓶中的颜色都变深
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2的化学方程式如下:
2NO+2CO 2CO2+N2
2CO2+N2
为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/mol·L-1 | 1.00×10-3 | 4.50×10-4 | 2.50×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO)/ mol·L-1 | 3.60×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
请回答:以下各题(均不考虑温度变化对催化效率的影响):
(1) 在上述条件下反应能够自发进行,则反应的ΔH 0(填写“>”、“<”、“=”)。
(2) 前2s内的平均反应速度v(N2)= 。
(3) 假设在容器中发生上述反应,达到平衡时下列能提高NO转化率的是 。
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积
(4) 研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中。
| 实验编号 | T/ ℃ | NO初始浓度/ mol·L-1 | CO初始浓度/ mol·L-1 | 催化剂的比表面积/ m2·g-1 |
| Ⅰ | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
| Ⅱ | 124 | |||
| Ⅲ | 350 | 124 |
①请在空格中填入剩余的实验条件数据。
②请在给出的坐标图中,画出上表中的II、III两个实验条件下混合气体中NO浓度随时间变化的趋势曲线图,并标明各条曲线的实验编号。


查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中,不正确的是
A.草酸能使酸性高锰酸钾溶液褪色
B. MnO2、FeCl3和CuSO4都可加快H2O2的分解速率
C.要判断反应进行的方向,必须综合考虑体系的焓变和熵变
D.用稀硫酸和Zn反应制H2时,加少量CuSO4溶液对反应速率无影响
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下的定容密闭容器中发生反应H2(g)+I2(g) 2HI(g),下列方法能说明反应已经达到平衡状态的是( )
2HI(g),下列方法能说明反应已经达到平衡状态的是( )
A.容器内每减少1mol I2,同时生成2mol HI B.容器内气体压强不再变化
C.混合气体的颜色不再变化 D.混合气体的密度恒定不变
查看答案和解析>>
科目:高中化学 来源: 题型:
在室温下,把5.0mL0.10mol/L 的Na2S2O3(aq)和5.0mL0.10mol/L 的H2SO4(aq)混合,析出淡黄色沉淀,回答下列问题:
(1)反应的离子方程式是 。
(2)若将上述两溶液分别在水浴中预热到60℃,然后再将它们混合,则析出淡黄色沉淀的速率显著加快,其原因是(用有效碰撞理论解释)
。
(3)若在混合溶液中加入几滴5.00mol/L 的H2SO4(aq),则析出淡黄色沉淀的速率 (填”明显加快””明显减慢”或”基本不变”,下同),若在混合溶液中加入5.0mL8.00mol/L 的Na2SO4(aq),则析出淡黄色沉淀的速率 .
查看答案和解析>>
科目:高中化学 来源: 题型:
在相同温度和压强下,对反应CO2(g)+H2(g)=CO(g)+H2O (g)进行甲、乙、丙、丁四组实验,,实验起始时放入容器内各组分的物质的量见下表
| 物质的量 | CO2 | H2 | CO | H2O |
| 甲 | a mol | a mol | 0 mol | 0 mol |
| 乙 | 2a mol | a mol | 0 mol | 0 mol |
| 丙 | 0 mol | 0 mol | a mol | a mol |
| 丁 | a mol | 0 mol | a mol | a mol |
上述四种情况达到平衡后,n(CO)的大小顺序是
A.乙=丁>丙=甲 B乙>丁>甲>丙 C.丁>乙>丙=甲 D.丁>丙>乙>甲
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com