
【题目】A、B、C、D、E为原子序数依次增大的短周期元素,对应单质为a、b、c、d、e。B、C、D的最外层电子数之和为10,对应的最高价氧化物的水化物分别为m、n、p;q为B和E形成的二元化合物。上述物质发生的转化关系如图所示(部分产物已略去)。下列说法不正确的是
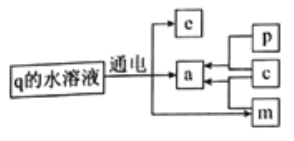
A. 可通过电解熔融状态的q制备b和e
B. 原子半径:B>C>D>E>A
C. n既能溶解在m的水溶液中,又能溶解在p的水溶液中
D. d可以保存在CS2中
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:
【题目】苯可被臭氧分解,发生化学反应![]() ,二甲苯通过上述反应可能的产物为
,二甲苯通过上述反应可能的产物为![]() ,若邻二甲苯进行上述反应,对其反应产物描述正确的是
,若邻二甲苯进行上述反应,对其反应产物描述正确的是
A. 产物为a、b、c,其分子个数比为a∶b∶c=1∶2∶3
B. 产物为a、b、c,其分子个数比为a∶b∶c=1∶2∶1
C. 产物为a和c,其分子个数比为a∶c=1∶2
D. 产物为b和c,其分子个数比为b∶c=2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室利用废弃旧电池的铜帽(Zn、Cu总含量约为99%)回收铜并制备ZnO的部分实验过程如图: 
(1)①写出铜帽溶解过程中铜发生反应的化学方程式 . ②铜帽溶解后需将溶液中过量H2O2除去.除去H2O2的简便方法是 .
(2)为确定加入锌灰(主要成分为Zn、ZnO,杂质为铁及其氧化物)的量,实验中需测定除去H2O2后溶液中Cu2+的含量.实验操作为:准确量取一定体积的含有Cu2+的溶液于带塞锥形瓶中,加适量水稀释,调节pH至3~4,加入过量KI,用Na2S2O3标准溶液滴定至终点.上述过程中的离子方程式如下: 2Cu2++4I﹣=2CuI(白色)↓+I2 I2+2S2O32﹣=2I﹣+S4O62﹣
①滴定选用的指示剂为 , 滴定终点观察到的现象为 .
②若滴定前溶液中H2O2没有除尽,所测得的Cu2+的含量将会(填“偏高”、“偏低”、“不变”).
(3)已知pH>11时Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2﹣ . 下表列出了几种离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0molL﹣1计算)
Fe3+ | Fe2+ | Zn2+ | |
开始沉淀的pH | 1.1 | 5.8 | 5.9 |
完全沉淀的pH | 3.2 | 8.8 | 8.9 |
实验中可选用的试剂:30% H2O2、1.0molL﹣1HNO3、1.0molL﹣1 NaOH.
由回收铜后的滤液制备ZnO的实验步骤依次为:
①向滤液中加入略过量 , 使其充分反应
②向反应后的溶液中滴加1.0moLL﹣1的NaOH溶液,调节溶液的pH范围为;
③过滤;
④向滤液中滴加1.0moLL﹣1的氢氧化钠,调节pH范围为;
⑤过滤、洗涤、干燥
⑥900℃煅烧.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,0.1molL﹣1CH3COONa溶液pH=11,下列表述正确的是( )
A.c(Na+)=c(CH3COO﹣)
B.c(CH3COO﹣)+c(CH3COOH)=0.1 molL﹣1
C.由水电离出来的c(OH﹣)=1.0×10﹣11 molL﹣1
D.往该溶液中加入0.05 molL﹣1的CH3COONa,pH值变大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,水溶液中H+和OH﹣的浓度变化曲线如图,下列说法正确的是( ) 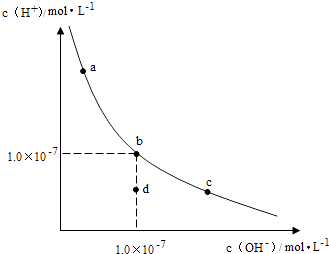
A.升高温度,可能引起由c向b的变化
B.该温度下,水的离子积常数为1.0×10﹣13
C.该温度下,加入FeCl3可能引起由b向a的变化
D.该温度下,稀释溶液可能引起由c向d的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国成功研制的一种新型可充放电AGDIB电池(铝-石墨双离子电池)采用石墨、铝锂合金作为电极材料,以常规锂盐和碳酸酯溶剂为电解液。电池反应为CxPF6+LiyAl=Cx+LiPF6+Liy-1+Al。放电过程如图,下列说法正确的是( )

A. B为负极,放电时铝失电子
B. 电解液可以用常规锂盐和水代替
C. 放电时A电极反应式为CxPF6+e-=Cx+PF6-
D. 放电时,若转移1mol电子,石墨电极上可增重7g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F为原子序数依次增大的前36号元素,其中只有两种金属元素。A与C同主族,B与E同主族;B与C能形成两种常见化合物;C与F最外层只有1个电子,且内层均已排满;基态D原子成对电子数是未成对电子数的4倍。
请问答下列问題:
(1)基态B原子的轨道表达式为______,其最高能级的电子云有_____个不同的伸展方向。
(2)B、C、E原子半径由大到小的顺序为_________(用元素符号表示)。
(3)D和E中第一电离能较大的是_______(填元素符号),原因为___________。
(4)A与B形成的最简单化合物比A与E形成的最简单化合物的熔点______(填“高“或“低”),原因为___________。
(5)D的最高价氧化物对应的水化物中,D原子的杂化轨道类型为______,已知该分子中除氢外其他原子均满足最外层8电子稳定结构,则其结构式为________。
(6)单质F及其同族元素P、Q的堆积模型均为面心立方最密堆积,三种原子的半径分别为128pm、144pm、144pm,其中P和Q的相对原子质量分别为Mτ(P)、Mτ(Q)。
①单质F中的配位数为______;密度为_____g/cm3(用NA表示阿伏加德罗常数的值,列式即可)。
②单质P和Q的密度之比为________[用含Mτ(P)、Mτ(Q)的代数式表示]。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298K时,向20mL0.01mol/LCH3COOH溶液中逐滴加入0.01mol/LKOH溶液,其pH变化曲线如图所示。下列叙述错误的是
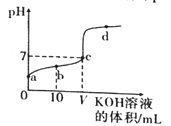
A. a>2
B. 醋酸的电离平衡常数:Ka= ![]()
C. b点溶液中:c(CH3COOH)+2c(H+)=c(CH3COO-)+2c(OH-)
D. a、b、c、d四点溶液的导电性强弱顺序:d>c>b>a
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com