
 .
. 分析 (1)设烷烃的分子式为CxH(2x+2),根据相对分子质量为72,列出方程式进行计算x值;
(2)烷烃在空气中燃烧的生成二氧化碳和水;
(3)根据烷烃同分异构体书写解答;
(4)因碳的最外层有4个电子,氢最外层1个电子,一个碳形成4对共用电子对,一氢形成一对共用电子对.
解答 解:(1)设烷烃的分子式为CxH(2x+2),则14x+2=72,解得x=5,所以该烷烃的分子式为C5H12,
故答案为:C5H12;
(2)C5H12在空气中燃烧生成二氧化碳和水,化学反应方程式为:C5H12+8O2$\frac{\underline{\;点燃\;}}{\;}$5CO2+6H2O,
故答案为:C5H12+8O2$\frac{\underline{\;点燃\;}}{\;}$5CO2+6H2O;
(3)分子式为C5H12的同分异构体有主链有5个碳原子的:CH3CH2CH2CH2CH3,
主链有4个碳原子的:CH3CH(CH3)CH2CH3,
主链有3个碳原子的:CH3C(CH3)2CH3;
故答案为:CH3CH2CH2CH2CH3、CH3CH(CH3)CH2CH3、CH3C(CH3)2CH3;
(4)因碳的最外层有4个电子,氢最外层1个电子,一个碳形成4对共用电子对,一氢形成一对共用电子对,所以电子式为 ,故答案为:
,故答案为: .
.
点评 本题考查有机物的分子式的确定,同分异构体的书写以及电子式等,题目难度不大,注意碳原子数目≤5的同分异构体的书写.


科目:高中化学 来源: 题型:选择题
| A. | 44.8 L氟化氢气体分解成22.4 L的氢气和22.4 L的氟气吸收270 kJ热量 | |
| B. | 1 mol氢气与1 mol氟气反应生成2 mol液态氟化氢放出的热量大于270 kJ | |
| C. | 相同条件下,1 mol氢气与1 mol氟气的能量总和高于2 mol氟化氢气体的能量 | |
| D. | 2 mol H-F键的键能比1 mol H-H键和1 mol F-F键的键能之和大270 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向氯化铝溶液中加入过量氨水:Al3++4NH3•H2O═AlO${\;}_{2}^{-}$+4NH${\;}_{4}^{+}$+2H2O | |
| B. | 用CH3 COOH溶解CaC03:CaCO3+2H+═Ca++H2O+CO2↑ | |
| C. | 0.1mol/LNH4Al(SO4)2溶液与0.2mol/LBa(OH)2溶液等体积混合:Al3++2SO${\;}_{4}^{2-}$+2Ba2++4OH-═2BaSO4↓+AlO${\;}_{2}^{-}$+2H2O | |
| D. | 用硫酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性: 2MnO${\;}_{4}^{-}$+6H++5H2O2═2Mn2++5O2↑+8H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ④⑥⑧ | B. | ①③④⑥⑦ | C. | ②④⑥⑦⑨ | D. | ①②③⑤⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 形成离子键的阴阳离子只存在静电吸引力 | |
| B. | 元素周期律是元素的原子核外电子排布周期性变化的结果 | |
| C. | 第三周期非金属元素含氧酸的酸性从左到右依次增加 | |
| D. | 离子化合物中只能含离子键、极性共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,2.24LCHCl3的原子总数为0.1NA | |
| B. | 1mol甲基(-CH3)所含的电子总数为9 NA | |
| C. | 1mol•L-1的醋酸钠溶液中含有的CH3COO-数目为NA | |
| D. | 60g二氧化硅晶体中含有Si-O键数目为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
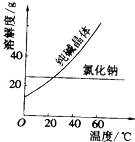 阅读、分析下列两个材料:
阅读、分析下列两个材料:| 物质 | 熔点/℃ | 沸点/℃ | 密度/g•cm-3 | 溶解性 |
| 乙二醇( C2H6O2) | -11.5 | 198 | 1.11 | 易溶于水和乙醇 |
| 丙三醇(C3H8O3) | 17.9 | 290 | 1.26 | 能跟水、酒精以任意比互溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH${\;}_{4}^{+}$、K+、Al3+、SO${\;}_{4}^{2-}$ | B. | Cl-、I-、K+、MnO${\;}_{4}^{-}$ | ||
| C. | Na+、S2O${\;}_{3}^{2-}$、SO${\;}_{4}^{2-}$、K+ | D. | Na+、NO${\;}_{3}^{-}$、PO${\;}_{4}^{3-}$、Cl- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com