
【题目】用带静电的有机玻璃棒靠近下列液体的细流,细流发生偏转的是( )
A.苯 B.二硫化碳 C.氯水 D.四氯化碳
 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案科目:高中化学 来源: 题型:
【题目】研究NO2、SO2 、CO等大气污染气体的处理具有重要意义。
(1)已知:2SO2(g)+O2(g)![]() 2SO3(g) ΔH=-196.6 kJ·mol-1
2SO3(g) ΔH=-196.6 kJ·mol-1
2NO(g)+O2(g)![]() 2NO2(g) ΔH=-113.0 kJ·mol-1
2NO2(g) ΔH=-113.0 kJ·mol-1
则反应NO2(g)+SO2(g)![]() SO3(g)+NO(g)的ΔH= kJ·mol-1。
SO3(g)+NO(g)的ΔH= kJ·mol-1。
(2) 一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是 。
a.体系压强保持不变
b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变
d.每消耗1 mol SO3的同时生成1 molNO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组利用下列实验装置探究SO2的性质。
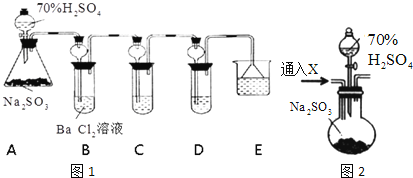
根据要求回答下列问题:
(1)装置A中反应的化学方程式为 。
(2)利用装置C可以证明SO2具有漂白性,C中盛放的溶液是 ;若要证明其漂白作用是可逆的,还需要的操作是 。
(3)通过观察D中现象,即可证明SO2具有氧化性,D中盛放的溶液可以是 ______ 。
a.NaCl溶液 b.酸性KMnO4 c.FeCl3 d.Na2S溶液
(4)研究小组发现B中有白色沉淀生成,若往B中加入过量稀盐酸,沉淀不溶解。沉淀物的化学式是 。
(5)为进一步验证B中产生沉淀的原因,研究小组进行如下两次实验:
实验i:另取BaCl2溶液,加热煮沸,冷却后加入少量苯(起液封作用),然后再按照上述装置进行实验,结果发现B中沉淀量减少,但仍有轻微浑浊.
实验ii:用如上图2的F装置代替上述实验中的A装置(其他装置不变),连接后往装置F中通入气体X一段时间,再加入70%H2SO4溶液,结果B中没有出现浑浊.
①“实验i”中煮沸BaCl2溶液的目的是 ;
②气体X可以是 (填序号)。
a.CO2 b.C12 c.N2 d.NO2
③B中形成沉淀的原因是(用化学方程式表示): 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸盐在能源、环保等方面有着广泛的用途。湿法、干法制备高铁酸盐的原理如下表所示。
湿法 | 强碱性介质中,Fe(NO3)3与NaClO反应生成紫红色高铁酸盐溶液 |
干法 | Fe2O3、KNO3、KOH混合加热共熔生成紫红色高铁酸盐和KNO2等产物 |
(1)工业上用湿法制备高铁酸钾(K2FeO4)的流程如下图所示:
![]()
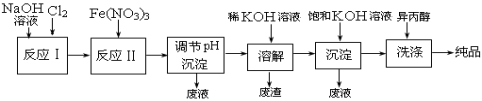
①反应I的化学方程式为 。
②反应II的离子方程式为 。
③加入饱和KOH溶液的目的是 。
(2)高铁酸钾是一种理想的水处理剂,其处理水的原理为 ;__ __。(用文字表述)
(3)干法制备K2FeO4的反应中,氧化剂与还原剂的物质的量之比为 。
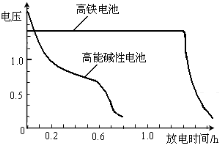
(4)高铁电池是正在研制中的可充电干电池,右图为该电池和常用的高能碱性电池的放电曲线,由此可得出的高铁电池的优点有 ; 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列递变规律不正确的是( )
A. Na、Mg、Al还原性依次减弱
B. I2、Br2、Cl2氧化性依次增强
C. C、N、O原子半径依次增大
D. P、S、Cl最高正价依次升高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:CO(g) +3H2 (g) ![]() .CH4 (g)+H2O(g)。起始以物质的量之比为1:1充人反应物,不同压强条件下,H2的平衡转化率随温度的变化情况如图所示(M、N点标记为)。下列有关说法正确的 是( )
.CH4 (g)+H2O(g)。起始以物质的量之比为1:1充人反应物,不同压强条件下,H2的平衡转化率随温度的变化情况如图所示(M、N点标记为)。下列有关说法正确的 是( )

A.上述反应的△H<0
B.N点时的反应速率一定比M点快
C.降低温度,H2的转化率可达到100%
D.工业用此法制取甲烷应采用更高的压强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的Fe与过量的稀硫酸反应制取氢气,一定温度下为加快反应速率而又不影响氢气的量,可向其中加入
A.KCl固体 B.Zn粉 C.SO3固体 D.CuSO4晶体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com