
��������ЧӦ����Դ��ȱ�����⣬��ν��ʹ����е�CO2���������Կ������ã������˸������ձ����ӡ�Ŀǰ��ҵ����һ�ַ�������CO2����ȼ�ϼ״�, һ�������·������·�Ӧ��
CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
��1��д���÷�Ӧ��ƽ�ⳣ������ʽ��K�� ����֪��K(300��)��K(350��)����÷�Ӧ��_______��Ӧ��������ȡ����ȡ���
��2�������������˵���÷�Ӧһ���ﵽƽ�����
A��������ƽ��ƽ����Է����������� B��������ѹǿ����
C��λʱ��������3mol H��H����ͬʱ����2 mol C=O��
D����������� c (H2) : c (CH3OH) = 3:1
��3��Ϊ̽����Ӧԭ�����ֽ�������ʵ�飺�����Ϊ1L�ĺ����ܱ������У�����1molCO2��3molH2�����CO2��CH3OH(g)��Ũ����ʱ��仯����ͼ��ʾ���ӷ�Ӧ��ʼ��ƽ�⣬��H2Ũ�ȱ仯��ʾ��ƽ����Ӧ����v(H2)Ϊ mol��L��1��min��1

��4�����д�ʩ����ʹ��3������n(CH3OH)/n(CO2)������� ��(����ĸ)
A�����¶� B������� C��H2O(g)����ϵ�з���
D����He(g)��ʹ��ϵ��ѹǿ���� E���ٳ���1molCO2��3molH2
��5��������һ���ܱ������г���1 mol CO2��3 mol H2������ѹǿ����,��ʹ��ʼ����루3���������������ȣ�������ͬ���¶��½��з�Ӧ���ﵽƽ��ʱ�������е�CO2������ٷ��� ________ ��3�����е�CO2������ٷ�����(�>����<����=��)
��1��K��c(CH3OH)c(H2O)/c(CO2)c3(H2)�����ȣ���2��CD����3��0.225����4��CE����5������
��������
�����������1�����ݷ�ӦCO2(g)+3H2(g) CH3OH(g)+H2O(g)�ͻ�ѧƽ�ⳣ���Ķ���д���÷�Ӧ��ƽ�ⳣ������ʽ��K��c(CH3OH)c(H2O)/c(CO2)c3(H2)����֪��K(300��)��K(350��)���������¶ȣ�ƽ�������ƶ��������¶ȣ�ƽ�������ȷ�Ӧ�����ƶ�����÷�Ӧ�Ƿ��ȷ�Ӧ����2��A������M=m/n�жϣ����ŷ�Ӧ�Ľ��У����������������䣬���ʵ��������仯����������ƽ����Է����������ϱ仯������������ƽ����Է����������䣬��Ӧ�Ѵ�ƽ��״̬������B�����ݰ����ӵ����ɣ�ͬ��ͬ��������£������ѹǿ֮�ȵ������ʵ���֮�ȣ����ŷ�Ӧ�Ľ�����������ʵ������ϱ仯����������ѹǿ���ϱ仯������������ѹǿ����ʱ����Ӧ�Ѵ�ƽ��״̬������C����λʱ��������3mol H��H����ͬʱ����2 mol C=O�� �����߾�Ϊ�淴Ӧ���ʣ�����˵���÷�Ӧһ���ﵽƽ�⣬��ȷ��D����������� c (H2) : c (CH3OH) = 3:1[������˵���÷�Ӧһ���ﵽƽ�⣬��ȷ��ѡCD����3���������ͼ��֪��10minʱ��Ӧ�ﵽƽ��״̬���״���Ũ�ȱ仯Ϊ0.75mol��L��1�����ݹ�ʽv=��c/��t���㣬v(CH3OH)=0.075 mol��L��1��min��1����������֮�ȵ��ڻ�ѧ������֮�ȼ��㣬v(H2)= 3v(CH3OH)= 0.225 mol��L��1��min��1����4��A���÷�ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ�������ƶ���n(CH3OH)/n(CO2)��С������B��������� ��ƽ�ⲻ�ƶ���n(CH3OH)/n(CO2)���䣬����C����H2O(g)����ϵ�з��룬ƽ�������ƶ���n(CH3OH)/n(CO2)������ȷ��D�����µ��������£�����He(g)����Ȼ��ϵ��ѹǿ�����뷴Ӧ��ص����ʵ�Ũ�Ȳ��䣬ƽ�ⲻ�ƶ���n(CH3OH)/n(CO2)���䣬����E�����µ��������£��ٳ���1molCO2��3molH2�൱������ѹǿ��ƽ�������ƶ���n(CH3OH)/n(CO2)������ȷ��ѡCE����5����һ���ܱ������г���1 mol CO2��3 mol H2������ѹǿ���䣬���ŷ�Ӧ�Ľ��У���������������ʵ������ϼ�С��������������ϼ�С���൱������ѹǿ��ƽ�������ƶ����ﵽƽ��ʱ�������е�CO2������ٷ��� �� ��3�����е�CO2������ٷ�����
CH3OH(g)+H2O(g)�ͻ�ѧƽ�ⳣ���Ķ���д���÷�Ӧ��ƽ�ⳣ������ʽ��K��c(CH3OH)c(H2O)/c(CO2)c3(H2)����֪��K(300��)��K(350��)���������¶ȣ�ƽ�������ƶ��������¶ȣ�ƽ�������ȷ�Ӧ�����ƶ�����÷�Ӧ�Ƿ��ȷ�Ӧ����2��A������M=m/n�жϣ����ŷ�Ӧ�Ľ��У����������������䣬���ʵ��������仯����������ƽ����Է����������ϱ仯������������ƽ����Է����������䣬��Ӧ�Ѵ�ƽ��״̬������B�����ݰ����ӵ����ɣ�ͬ��ͬ��������£������ѹǿ֮�ȵ������ʵ���֮�ȣ����ŷ�Ӧ�Ľ�����������ʵ������ϱ仯����������ѹǿ���ϱ仯������������ѹǿ����ʱ����Ӧ�Ѵ�ƽ��״̬������C����λʱ��������3mol H��H����ͬʱ����2 mol C=O�� �����߾�Ϊ�淴Ӧ���ʣ�����˵���÷�Ӧһ���ﵽƽ�⣬��ȷ��D����������� c (H2) : c (CH3OH) = 3:1[������˵���÷�Ӧһ���ﵽƽ�⣬��ȷ��ѡCD����3���������ͼ��֪��10minʱ��Ӧ�ﵽƽ��״̬���״���Ũ�ȱ仯Ϊ0.75mol��L��1�����ݹ�ʽv=��c/��t���㣬v(CH3OH)=0.075 mol��L��1��min��1����������֮�ȵ��ڻ�ѧ������֮�ȼ��㣬v(H2)= 3v(CH3OH)= 0.225 mol��L��1��min��1����4��A���÷�ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ�������ƶ���n(CH3OH)/n(CO2)��С������B��������� ��ƽ�ⲻ�ƶ���n(CH3OH)/n(CO2)���䣬����C����H2O(g)����ϵ�з��룬ƽ�������ƶ���n(CH3OH)/n(CO2)������ȷ��D�����µ��������£�����He(g)����Ȼ��ϵ��ѹǿ�����뷴Ӧ��ص����ʵ�Ũ�Ȳ��䣬ƽ�ⲻ�ƶ���n(CH3OH)/n(CO2)���䣬����E�����µ��������£��ٳ���1molCO2��3molH2�൱������ѹǿ��ƽ�������ƶ���n(CH3OH)/n(CO2)������ȷ��ѡCE����5����һ���ܱ������г���1 mol CO2��3 mol H2������ѹǿ���䣬���ŷ�Ӧ�Ľ��У���������������ʵ������ϼ�С��������������ϼ�С���൱������ѹǿ��ƽ�������ƶ����ﵽƽ��ʱ�������е�CO2������ٷ��� �� ��3�����е�CO2������ٷ�����
���㣺���黯ѧ��Ӧ���ʺͻ�ѧƽ�⡣



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2013-2014�ӱ�ʡ�����еڶ�ѧ�����п��Ը߶���ѧ�Ծ��������棩 ���ͣ�ѡ����
������������������Ļ�����Ʒ���������ijЩ���ƻ�������ġ����ﰺ����Ʒ�������յ���������䶳����е�����������ж϶�������Ľṹ��ʽ �� ����
A����4�֡���B����3�֡���C����2�֡��� D��ֻ��1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡӥ̶�и����ڶ���ģ�⿼�����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵���������ȷ���ǣ� ��
�ٻ���̿��SO2��HClO������Ư�����ã���Ư�Ļ�ѧԭ����ͬ
����100 mL0.1 mol/L ���廯������Һ��ͨ��0.05 mol������ʱ������Ӧ�����ӷ���ʽ��
2Fe2����4Br-��3Cl2=2Fe3����2Br2��6Cl-
��б��ʯKAlSi3O8����������ʽ�ɱ�ʾΪ��K2O?Al2O3?3SiO2
������������KIO3��Һ��KI��Һ������Ӧ����I2ʱ�����ӷ���ʽ��
IO3����5I����3H2O=I2��6OH��
��̼��������ӵĵ��뷽��ʽ�ɱ�ʾΪ��
��Ԫ�����ڱ��У����ϵ��£�±��Ԫ�صķǽ�������������±����������μ���
��500�桢30MPa�£���0.5 mol N2��1.5 mol H2�����ܱյ������г�ַ�Ӧ����NH3(g)����
��19.3kJ�����Ȼ�ѧ����ʽΪ��N2(g)��3H2(g)  2NH3(g) ��H= -38.6 kJ��mol-1
2NH3(g) ��H= -38.6 kJ��mol-1
A��ȫ�� B���ڢ� C���ڢۢܢ� D���ڢܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡӥ̶����ѧ����ĩ�������߶���ѧ�Ծ��������棩 ���ͣ�ѡ����
һ���¶��£���2L���ܱ������У�X��Y��Z������������ʵ�����ʱ��仯��������ͼ��ʾ������������ȷ���� ( )
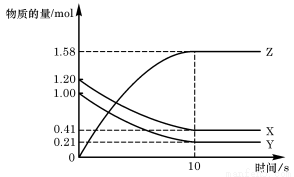
A����Ӧ��ʼ��10s����Z��ʾ�ķ�Ӧ����Ϊ0��158mol/(L��s��
B����Ӧ��ʼ��10s�� X�����ʵ���Ũ�ȼ�����0��79mol/L
C����Ӧ��ʼʱ10s�� Y��ת����Ϊ79��0%
D����Ӧ�Ļ�ѧ����ʽΪ��X(g)�� Y(g) Z(g)
Z(g)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡӥ̶����ѧ����ĩ�������߶���ѧ�Ծ��������棩 ���ͣ�ѡ����
���и��ѧ�����б�ʾ��ȷ���ǣ� ��
A��Na2O2�ĵ���ʽΪ: 
B��������ӵı���ģ��Ϊ��
C����ȩ�Ľṹ��ʽ��HCHO
D���۱�ϩ�Ľṹ��ʽΪ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡӥ̶����ѧ����ĩ��������һ��ѧ�Ծ��������棩 ���ͣ�ѡ����
��ӦA(g)��B(g)  C(g)��D(g)�����е������仯��ͼ��ʾ���ɴ˿��жϣ� ��
C(g)��D(g)�����е������仯��ͼ��ʾ���ɴ˿��жϣ� ��
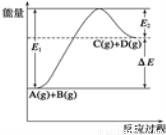
A��1molA��1molB��ַ�Ӧ�������仯Ϊ��E
B�����������Ӧ�ӿ죬��E��С
C����Ӧ����ܼ���С����������ܼ���
D����Ӧ�ﵽƽ��ʱ�������¶ȣ�A��ת��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡӥ̶����ѧ����ĩ��������һ��ѧ�Ծ��������棩 ���ͣ�ѡ����
��ͼ��Ԫ�����ڱ�ǰ�����ڵ�һ���֣�����Ԫ��R��W��X��Y��Z��������ȷ����(����)

A������������ˮ��������ԣ�W��Y
B��Z�ĵ��ʳ�������Һ�壬���ڵ������к���32��Ԫ��
C��Z��ԭ��������R��17
D���⻯��ķе㣺X��Z
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ����4���������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
�й����ʵ�ת����ϵ����ͼ��ʾ���������ʺ�������ʡȥ����C��X���ǵ��ʣ�H��Һ��dz��ɫ��I��Һ���ػ�ɫ�������й��ж���ȷ����

A. X��������ǵⵥ��
B. ͼ����ʾ��Ӧ��Ϊ������ԭ��Ӧ
C. 1mol C��E��Һ��ȫ��Ӧת�Ƶ�����ΪNA��NAΪ�����ӵ�������
D. E��H��I��Һ����ʱ����������ֹ��ˮ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ�˴��и���ģ�⿼�����ۻ�ѧ�Ծ��������棩 ���ͣ������
[��ѧ����ѡ��5���л��ﻯѧ����]��15�֣�
�߷��Ӳ���E�ͺ�����Ϣʹ�߷���ҩ��ĺϳ�������ͼ��ʾ��

��֪��I��������Ϣʹ�߷���ҩ��ĽṹΪ

�Իش��������⣺
��1����Ӧ�ٵķ�Ӧ����Ϊ ��G�ķ���ʽΪ ��
��2����1mol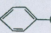 CH�� CH3��2��ת��Ϊ1mol A��1mol B����A��FeCl3��Һ��������ɫ��д��A��ϡ��Һ�����Ũ��ˮ������Ӧ�Ļ�ѧ����ʽ�� ��
CH�� CH3��2��ת��Ϊ1mol A��1mol B����A��FeCl3��Һ��������ɫ��д��A��ϡ��Һ�����Ũ��ˮ������Ӧ�Ļ�ѧ����ʽ�� ��
��3����Ӧ��Ϊ�ӳɷ�Ӧ����B�Ľṹ��ʽΪ ������Ϣʹ�Ľṹ��ʽΪ ��
��4��D�����ܶ�����ͬ״̬�¼����ܶȵ�6��25����D�и�Ԫ�ص����������ֱ�Ϊ̼60%����8%����32%��D����������������Ϊ ��
��5��д��������Ϣʹ�߷���ҩ��������������Һ������Ӧ�Ļ�ѧ����ʽΪ ��
��6��D�ж���ͬ���칹�壬������D������ͬ���������ܷ���������Ӧ��ͬ���칹����
�֣�����˳���칹����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com