
| A. | 920kJ | B. | 557kJ | C. | 188kJ | D. | 436kJ |
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加碘食盐中加入的是KIO3 | |
| B. | 常用于杀菌消毒的84消毒液的主要成份是NaClO | |
| C. | CO、NO、NO2都是大气污染气体,在空气中都能稳定存在 | |
| D. | 变色眼镜和照相器材的生产都可能要用到溴化银 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 羊毛与聚酯纤维的化学成分相同 | |
| B. | 聚酯纤维和羊毛在一定条件下均能水解 | |
| C. | 该聚酯纤维的单体为对苯二甲酸和乙醇 | |
| D. | 聚酯纤维属于纯净物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
| Ksp | 2.2×10-20 | 2.6×10-39 | 1.7×10-7 | 1.3×10-12 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
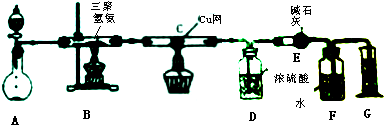
| 装置 | D | E |
| 实验前 | 101.0g | 56.0g |
| 实验后 | 106.4g | 69.2g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
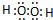 ,该分子含有极性键和非极性键(填“极性”、“非极性”)键
,该分子含有极性键和非极性键(填“极性”、“非极性”)键查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com