
| A�� | ͬ��ͬѹ�£�a g�������2a g��������ռ���֮��Ϊ1��2��ͬ��ͬѹ�¼��ҵ��ܶ�֮��Ϊ1��2 | |
| B�� | ͬ��ͬ����µ�������CO��N2��ѹǿ֮��Ϊ1��1 | |
| C�� | ij�¶�T�£�ѹǿΪ2������ѹʱ��һ���� C2H4 ����������ڱ���µ������ȣ���T=546K | |
| D�� | ͬ��ͬѹ�µ�������H218O��D216O����ԭ������� |
���� A��ͬ��ͬѹ�£����ݦ�=$\frac{m}{V}$�����ܶ�֮�ȣ�
B������PV=nRT=$\frac{m}{M}$RT֪��ͬ��ͬ����µ������ļ��ҵ�ѹǿ֮�ȵ�����Ħ�������ķ��ȣ�
C������PV=nRT֪��ͬ�����壬�¶�֮�ȵ���ѹǿ֮�ȣ�
D��n=$\frac{m}{M}$��ͬ������A��B���Ӹ���֮�ȵ���Ħ�������ķ��ȣ�������ʵĹ��������
��� �⣺A��ͬ��ͬѹ�£�a g�������2a g��������ռ�����֮��Ϊ1��2���ܶȹ�ʽΪ��=$\frac{m}{V}$������ҵ��ܶ�֮��$\frac{a}{V}$��$\frac{2a}{2V}$=1��1�����ܶ���ͬ����A����
B������PV=nRT=$\frac{m}{M}$RT֪��ͬ��ͬ����µ�������CO��N2��ѹǿ֮�ȵ�����Ħ�������ķ��ȣ���Ϊ����Ħ��������ͬ������ѹǿ��ͬ����B��ȷ��
C��PV=nRT��ͬ�����壬һ����C2H4��n��ͬ��RΪ������ѹǿΪ2������ѹʱ������������ڱ���µ������ȣ����¶�֮�ȵ���ѹǿ֮�ȣ�$\frac{2P}{P}$=$\frac{T}{273K}$��T=546K����C��ȷ��
D��H218O��D216OĦ������֮��Ϊ20��20=1��1��ͬ��ͬѹ�µ�������H218O��D216O������������ȣ�H218O��D216O����ԭ������ȣ���D��ȷ��
��ѡA��
���� ���⿼�鰢��٤�����ɼ������۵�Ӧ�ã�������������������ܶȵ��������Ŀ��飬��Ŀ�Ѷ��еȣ�ע�������ؼ��㹫ʽ�����ã�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ʯ��ʳ�Ρ��ɱ���ˮ | B�� | ʳ�Ρ����ʯ��ˮ���ɱ� | ||
| C�� | ˮ���ɱ���ʳ�Ρ����ʯ | D�� | �ɱ���ˮ��ʳ�Ρ����ʯ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | C3H6Cl2 | B�� | C3H8 | C�� | C2H6O | D�� | C3H6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | K��Na��Li | B�� | Al��Mg��Na | C�� | F��Cl��Br | D�� | Cl��S��P |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 3
3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
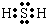 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1 mol | B�� | 1.5 mol | C�� | 2 mol | D�� | 2.5 mol |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com