
���� ��1����Ӧǰ���������ʵ������䣬��ƽ��������������ʵ���Ϊ3mol����������C�����������
��2����Ӧǰ������������䣬���º����£�����ͬ�����м���2molA 4molB��A��B�����ʵ���֮��Ϊ1��2����ԭƽ����ͬ��Ϊ��Чƽ�⣬ƽ��ʱ��ת���ʲ��䣬����ֺ�����ͬ��
��3��ƽ���C�ڷ�Ӧ������е�����������䣬��ƽ���Ч����ӦΪǰ�������������ķ�Ӧ������ѧ������ת������ߣ�����A��B�����ʵ���֮��Ϊ1��2���ɣ�
ƽ��ʱ��ͬ��ֵĺ�����ͬ����ԭƽ����Aת����Ϊx����ƽ����A��ת����Ϊy����ʾ��ƽ��ʱA�ĺ���������ƽ��ʱA�ĺ�����Ƚ��н��
��� �⣺��1����Ӧǰ���������ʵ������䣬��ƽ��������������ʵ���Ϊ3mol���ﵽƽ���������a mol C����C���������Ϊ$\frac{amol}{3mol}$=$\frac{a}{3}$���ʴ�Ϊ��$\frac{a}{3}$��
��2�����º����£���Ϊ����2molA��4molB��A��B�����ʵ���֮��Ϊ1��2����ԭƽ����ͬ����ӦΪǰ������������䣬������ԭƽ���Ч��ת���ʲ��䣬����ֺ������䣬����C�����ʵ���Ϊ$\frac{a}{3}$����2mol+4mol��=2amol���ʴ�Ϊ��2amol�����䣻
��3��ƽ���C�ڷ�Ӧ������е�����������䣬��ƽ���Ч����ӦΪǰ�������������ķ�Ӧ������ѧ������ת������ߣ�Ӧ����A��B�����ʵ���֮��Ϊ1��2���Ӧ����C�����ʵ���Ϊnmol����2+$\frac{2}{3}$n��mol����5+$\frac{1}{3}$n��mol=1��2�����n=1��
ƽ��ʱ��ͬ��ֵĺ�����ͬ����ԭƽ����Aת����Ϊx����ƽ����A��ת����Ϊy����$\frac{1-x}{3}$=$\frac{2��1-y��}{8}$=$\frac{1-y}{4}$�������ɵ�4��$\frac{x}{y}$=$\frac{1}{y}$+3������y��1����$\frac{x}{y}$��1����y��x����A��ת������ԭƽ��Ƚϼ�С��
�ʴ�Ϊ��1����С��
���� ������Ҫ�����Чƽ�⼰�йؼ��㣬�ѶȽϴ������Чƽ����ɣ�1�����º��ݣ���Ӧǰ������������ȣ�����ѧ������ת��һ�ߣ���Ӧ���������������Ӧǰ�����������ȣ�����ѧ������ת��һ�ߣ���Ӧ��������Աȣ�2�����º�ѹ������ѧ������ת��һ�ߣ���Ӧ��������Աȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 10mL | B�� | 20mL | C�� | 50mL | D�� | 100mL |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ⷨ����ʱһ���������ڵ����������е�⣬��Ҳ������Ӧ���Σ�������̬�������� | |
| B�� | ��ⷨ������ʱ���������������ᴿ�����ᴿ������Ӧ�������������������������� | |
| C�� | ���ȼҵ�У������е�������������Na0H��H2 | |
| D�� | �ȼҵ�ͽ����Ƶ������ж��õ���NaCl���ڵ��ʱ���ǵ���������Cl-ʧ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
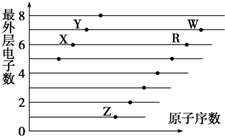
| A�� | X��R��ͬһ���� | |
| B�� | ���������ԣ�W��R | |
| C�� | X��W��������������� | |
| D�� | X��Z�γɵĻ������п��ܺ��й��ۼ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 30 g•mol-1��46 g•mol-1 | B�� | 44 g•mol-1��80 g•mol-1 | ||
| C�� | 28 g•mol-1 | D�� | 46 g•mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��ͼΪһ�������� Ca��OH��2��Һ��ͨ�������̼������� CaCO3 ��ɫ�����������������̼���֮��Ĺ�ϵ���ߣ�
��ͼΪһ�������� Ca��OH��2��Һ��ͨ�������̼������� CaCO3 ��ɫ�����������������̼���֮��Ĺ�ϵ���ߣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ̼���ƺ�ϡ���� | B�� | �����ƺ�����ͭ��Һ | ||
| C�� | ����þ������ͭ��Һ | D�� | ���ۺ�����������Һ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com