
共价键、离子键和范德华力都是微观粒子之间的不同作用力,下列物质:①Na2O2;
②SiO2;③碘;④金刚石;⑤NaCl;⑥白磷,其中含有两种作用力的组合是( )
A.①②⑤ B.①③⑥ C.②④⑥ D.①②③⑥
 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:
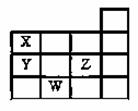
右图表示元素周期表中1~4周期的一部分,关于元素X、Y、Z、W 的 叙述错误的是 ( )
A.X、Y的最高价氧化物的水化物酸性为Y<X
B.Y、Z的气态氢化物的稳定性为Y<Z
C.Z有5种不同运动状态的电子
D.W的原子序数比Y大19
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:Fe2O3(s)+  C(s)====
C(s)====  CO2(g)+2Fe(s) ΔH=+234.1 kJ/mol
CO2(g)+2Fe(s) ΔH=+234.1 kJ/mol
C(s)+O2(g)====CO2(g) ΔH=-393.5 kJ/mol
则2Fe(s)+  O2(g)====Fe2O3(s)的ΔH是( )
O2(g)====Fe2O3(s)的ΔH是( )
A.-824.4 kJ/mol B.-627.6 kJ/mol C.-744.7 kJ/mol D.-169.4 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
氨在国民经济中占有重要地位。
(1)工业合成氨时,合成塔中每产生1 mol NH3,放出46.1 kJ的热量。
① 工业合成氨的热化学方程式是 。

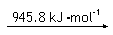 ② 已知:
② 已知:
N2 (g) 2N (g)
H2 (g) 2H (g)
则断开1 mol N-H键所需的能量是_______kJ。
(2)下表是当反应器中按n(N2):n(H2)=1:3投料后,在200℃、400℃、600℃下,反应达到平衡时,混合物中NH3的物质的量分数随压强的变化曲线。
|

① 曲线a对应的温度是 。
② 关于工业合成氨的反应,下列叙述正确的是 (填字母)。
A.及时分离出NH3可以提高H2的平衡转化率
B.加催化剂能加快反应速率且提高H2的平衡转化率
C.上图中M、N、Q点平衡常数K的大小关系是K(M)= K(Q) >K(N)
③ M点对应的H2转化率是 。
(3)氨是一种潜在的清洁能源,可用作碱性燃料电池的燃料。电池的总反应为:
4NH3(g) + 3O2(g) == 2N2(g) + 6H2O(g)。
则该燃料电池的负极反应式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质中都是既有离子键又有共价键的一组是( )
A.NaOH H2O NH4Cl B.KOH Na2O2 (NH4) 2S
C.MgO CaBr2 NaCl D.Na2SO4 HCl MgCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列能说明氯元素原子得电子能力比硫强的是( )
①HCl的溶解度比H2S大 ②HCl的酸性比H2S强③HCl的稳定性比H2S强 ④HCl的还原性比H2S强⑤HClO的酸性比H2SO4强 ⑥Cl2能与H2S反应生成S ⑦Cl2与铁反应生成FeCl3,而S与铁反应生成FeS ⑧还原性:Cl- <S2-
A.③④⑤⑧ B.③⑥⑦ C.③⑥⑦⑧ D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.有些物质是由原子直接构成,如金刚石、水晶等;有些物质是由分子直接构成,如干冰、氯化铵等;有些物质是由离子直接构成的,如食盐、烧碱等
B.BF3、H2O、SiCl4、PCl5四种分子中所有原子都满足最外层为8电子结构
C.非金属氧化物不都是酸性氧化物;碱性氧化物都是金属氧化物
D.硫单质的熔点比钠单质的熔点高,这是由于前者比后者有更大的范德华力所致
查看答案和解析>>
科目:高中化学 来源: 题型:
已知滤渣2的主要成分是Fe(OH)3和Al(OH)3,由滤渣2制取Al2(SO4)3·18H2O,该探究小组设计了如下实验方案:

下列关于此方案的说法,错误的是
A.加入NaOH溶液后过滤,滤渣为Fe(OH)3
B.也可以先加硫酸,再加NaOH溶液后蒸发、冷却、结晶、过滤
C.加硫酸后,溶液中的盐除含有硫酸铝外,还有硫酸钠
D.如果滤渣2中含1molAl(OH)3,则至少需要1molNaOH才能使Al(OH)3完全溶解
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com