

| A. | 在t1、t3℃时,NaCl和MgSO4的溶解度相等 | |
| B. | t2~t3℃,MgSO4的溶解度随温度升高而增大 | |
| C. | 在t2℃时,MgSO4饱和溶液的溶质质量分数最大 | |
| D. | 把MgSO4饱和溶液的温度从t2℃升至t3℃时,有晶体析出 |
分析 A.根据图象判断在t1℃、t3℃时NaCl、MgSO4的溶解度大小;
B.结合图象可知t2℃之后,随温度的升高而降低;
C.饱和溶液中溶质质量分数=w=$\frac{S}{100+S}$×100%,S越大,w越大;
D.t3℃的溶解度小于t2℃,把MgSO4饱和溶液的温度从t2℃升至t3℃时,会有晶体析出.
解答 解:A.根据图象可知,在t1℃、t3℃时,NaCl、MgSO4的溶解度相等,故A正确;
B.t2之前,MgSO4的溶解度随温度的升高而增大,t2之后,随温度的升高而降低,故B错误;
C.w=$\frac{S}{100+S}$×100%,S越大,w越大,在t2℃时,MgSO4饱和溶液的溶解度最大,则溶质质量分数也最大,故C正确;
D.把MgSO4饱和溶液的温度从t2℃升至t3℃时,硫酸镁的溶解度减小,则会有晶体析出,故D正确;
故选B.
点评 本题考查了溶质质量分数的计算、饱和溶液的判断,题目难度中等,明确饱和溶液特点为解答关键,注意掌握溶质质量分数的概念及计算方法,试题侧重考查学生分析图象的能力.


科目:高中化学 来源: 题型:选择题
| A. | 常温下,pH=7的NH4Cl和NH3•H2O的混合溶液中:c(Cl-)=c(NH4+)>c(OH-)=c(H+) | |
| B. | pH=12的氨水与pH=2的盐酸等体积混合溶液中:c(NH4+)>c(Cl-)>c(OH-)>c(H+) | |
| C. | 25℃时,0.1 mol•L-1pH=4.5的NaHSO3溶液中:c(HSO3-)>c(H2SO3)>c(SO32-) | |
| D. | 常温下,等浓度的CH3COONa和CH3COOH混合溶液:c(CH3COO-)-c(CH3COOH)=2[c(H+)-c(OH-)] |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、Cu2+、Cl-、SO42- | B. | Na+、AlO2-、NO3-、CH3COO- | ||
| C. | Na+、NH4+、NO3-、S2- | D. | Na+、Ag+、NO3-、Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使酚酞试液变红的溶液:Na+、Cl-、SO42-、Cu2+ | |
| B. | 在pH=1的溶液中:Fe2+、Mg2+、NO3-、ClO- | |
| C. | c(H+)=10-12 mol•L-1的溶液:Na+、S2-、AlO2-、SO32- | |
| D. | 使石蕊试液变红的溶液:K+、NH4+、I-、MnO4- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2O、MgO、Al2O3都是碱性氧化物 | |
| B. | 硬铝、黄铜、钢铁都属于合金 | |
| C. | 纤维素、硝化纤维、纤维二糖都是高分子 | |
| D. | 蔗糖、乙醇、液氯都是非电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 指定环境 | 能够共存的离子 |
| A | 滴加酚酞显红色的溶液 | K+、S2-、SO42-、NO3- |
| B | 有HCO3-存在的溶液 | Na+、K+、C1-、A13+ |
| C | pH=1的溶液中 | C1-、CO32-、NO3-、NH4+ |
| D | 使石蕊变红的溶液中 | Fe2+、MnO4-、NO3-、SO42- |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
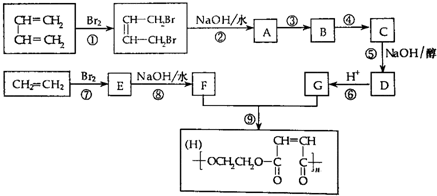
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | I-和IO-都是该反应的催化剂 | |
| B. | H2O2分解的速率取决于第二步反应的快慢 | |
| C. | 反应物的总能量比生成物总能量低98kJ | |
| D. | 第一步H2O2被还原,第二步H2O2被氧化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com