
| A. | 任何条件下,反应2CO2(g)═2CO(g)+O2(g)均不能自发进行 | |
| B. | 依据反应I2+2S2O32-═2I-+S4O62-,若要测定平衡体系I2+I-?I3-中平衡时的 c(I2),可用已知物质的量浓度的Na2S2O3溶液进行滴定实验 | |
| C. | 向含有苯酚的苯溶液中滴入少量浓溴水未见白色沉淀,是因为生成的三溴苯酚又溶于苯中 | |
| D. | 检验某物质是否含有Fe2O3的操作步骤是:样品粉碎→加水溶解→过滤,向滤液中滴加KSCN溶液 |
分析 A.该反应的△S>0,△H>0,△H-T△S<0的反应可自发进行;
B.I2+2S2O32-═2I-+S4O62-可使I2+I-?I3-平衡发生移动;
C.少量三溴苯酚可溶于苯中;
D.氧化铁不溶于水.
解答 解:A.该反应的△S>0,△H>0,△H-T△S<0的反应可自发进行,则2CO2(g)═2CO(g)+O2(g)高温下能自发进行,故A错误;
B.I2+2S2O32-═2I-+S4O62-可使I2+I-?I3-平衡发生移动,则不能测定平衡时的 c(I2),可测定体系中的 c(I2),故B错误;
C.少量三溴苯酚可溶于苯中,则向含有苯酚的苯溶液中滴入少量浓溴水未见白色沉淀,故C正确;
D.氧化铁不溶于水,应样品粉碎→加盐酸溶解→过滤,向滤液中滴加KSCN溶液,观察到血红色可说明,故D错误;
故选C.
点评 本题考查反应热与焓变,为高频考点,把握反应中能量变化、反应进行方向、离子检验为解答的关键,侧重分析与应用能力的考查,注意选项B为解答的难点,题目难度不大.


科目:高中化学 来源: 题型:填空题
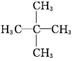 2,2-二甲基丙烷,写出它和氯气发生一取代反应的方程式
2,2-二甲基丙烷,写出它和氯气发生一取代反应的方程式 +Cl2$\stackrel{光照}{→}$
+Cl2$\stackrel{光照}{→}$ +HCl
+HCl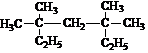 3,3,5,5-四甲基庚烷;它的一氯代物具有不同沸点的产物有4种
3,3,5,5-四甲基庚烷;它的一氯代物具有不同沸点的产物有4种 ;
; .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

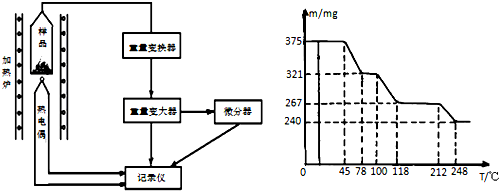
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
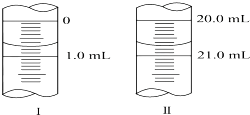 在分析化学中常用Na2C2O4晶体作为基准物质测定KMnO4溶液的浓度.在H2SO4溶液中,反应如下:
在分析化学中常用Na2C2O4晶体作为基准物质测定KMnO4溶液的浓度.在H2SO4溶液中,反应如下:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应①中电能转化为化学能 | |
| B. | 反应②为放热反应 | |
| C. | 反应③使用催化剂,△H3减小 | |
| D. | 反应CH4(g)=C(s)+2H2(g)的△H=+74.8 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、Mg2+、CO32-、I- | B. | H+、NO3-、Fe2+、Br- | ||
| C. | NH4+、K+、SO42-、Cl- | D. | Na+、S2-、Cu2+、SO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入少量Na2CO3固体,平衡①右移,平衡②左移,溶液中c(F-)增大 | |
| B. | 加入少量NaOH固体至c(F-)>c(HF),溶液一定呈碱性 | |
| C. | 加入少量Na至pH=8,则C(Na+)-c(F-)=0.99×10-7mol•L-1 | |
| D. | 加入少量盐酸,$\frac{c({F}^{-})}{c(HF)•c(O{H}^{-})}$不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2KMnO4+H2O2+3H2SO4═K2SO4+2MnSO4+3O2↑+4H2O | |
| B. | 2KMnO4+3H2O2+3H2SO4═K2SO4+2MnSO4+4O2↑+6H2O | |
| C. | 2KMnO4+5H2O2+3H2SO4═K2SO4+2MnSO4+5O2↑+8H2O | |
| D. | 8KMnO4+2H2O2+12H2SO4═4K2SO4+8MnSO4+11O2↑+14H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com