
下列有关溶液中微粒的物质的量浓度的关系,正确的是
A.0.1 mol·L-1的NH4Cl溶液与0.05 mol·L-1的NaOH溶液等体积混合的溶液:c(Cl-)>c(Na+)>c( )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
B.等物质的量的NaClO、NaHCO3混合溶液:c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)+c( )
)
C.pH=2的HA溶液与pH=12的MOH溶液等体积混合:c(M+)=c(A-)>c(OH-)=c(H+)
D.某二元弱酸的酸式盐NaHA溶液:c(OH-)+c(H2A)=c(H+)+2c(A2-)
B
【解析】
试题分析:A、0.1 mol·L-1的NH4Cl溶液与0.05 mol·L-1的NaOH溶液等体积混合的溶液,得到等浓度的氯化铵、一水合氨、氯化钠的混合液,溶液呈碱性,所以溶液中的离子浓度的大小关系是c(Cl-)> >c(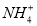 )>c(Na+)>c(OH-)>c(H+),错误;B、等物质的量的NaClO、NaHCO3混合溶液中,根据物料守恒,可得c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)+c(
)>c(Na+)>c(OH-)>c(H+),错误;B、等物质的量的NaClO、NaHCO3混合溶液中,根据物料守恒,可得c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)+c(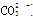 ),正确;C、因为酸、碱的强弱未知,所以混合后溶液的酸碱性不能确定,错误;D、根据质子守恒,应有c(OH-)=c(H+)-c(A2-)+ c(H2A),则c(OH-)+c(A2-)=c(H+)+c(H2A),错误,答案选B。
),正确;C、因为酸、碱的强弱未知,所以混合后溶液的酸碱性不能确定,错误;D、根据质子守恒,应有c(OH-)=c(H+)-c(A2-)+ c(H2A),则c(OH-)+c(A2-)=c(H+)+c(H2A),错误,答案选B。
考点:考查溶液混合的计算,离子浓度的比较,守恒规律的应用


科目:高中化学 来源:2014-2015学年甘肃省高一上学期期中化学试卷(解析版) 题型:选择题
某一化学兴趣小组的同学在家中进行实验,按照图甲连接好线路,发现灯泡没亮,但是按照图乙接好路线,灯泡亮了。由此得出的以下结论中正确的是

A.NaCl是非电解质
B.NaCl在水溶液中电离出了可以自由移动的离子
C.NaCl溶液是电解质
D.在NaCl溶液中,水电离出了大量的离子
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高三上学期期中考试化学试卷(解析版) 题型:选择题
将钠、铝混合物W1g投入一定量水中充分反应,金属没有剩余,共收集到标准状况下的气体V1L。向反应后的溶液中逐滴加入浓度为a mol·L-1的盐酸,在此过程中有白色沉淀生成后又逐渐溶解,当沉淀恰好消失时所加盐酸体积为V2L,将溶液蒸干、灼烧得固体W2g。下列关系式错误的是
A.35.5aV2=W2-W1 B.23n(Na)+27n(Al)=W1
C.n(Na)+3n(Al)=2V1/22.4 D.aV2=V1/11.2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高三上学期期中考试化学试卷(解析版) 题型:选择题
用氢氧化钠固体配制0.1 mol/L的氢氧化钠溶液,下列说法错误的是
A.定容时俯视,会造成浓度偏高
B.转移时不慎将转移液溅出,会造成浓度偏低
C.称量时托盘上要垫上干净的称量纸
D.定容摇匀后发现液面下降,不应继续加水
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省焦作市高三上学期期中化学试卷(解析版) 题型:填空题
(10分) CO2和CH4是两种重要的温室气体,通过CH4和CO2反应来制造更高价值的化学品是目前的研究目标。
(1)250 ℃时,以镍合金为催化剂,向体积为4 L的密闭容器中通入6 mol CO2、6 mol CH4,发生如下反应:CO2(g)+CH4(g) 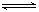 ?2CO(g)+2H2(g)。
?2CO(g)+2H2(g)。
平衡体系中各组分体积分数(某一成分物质的量占总气体物质的量的百分数)如下表:
物质 | CH4 | CO2 | CO | H2 |
体积分数 | 0.1 | 0.1 | 0.4 | 0.4 |
①此温度下该反应的平衡常数K=________。
②已知:CH4(g)+2O2(g)===CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1
CO(g)+H2O(g)===CO2(g)+H2(g) ΔH=+2.8 kJ·mol-1
2CO(g)+O2(g)===2CO2(g) ΔH=-566.0 kJ·mol-1
反应CO2(g)+CH4(g) ===?2CO(g)+2H2(g) ΔH=________。
(2)以二氧化钛表面覆盖Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸。
①在不同温度下催化剂的催化效率与乙酸的生成速率如下图所示。250~300 ℃时,乙酸的生成速率减小的原因是__________________________________________________。

②将Cu2Al2O4溶解在稀硝酸中的离子方程式为_______________________________。
(3)以CO2为原料可以合成多种物质。
如合成聚碳酸酯。已知CO2的分子结构为O===C===O,它的“C===O”双键与乙烯的“C===C”双键一样,在一定条件下可发生加聚反应,聚碳酸酯是一种易降解的新型合成材料,它是由CO2加聚而成。写出聚碳酸酯的结构简式:______________________________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省焦作市高三上学期期中化学试卷(解析版) 题型:选择题
实验室中某些气体的制取、收集及尾气处理装置如图所示。
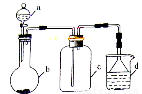
仅用此装置和表中提供的物质完成相关实验,最合理的是
选项 | a中物质 | b中物质 | c中收集的气体 | d中物质 |
A | 浓氨水 | CaO | NH3 | H2O |
B | 浓硫酸 | Na2SO3 | SO2 | NaOH溶液 |
C | 饱和食盐水 | 电石 | CH≡CH | H2O |
D | 浓盐酸 | MnO2 | Cl2 | NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省焦作市高三上学期期中化学试卷(解析版) 题型:选择题
能区别地沟油(加工过的餐饮废弃油)与矿物油(汽油、煤油、柴油等)的方法是
A.点燃,能燃烧的是矿物油
B.测定沸点,有固定沸点的是矿物油
C.加入水中,浮在水面上的是地沟油
D.加入足量氢氧化钠溶液共热,不分层的是地沟油
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省等四校高三上学期期中联考化学试卷(解析版) 题型:填空题
(8分)常温下,某水溶液M中存在的离子有:Na+、A2-、HA-、H+、OH-,存在的分子有H2O、H2A。根据题意回答下列问题:
(1)写出酸H2A的电离方程式_______ __ ___。
(2)若溶液M由10 mL 2 mol·L-1 NaHA溶液与2 mol·L-1 NaOH溶液等体积混合而得,
则溶液M的pH_ __7(填“>”、“<”或“=”),溶液中离子浓度由大到小顺序为_ _ __。
(3)若溶液M有下列三种情况:
①0.01 mol·L-1的H2A溶液
②0.01 mol·L-1的NaHA溶液
③0.02 mol·L-1的HCl与0.04 mol·L-1的NaHA溶液等体积混合液,
则三种情况的溶液中H2A分子浓度最大的为___ ___;pH由大到小的顺序为__ ____。
(4)若溶液M由pH=3的H2A溶液V1 mL与pH=11的NaOH溶液V2 mL混合反应而得,混合溶液c(H+)/c(OH-)=104,V1与V2的大小关系为___ _____(填“大于、等于、小于”或“均有可能”)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年云南省高三上学期第二次月考化学试卷(解析版) 题型:选择题
以下物质间的转化,不能通过一步反应实现的是
A.S→SO3→H2SO4 B.Al(OH)3→Al2O3→Al
C.Cu→CuCl2→Cu(OH)2 D.Na→Na2O2→Na2CO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com