
����Ŀ��Ϊ�˲ⶨij�����Ũ�ȣ���0.2molL��1��̼���Ʊ�Һ�������з�Ӧ��Ϊ����480mL�ı�Һ��ijͬѧ���������в�����������
��1����ҡ�Ⱥ���������ˮ���̶���1cm�������ý�ͷ�ιܼ�ˮ�� ֹ��Ȼ�����ƿ����������ָ�����Լ�ƿ�ڣ�
�����ձ���ע��Լ100mLˮ���ڽ����ºܿ��ܽ��꣮
��������ˮϴ�����ձ�3�Σ���ϴ��Һע���˷�Һ���ڣ�
�ܽ����º����Һ�ز�����ע�� �У� ������ƽ���� ��̼���Ʒ�ĩ������250mL���ձ��У�
��2����ͬѧ������ȷ��˳���� �����ţ�
��3����ͬѧ�IJ������������Ǵ��ģ����ţ�������������Һ��Ũ�� 0.2molL��1 �� ����=������������
���𰸡�
��1����Һ����ʹ���̶������У�500mL��10.6
��2���ݢڢܢۢ�
��3���ۣ���
���������⣺�ٶ���ʱ��ֱ�Ӽ�����ˮ����̶���1��2cm�����ý�ͷ�ι���εμӵ���Һ����ʹ���̶�������Ϊֹ��
���Դ��ǣ���Һ����ʹ���̶������У�����Ҫ480mL��Һ��Ӧѡ��500mL����ƿ����Ҫ���ʵ�����m=0.2molL��1��0.5L��106g/mol=10.6g��
���Դ��ǣ�10.6����1������һ�����ʵ�Ũ����Һ��һ�㲽��Ϊ�����㡢�������ܽ⡢��ȴ����Һ��ϴ�ӡ����ݡ�ҡ��װƿ��������ȷ��˳��Ϊ���ݢڢܢۢ٣�
���Դ��ǣ��ݢڢܢۢ٣���2��Ϊ��֤ʵ��ɹ���Ӧ����������ȫ��ת�Ƶ�����ƿ�����������ˮϴ�����ձ�3�Σ���ϴ��Һע���˷�Һ���ڣ��������ʲ�����ģ����ʵ����ʵ���ƫС������C= ![]() ��֪����ҺŨ��ƫ�ͣ����Ԣ۲�������Ӧ��ϴҺȫ��ת�Ƶ�����ƿ�У�
��֪����ҺŨ��ƫ�ͣ����Ԣ۲�������Ӧ��ϴҺȫ��ת�Ƶ�����ƿ�У�
���Դ��ǣ��ۣ�����
�����㾫�����������⣬������Ҫ�˽�����һ�����ʵ���Ũ�ȵ���Һ(�������ʵ���Ũ����Һʱ�������ձ�������ˮ������ƿ�̶���1cm��2cm���ٸ��ý�Ͷ�ιܼ�ˮ���̶���)��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����50mL NaNO3��Na2SO4�Ļ����Һ�У�c ��Na+��=1mol/L�������м�������BaCl2��Һǡ����ȫ��Ӧ���õ�2.33g��ɫ��������ԭ�����Һ��c ��NO3����=mol/L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���20.00mL 0.1000molL��1 ��NH4��2SO4��Һ����μ���0.2000molL��1 NaOHʱ����Һ��pH������NaOH��Һ����Ĺ�ϵ��ͼ��ʾ�������ǻӷ���������˵����ȷ���ǣ� �� 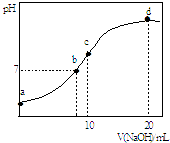
A.��a��ʾ��Һ�У�c��SO42������c��NH4+����c��H+����c��OH����
B.��b��ʾ��Һ�У�c��NH4+��=c��Na+����c��H+��=c��OH����
C.��d��ʾ��Һ�У�c��SO42������c��NH3H2O ����c��OH������c��NH4+��
D.��c��ʾ��Һ�У�c��SO42����+c��H+��=c��NH3H2O ��+c��OH����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й�������ƿ����ʹ�÷�������������ȷ����
��������һ�����ʵ���Ũ�ȵ���Һ��ר������
��ʹ��ǰҪ�ȼ������ƿ�Ƿ�©Һ
������ƿ������������
�ܲ���������ƿ�������ƺõ���Һ
�ݿ�����500mL����ƿ����250mL��Һ
A. �ٺ͢� B. �٢ڢ� C. ���ˢ� D. ���ˢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������岻��ȱ�ٵ���Ԫ�أ����뺬���Ļ�����ɲ��������������ơ����г���һ�ֳ����IJ���ҩ���ͼ1������˵���飺 
��ҩƷ��Fe2+�Ỻ�����������ҹ涨��ҩ����Fe2+�������ʳ���10%�������ٷ��ã�
��1��Ϊ�˼���ijҩ����۵ġ������ơ��Ƿ�������ʵ���ҿ�ѡ�õ�������������ļ����Լ�Ϊ�����Լ������ƣ���
��2��ʵ���Ҳ���H2SO4�ữ��KMnO4��Һ�ԡ������ơ��е�Fe2+���еζ�������ҩƷ�������ɷֲ���KMnO4��Ӧ�����÷�Ӧ�����ӷ���ʽΪ�� ��
��3��������������Ԫ����������Ϊ20.00%�ġ������ơ�19.00g������ȫ������ϡ�����У����Ƴ�1000.00mL��Һ��ȡ��20.00mL����0.01300mol/L��KMnO4��Һ�ζ�������KMnO4��Һ�����ͼ2��ʾ��
��ʵ��ǰ������Ҫ��ȷ����0.01300mol/L KMnO4��Һ250mL������ʱ��Ҫ�IJ������������������ձ�����ͷ�ι��⣬���� ��
��ijͬѧ�ĵζ���ʽ���гֲ�����ȥ����ͼ����������� �� 
����ͼ��֪����KMnO4��Һ���ΪmL��
�ܵζ��յ�۲쵽������Ϊ��
���Ա�KMnO4��Һ�ζ���Ʒ��Һ��Ũ�ȣ��ж����²���������ʵ����ƫС���� ��
A���ζ������У���ƿ��̫���ң�������Һ�ν���
B��δ�ñ�KMnO4��Һ��ϴ�ζ���
C���ζ��ӽ��յ�ʱ������������ˮ��ϴ��ƿ�ڱ�
D���ζ�ǰ���ӣ��ζ����ӣ���Һ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Һ��Cl2����������������Cl2+SO2+2H2O��2HCl+H2SO4����ͼ���йض����������ʵ�ʵ��װ��ͼ���Իش�����������
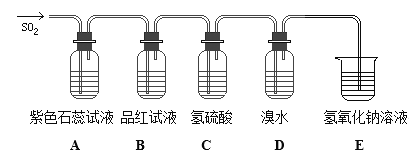
��1��A��B��C��D�ĸ�װ���з���������������________________��________________��_________________��__________________��
��2������������У���Ư���� ����������������� �ۻ�ԭ�� �������ԡ�����ͼ����װ���ж�Ӧ���ֳ��������ǣ�����ţ�
A��_______________B��______________C��________________D��________________��
��3��ʵ����ϣ���B����Һȡ�������Թ��У����ȣ�������_______________��ԭ���ǣ�________________________________��
��4��ʵ����ϣ�ȡ����D����Һ���Թ��У�����BaCl2��Һ��ϡ���ᣬ�����ǣ�_______________________________________________��
��5��E�з�����Ӧ�Ļ�ѧ����ʽΪ____________________________________________��
��6������һ����ʵ֤��Cl�ķǽ����Ա�Sǿ___________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���й����в�ҩ�ķ�Դ�أ�Ŀǰ�й���Լ��12000��ҩ��ֲ���ij�в�ҩ��ȡ���л���ṹ��ͼ��ʾ�����л��������˵���в���ȷ���ǣ� �� 
A.����ʽΪC14H18O6
B.������ԭ�ӵ�һ��ȡ����5��
C.1mol���л����������Ľ����Ʒ�Ӧ����4mol H2
D.���Ӽ��ܷ���������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������¡�0.2mol/L��һԪ��HA���Ũ�ȵ�NaOH��Һ�������Ϻ�����Һ���Ϊ����֮�ͣ���������Һ�в�������ּ�Ũ����ͼ��ʾ������˵������ȷ���ǣ� �� 
A.HA������
B.�û��ҺpH��7
C.�û����Һ�У�c��A����+c��Y��=c��Na+��
D.ͼ��X��ʾHA��Y��ʾOH�� �� Z��ʾH+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����200 mL��NaCl��MgCl2��KCl��ɵĻ��Һ�У���������Ũ�ȴ�С��ͼ��ʾ���ش��������⣺
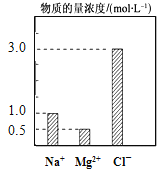
��1���û��Һ�У�NaCl�����ʵ�����Ũ��Ϊ molL������������MgCl2�����ʵ���Ϊ mol��
��2���û��Һ��KCl������Ϊ g��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com