

(1)写出两个阶段OA、AB反应的离子方程式。
OA段: ;
AB段: 。
(2)计算出A点、B点所对应的m、V以及沉淀的化学式,填在下面横线上。
V1= ,m1= ,沉淀的化学式 ;
V2= ,m2= ,沉淀的化学式 。
解析:含0.02 mol Al3+的明矾溶液,含n(![]() )=0.02mol×2=0.04 mol。向其中加入Ba(OH)2,刚开始生成BaSO4和Al(OH)3,至Al3+完全沉淀,消耗V〔Ba(OH)2〕=
)=0.02mol×2=0.04 mol。向其中加入Ba(OH)2,刚开始生成BaSO4和Al(OH)3,至Al3+完全沉淀,消耗V〔Ba(OH)2〕=![]() =
=![]() )=0.04 mol-0.2 mol·L-1×
)=0.04 mol-0.2 mol·L-1×![]() 逐渐沉淀至完全。由于此过程中溶解m〔Al(OH)3〕=0.02 mol×
逐渐沉淀至完全。由于此过程中溶解m〔Al(OH)3〕=0.02 mol×
答案:(1)3Ba2++6OH-+2Al3++3![]()
![]() 3BaSO4↓+2Al(OH)3↓
3BaSO4↓+2Al(OH)3↓
2Al(OH)3+![]() +Ba2++2OH-
+Ba2++2OH-![]() BaSO4↓+2
BaSO4↓+2![]() +4H2O
+4H2O
(2)150 mL 8.55 g Al(OH)3、BaSO4
200 mL 9.32 g BaSO4


科目:高中化学 来源:上海市杨浦区2011届高三一模化学试题 题型:038
科研人员发现,一些化学反应在固体之间发生和在水溶液中发生,产物不同.
铜合金是人类使用最早的金属材料,铜在化合物中的常见化合价有+1、+2.
将CuCl2·2H2O晶体和NaOH固体混合研磨,生成物中有一黑色的固体A.A不溶于水,但可溶于稀硫酸生成蓝色溶液B.
(1)A的化学式为________;A不同于CuCl2和NaOH在溶液中反应所得产物的可能原因是________.
(2)在含0.02 mol B的溶液中加入适量氨水恰好完全反应,得到浅蓝色沉淀C和无色的溶液D;C溶于盐酸后,加入足量的BaCl2溶液,生成2.33 g白色沉淀;无色的溶液D中加入足量的NaOH,加热收集到无色有刺激性气味的气体E.
①通过计算确定C的化学式.
②E是________(填物质名称),E在标准状况下的体积为________mL.
(3)若向B中加过量氨水后,再通入SO2至微酸性,最终得到白色沉淀F和无色的溶液.分析知,F是不含结晶水的复盐,其部分元素的质量分数为:Cu 39.31%、S 19.84%、N 8.67%.
①通过计算确定F的化学式.
②写出由B生成F的化学方程式.
(4)将F与中等浓度的硫酸混合加热,会放出无色有刺激性气味的气体,析出紫红色沉淀,同时得到蓝色的溶液.写出该反应的化学方程式.
查看答案和解析>>
科目:高中化学 来源: 题型:

(1)写出两个阶段OA、AB反应的离子方程式。
OA段:________________________________;
AB段:________________________________。
(2)计算出A点、B点所对应的m和V,填在下面横线上。
V1=_____________________,m1=________________________;
V2=_____________________,m2=________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
V1=_______________ V2=_______________
m1_________________ m2=_______________

查看答案和解析>>
科目:高中化学 来源: 题型:
向含0.02 mol Al3+的明矾溶液中逐滴加入0.2 mol·L-1的Ba(OH)2溶液时,测得产生沉淀的质量m和逐滴加入的Ba(OH)2溶液的体积V的关系如右图所示。
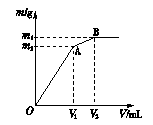
(1)写出两个阶段OA、AB反应的离子方程式。
OA段: ;
AB段: 。
(2)计算出A点、B点所对应的m、V以及沉淀的化学式,填在下面横线上。
V1= ,m1= ,沉淀的化学式 ;
V2= ,m2= ,沉淀的化学式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com