
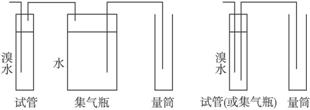
(1)混合气体进入反应管后,量气管内增加的水的体积等于_____的体积。(填写气体的化学式)
(2)反应管内溶液蓝色消失后,没有及时停止通气,则测得的SO2含量_________。(选填“偏高”“偏低”“不受影响”)
(3)反应管内的碘的淀粉溶液也可以用_________代替。(填写物质名称)
(4)若碘溶液体积为Va mL,浓度为c mol·L-1,N2与O2的体积为Vb mL(已折算为标准状况下的体积)。用c、Va、Vb表示SO2的体积百分含量为_________。
(5)将上述装置改为简易实验装置,除导管外,还需用的仪器为________(选下列仪器的编号)。
a.烧杯 b.试管 c.广口瓶 d.容量瓶 e.量筒 f.单孔塞 g.双孔塞
解析:(1)SO2、N2、O2混合气体进入反应管,SO2被吸收,气体体积的膨胀值即量气管内增加的水的体积,等于N2和O2的体积。
(2)根据下列反应:
SO2+I2+2H2O![]() H2SO4+2HI
H2SO4+2HI
可求出吸收的SO2的体积:
V(SO2)=Vm×n(I2)
SO2的体积百分含量,可如下求出:
φ(SO2)=V(SO2)/V(混合气体)
式中V(SO2)的量是由n(I2)的物质的量决定的,而“没有及时停止通气”就会使得V(混合气体)增大,则φ(SO2)偏低。
(3)反应管内的磺的淀粉溶液可以用能吸收SO2的有色溶液代替,中学常见且可用的是溴水(或溴的四氯化碳溶液)或高锰酸钾酸性溶液。
(4)由(2)中分析,易得出答案:
φ(SO2)=22.4cVa/(22.4cVa+Vb)
(5)可组合为如下图简笔画所示的装置:

可以是bceg或beg或ceg等组合。
答案:(1)N2和O2 (2)偏低
(3)溴水(或溴的四氯化碳溶液)或高锰酸钾酸性溶液
(4)22.4cVa/(22.4cVa+Vb)
(5)bceg或beg或ceg


科目:高中化学 来源: 题型:
(13分)
空气质量高低直接影响着人类的生产和生活,它越来越受到人们的关注。被污染的空气中杂质的成分有多种,其中计入《空气质量日报》空气污染指数的项目有SO2、CO、NO2、O3和可吸入颗粒物等。
请回答下列问题:
(1)S、N、O的的第一电离能由大到小的顺序为 。
(2)SO2、CO、NO2、O3常温下均为气体,固态时均属于 晶体。
(3)随着人们生活质量的提高,室内的环境安全和食品安全越来越为人们所关注。甲醛(HCHO)是室内主要空气污染物之一(其沸点是–19.5 ℃),甲醇(CH3OH)是“假酒”中的主要有害物质(其沸点是64.65 ℃)。甲醛分子中C原子采取 杂化轨道方式。甲醇的沸点明显高于甲醛的主要原因是:__________ 。
(4)CuCl的盐酸溶液能够与CO发生反应:CuCl+CO+H2O=Cu(CO)Cl·H2O,该反应可用于测定空气中CO含量。
①写出铜原子的基态电子排布式 。
②CuCl的晶体结构如下图甲所示,与同一个Cl-距离最近的相邻Cu+有 个。
③Cu(CO)Cl·H2O的结构如上图乙所示,图中标示出8个是共价键,其中6个是配位键,请在图中用箭头标示出。
查看答案和解析>>
科目:高中化学 来源: 题型:
(15分)现用下图所示装置及所给药品探究工业制硫酸时二氧化硫的转化率。已知C中含硫酸n mol,设气体进入C和D时能分别完全吸收某一种气体,且忽略装置内空气中的CO2。
请回答下列问题:
(1)检查完装置的气密性且加入药品后,开始进行时首先应进行的操作是
。
(2)通过观察中气泡的逸出速率可控制SO2和O2的流量和体积比,A装置还起的作用有 。
(3)为了提高测定SO2转化率的准确度,下列操作或改进可行的是(填序号) 。
①熄灭酒精灯后,停止通入SO2,继续通入O2一段时间
②熄灭酒精灯后,停止通入O2,继续通入SO2一段时间
③在C、D之间加装一个盛有浓硫酸的洗气瓶
(4)若气体经过充分,实验结束后,稀释装置C中的溶液,并向其中加入足量的BaCl2溶液,得到的沉淀质量为w g。若装置D增加的质量为a g,则二氧化硫的转化率是:
(用含字母的代数式表示,结果可不化简)。
(5)若向接触室中通入2 molSO2(g)和1molO2(g),在一定温度下,反应达到平衡时测得接触室内的压强为起始时的0.75倍,则SO2的转化率为 ;相同条件下,当起始时同时通入a mol SO2、bmol O2、c mol SO3(g)时,达到平衡时与原平衡等效,且起始时维持化学反应向逆反应方向进行,则c的取值范围为 。
查看答案和解析>>
科目:高中化学 来源:2011届福建省三明二中高三第二次模拟考试(理综)化学试题 题型:填空题
空气质量高低直接影响着人类的生产和生活,它越来越受到人们的关注。被污染的空气中杂质的成分有多种,其中计入《空气质量日报》空气污染指数的项目有SO2、CO、NO2、O3和可吸入颗粒物等。
请回答下列问题:
(1)S、N、O的的第一电离能由大到小的顺序为 。
(2)SO2、CO、NO2、O3常温下均为气体,固态时均属于 晶体。
(3)随着人们生活质量的提高,室内的环境安全和食品安全越来越为人们所关注。甲醛(HCHO)是室内主要空气污染物之一(其沸点是–19.5 ℃),甲醇(CH3OH)是“假酒”中的主要有害物质(其沸点是64.65 ℃)。甲醛分子中C原子采取 杂化轨道方式。甲醇的沸点明显高于甲醛的主要原因是:
__________ 。
(4)CuCl的盐酸溶液能够与CO发生反应:CuCl+CO+H2O=Cu(CO)Cl·H2O,该反应可用于测定空气中CO含量。
①写出铜原子的基态电子排布式 。
②CuCl的晶体结构如下图甲所示,与同一个Cl-距离最近的相邻Cu+有 个。
③Cu(CO)Cl·H2O的结构如上图乙所示,图中标示出8个是共价键,其中 个是配位键,
查看答案和解析>>
科目:高中化学 来源:2010-2011学年福建省莆田市高三适应性练习(理综)化学部分 题型:填空题
(13分)
空气质量高低直接影响着人类的生产和生活,它越来越受到人们的关注。被污染的空气中杂质的成分有多种,其中计入《空气质量日报》空气污染指数的项目有SO2、CO、NO2、O3和可吸入颗粒物等。
请回答下列问题:
(1)S、N、O的的第一电离能由大到小的顺序为 。
(2)SO2、CO、NO2、O3常温下均为气体,固态时均属于 晶体。
(3)随着人们生活质量的提高,室内的环境安全和食品安全越来越为人们所关注。甲醛(HCHO)是室内主要空气污染物之一(其沸点是–19.5 ℃),甲醇(CH3OH)是“假酒”中的主要有害物质(其沸点是64.65 ℃)。甲醛分子中C原子采取 杂化轨道方式。甲醇的沸点明显高于甲醛的主要原因是:__________ 。
(4)CuCl的盐酸溶液能够与CO发生反应:CuCl+CO+H2O=Cu(CO)Cl·H2O,该反应可用于测定空气中CO含量。
①写出铜原子的基态电子排布式 。
②CuCl的晶体结构如下图甲所示,与同一个Cl-距离最近的相邻Cu+有 个。

③Cu(CO)Cl·H2O的结构如上图乙所示,图中标示出8个是共价键,其中6个是配位键,请在图中用箭头标示出。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com