
| A. | Al2O3→NaAlO2 | B. | Cl2→HClO | C. | Al2O3→Al(OH)3 | D. | H2SO4(浓)→SO2 |
分析 A.Al与NaOH反应生成NaAlO2;
B.氯气与水反应生成HClO;
C.Al2O3不能与水或碱反应生成Al(OH)3;
D.浓硫酸与Cu在加热条件下反应生成二氧化硫.
解答 解:A.Al与NaOH反应生成NaAlO2,发生2Al+2NaOH+2H2O=2NaAlO2+3H2↑,一步转化可实现,故A不选;
B.氯气与水反应生成HClO,发生Cl2+H2O=HCl+HClO,一步转化可实现,故B不选;
C.Al2O3不能与水或碱反应生成Al(OH)3,不能实现一步转化,故C选;
D.浓硫酸与Cu在加热条件下反应生成二氧化硫,发生Cu+2H2SO4(浓)$\frac{\underline{\;加热\;}}{\;}$CuSO4+SO2↑+2H2O,一步转化可实现,故D不选;
故选C.
点评 本题考查物质的性质,综合考查元素化合物知识,把握物质的性质及发生的化学反应为解答的关键,侧重分析与应用能力的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | ③→⑧→①←④→⑨ | B. | ⑦→③→⑥→①←④→⑨→② | C. | ②→⑨→④→①←⑥←③ | D. | ②→④→⑤→①←⑥←③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA |
| 1 | ① | ||||||
| 2 | ② | ③ | ④ | ⑤ | ⑥ | ||
| 3 | ⑦ | ⑧ | ⑨ | ⑩ |
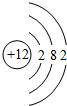 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
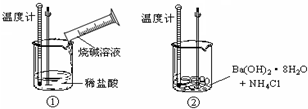
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
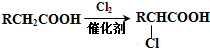
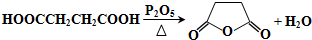
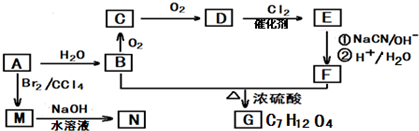
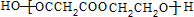 +(2n-1)H2O.
+(2n-1)H2O.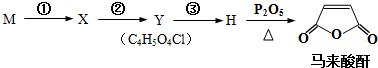
| 序号 | 所加试剂及条件 | 反应类型 |
| ② | ||
| ③ | , |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③⑤ | B. | ①③⑤⑦ | C. | ②③④⑤⑦ | D. | ①③⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 2015年8月12号接近午夜时分,天津滨海新区一处集装箱码头发生爆炸.发生爆炸的是集装箱内的易燃易爆物品,爆炸火光震天,并产生巨大蘑菇云.根据掌握的信息分析,装箱区的危险化学品可能有钾、钠、氯酸钠、硝酸钾、烧碱,硫化碱、硅化钙、三氯乙烯、氯碘酸等.运抵区的危险化学品可能有环己胺、二甲基二硫、甲酸、硝酸铵、氰化钠、4,6-二硝基苯-邻仲丁基苯酚等.
2015年8月12号接近午夜时分,天津滨海新区一处集装箱码头发生爆炸.发生爆炸的是集装箱内的易燃易爆物品,爆炸火光震天,并产生巨大蘑菇云.根据掌握的信息分析,装箱区的危险化学品可能有钾、钠、氯酸钠、硝酸钾、烧碱,硫化碱、硅化钙、三氯乙烯、氯碘酸等.运抵区的危险化学品可能有环己胺、二甲基二硫、甲酸、硝酸铵、氰化钠、4,6-二硝基苯-邻仲丁基苯酚等.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com