
| A、用饱和NaHCO3溶液除去CO2中混有的HCl |
| B、用加热蒸干AlCl3溶液的方法制备无水AlCl3固体 |
| C、用分液漏斗分离CCl4萃取碘水后已分层的有机层和水层 |
| D、用加热分解的方法区分碳酸钠和碳酸氢钠两种固体 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原溶液的浓度为0.1mol/L |
| B、反应后溶液中c(Fe3+)=0.1mol/L |
| C、原溶 液中c(Br?)=0.4mol/L |
| D、反应后溶液中c(Fe3+)=c(Fe2+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在组装蒸馏装置时,温度计的水银球应伸入液面下 |
| B、用96%的工业酒精制取无水乙醇,可采用的方法是加生石灰,再蒸馏 |
| C、在苯甲酸重结晶实验中,粗苯甲酸加热溶解后还要加少量蒸馏水 |
| D、分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验操作及现象 | 实验目的或结论 |
| A | 向1,2两试管中分别加入等浓度H2O2溶液10 mL、1 mL,再向H2O2溶液中分别滴入等浓度等体积CuSO4、FeCl3溶液;试管2中产生气体较快 | 证明FeCl3溶液的催化效率 更高 |
| B | 硅酸钠溶液中滴入酚酞,溶液变红,再滴加稀盐酸,溶液红色变浅直至消失 | 证明非金属性:Cl>Si |
| C | 测定物质的量浓度相同的盐酸和醋酸溶液的pH;盐酸pH小于醋酸pH | 证明盐酸酸性比醋酸强 |
| D | 取5 mL,0.1mol/L的AgNO3溶液于试管中,向试管中加入1-2滴0.1mol/L的NaCl溶液,出现白色沉淀,再向该试管中加入2滴0.1mol/L的KI溶液,出现黄色沉淀(AgI沉淀为黄色). | 证明: Ksp(AgI)<Ksp(AgCl) |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验操作 | 实验现象 | 解释或结论 |
| A | 把S02通入紫色石蕊试液中 | 紫色褪去 | S02具有漂白性 |
B | 向NaOH溶液中滴加足量的MgCl2溶液,然后再滴加足量的CuCl2溶液 | 先产生白色沉淀,然后沉淀变蓝色 | Ksp[Cu(OH)2]>Ksp[Mg(OH)2] |
| C | 向某溶液中滴加KSCN溶液 | 溶液变红色 | 溶液中含有Fe2+ |
| D | 将充满N02的密闭玻璃球浸泡在热水中 | 红棕色变深 | 反应2NO2(g)?N2O4(g)的△H<0 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②④⑤ | B、①③⑤⑥ |
| C、①④⑤⑥ | D、②③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
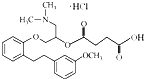 ),是改善慢性动脉闭塞症所引起的溃疡、疼痛以及冷感等缺血性诸症状的一种药物.其合成路线如下:
),是改善慢性动脉闭塞症所引起的溃疡、疼痛以及冷感等缺血性诸症状的一种药物.其合成路线如下: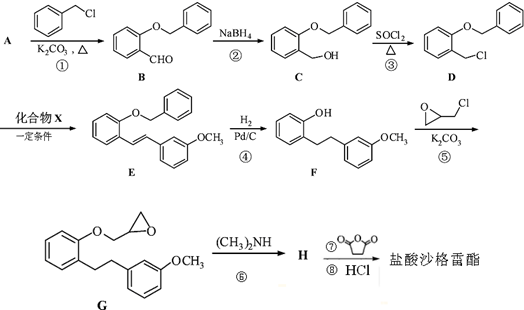
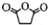 是丁二酸酐
是丁二酸酐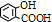 ),分析该制备过程的关键所在
),分析该制备过程的关键所在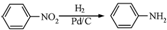 .化合物
.化合物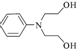 是合成抗癌药物的中间体,请写出以
是合成抗癌药物的中间体,请写出以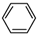 和
和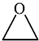 为原料制备该化合物的合成路线流程图(无机试剂任用).
为原料制备该化合物的合成路线流程图(无机试剂任用).| HBr |
| NaOH溶液 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com