
已知:I2+2S2O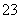 ===S4O
===S4O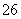 +2I-
+2I-
相关物质的溶度积常数见下表:
| 物质 | CuCl | CuI |
| Ksp | 1.7×10-7 | 1.3×10-12 |
某学习小组用“间接碘量法”测定含有CuCl2·2H2O晶体的试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下:取0.36 g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀。用0.100 0 mol·L-1 Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00 mL。
①可选用________作滴定指示剂,滴定终点的现象是__________________________。
②CuCl2溶液与KI反应的离子方程式为______________________________________。
③该试样中CuCl2·2H2O的质量百分数为__________。
科目:高中化学 来源: 题型:
下图 为直流电,
为直流电, 为浸透饱和氯化钠溶液和酚酞试液的滤纸,
为浸透饱和氯化钠溶液和酚酞试液的滤纸, 为电镀槽,接通电路后发现
为电镀槽,接通电路后发现 上的c点显红色,为实现铁上镀锌,接通
上的c点显红色,为实现铁上镀锌,接通 后,使c、d两点短路.下列叙述正确的是
后,使c、d两点短路.下列叙述正确的是
A.a为直流电的负极
B.c极发生的反应为2H++2e-=H2↑
C.f电极为锌板
D.e极发生还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
有一固体粉末,其中可能含有Na2CO3、NaCl、Na2SO4、CuCl2、Ba(NO3)2、K2CO3、K2SO4中的一种或几种,现按下列步骤进行实验。
①将该粉末溶于水得无色溶液和白色沉淀。
②在滤出的沉淀中加入稀硝酸,有部分沉淀溶解,同时产生无色气体。
③取滤液做焰色反应,可证明滤液中含Na+,不含K+。
由上述现象推断:
(1)该混合物中一定含有 ;一定不含有 ,可能含有 。
(2)如要检验其是否存在,将如何操作 。
查看答案和解析>>
科目:高中化学 来源: 题型:
以下各组离子在该溶液中能大量共存的有 ( )
A. 滴加石蕊试液显红色的溶液:Fe3+、NH4+、CO32- 、I-
B. pH值为1的溶液:Cu2+、Na+、Mg2+、NO3-
C. 水电离出来的c(H+)=10-13mol/L的溶液:K+、HCO3-、Cl-、Ba2+
D. 所含溶质为Na2CO3的溶液:K+、Na+、NO3-、Al3+
查看答案和解析>>
科目:高中化学 来源: 题型:
在恒温、恒容的条件下,有反应2A(气)+2B(气)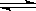 C(气)+3D(气),现从两条途径分别建立平衡。途径I:A、B的起始浓度分别为2mol/L
C(气)+3D(气),现从两条途径分别建立平衡。途径I:A、B的起始浓度分别为2mol/L
途径Ⅱ:C、D的起始浓度分别为2mol/L 和6mol/L;则以下叙述中正确的是( )
A.两途径最终达到平衡时,体系内混合气体各组分百分组成相同
B.两途径最终达到平衡时,体系内混合气体各组分百分组成不同
C.达到平衡时,途径I的反应速率等于途径Ⅱ的反应速率
D.达到平衡时,途径I所得混合气的密度等于途径Ⅱ所得混合气密度
查看答案和解析>>
科目:高中化学 来源: 题型:
某硫酸镁和硫酸铝的混合溶液中,c(Mg2+)=2 mol·L-1,c(SO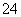 )=6.5 mol·L-1,若将
)=6.5 mol·L-1,若将
200 mL此混合液中的Mg2+和Al3+ 分离,至少应加入1.6 mol·L-1的苛性钠溶液( )
A.0.5 L B.1.625 L C.1.8 L D.2 L
查看答案和解析>>
科目:高中化学 来源: 题型:
含有砒霜(As2O3)的试样和锌、盐酸混合反应,生成的砷化氢(AsH3)在热玻璃管中完全分解成单质砷和氢气。若砷的质量为1.50mg,则
A.被氧化的砒霜为1.98mg
B.分解产生的氢气为0.672ml
C.和砒霜反应的锌为3.90mg
D.转移的电子总数为6×10—5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
将0.34 g Cu和CuO的混合物加入约12 mol·L-1浓硫酸中,并加热使其完全溶解,然后用NaOH溶液中和过量硫酸,再用水稀释到0.5 L,加入纯铁粉1.85 g,反应后过滤、干燥,得不溶物1.89 g。求置换出的铜的质量及原混合物中铜的质量分数。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关叙述正确的是
A.碱性锌锰电池中,MnO2 是催化剂
是催化剂
B.银锌纽扣电池工作时,Ag2O被还原为Ag
C.放电时,铅酸蓄电池中硫酸浓度不断增大
D.电镀时,待镀的金属制品表面发生还原反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com