
明矾石是制取钾肥和氢氧化铝的重要原料,明矾石的组成和明矾[KAl(SO4)2?12H2O]相似,此外还含有氧化铝和少量氧化铁杂质。具体实验步骤如下图所示: 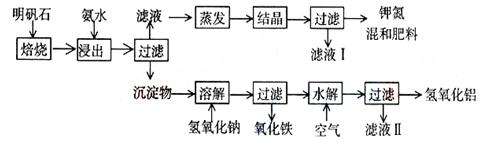
根据上述图示,完成下列填空:
(1)明矾石焙烧后用稀氨水浸出。配制500ml稀氨水(每升含有39.00g氨)需要取浓氨水(每升含有250g氨)__________ml,用规格为_______ml量筒量取。
(2)氨水浸出后得到固体混合体系,过滤,滤液中除K+、SO42-外,还有大量的NH4+。检验NH4+的方法是_______________________________________________________。
(3)写出沉淀物中所有物质的化学式________________________________________。
(4)滤液的成分是水和______________。
(5)为测定混合肥料K2SO4、(NH4)2SO4中钾的含量,请完善下列步骤:
①称取钾氮肥试样并溶于水,加入足量______溶液,产生白色沉淀。②_______、______、干燥(填实验操作名称)。③冷却、称重。
(6)若试样为mg,沉淀的物质的量为n mol,则试样中K2SO4的物质的量为:______(用含有m、n的代数式表示)。
(1)78;100(各1分,共2分)
(2)取滤液少许,加入NaOH,加热,生成的气体能使湿润的红色石蕊试纸变蓝。(3分)
(3)Al(OH)3;Al2O3;Fe2O3(3分) (4)K2SO4;(NH4)2SO4(2分)
(5)BaCl2(其他合理答案也给分);过滤;洗涤;(3分) (6)  mol(2分)
mol(2分)
解析试题分析:(1)配制500mL稀氨水(每升含有39.00g氨),需要使用500mL容量瓶,需要浓氨水(每升含有250.00g氨)的体积为: =0.078L=78mL。依据规格对应的原则可知,要量取78ml溶液有关选择100ml量筒。
=0.078L=78mL。依据规格对应的原则可知,要量取78ml溶液有关选择100ml量筒。
(2)铵盐能与强碱反应放出碱性气体氨气,据此可以检验,即可以使用氢氧化钠和红色石蕊试纸进行检验,具体检验NH4+的方法为:取滤液少许,加入NaOH加热,生成的气体能使润湿的红色石蕊试纸变蓝。
(3)明矾石的组成和明矾相似,所以能够与氨水反应生成氢氧化铝沉淀,还含有氧化铝和少量氧化铁杂质不与氨水反应也不溶于水,所以沉淀物为:Al(OH)3;Al2O3;Fe2O3。
(4)明矾石的组成和明矾相似,根据工艺流程转化关系可知,滤液I中含有K2SO4和反应生成(NH4)2SO4。
(5)混合肥料中含有K2SO4、(NH4)2SO4,要产生白色沉淀,加入的溶液为BaCl2或Ba(NO3)2溶液;然后进行操作:先将混合液过滤,然后洗涤沉淀,最后干燥,冷却后称重。
(6)试样为mg,则174n(K2SO4)+132n[(NH4)2SO4]=m,沉淀的物质的量为nmol,即BaSO4的物质的量为nmol,根据硫酸根守恒有:n(K2SO4)+n[(NH4)2SO4]=n,联立解得,n(K2SO4)= mol。
mol。
考点:考查学生对工艺流程的理解、离子的检验与共存、物质分离提纯等基本操作、物质性质与化学用语、化学计算等


 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案科目:高中化学 来源: 题型:填空题
将一块铝硅合金恰好与NaOH溶液完全反应而溶解。
(1)写出合金溶解的离子方程式______________________________________________。
(2)向所得的溶液中加入足量的盐酸,充分反应后,溶液中大量存在的离子为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
合金是建造航空母舰的主体材料。
(1)航母升降机可由铝合金制造。
①铝元素在周期表中的位置为________。工业炼铝的原料由铝土矿提取而得,提取过程中通入的气体为________。
②Al-Mg合金焊接前用NaOH溶液处理Al2O3膜,其化学方程式为____________________________________。
焊接过程中使用的保护气为________(填化学式)。
(2)航母舰体材料为合金钢。
①舰体在海水中发生的电化学腐蚀主要为________。
②航母用钢可由低硅生铁冶炼而成,则在炼铁过程中为降低硅含量需加入的物质为________。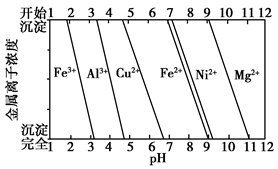
(3)航母螺旋桨主要用铜合金制造。
①80.0 g Cu-Al合金用酸完全溶解后,加入过量氨水,过滤得白色沉淀39.0 g,则合金中Cu的质量分数为________。
②为分析某铜合金的成分,用酸将其完全溶解后,用NaOH溶液调节pH,当pH=3.4时开始出现沉淀,分别在pH为7.0、8.0时过滤沉淀,结合题图信息推断该合金中除铜外一定含有________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
明矾石经处理后得到明矾[KAl(SO4)2·12H2O]。从明矾制备Al、K2SO4和H2SO4的工艺过程如下所示: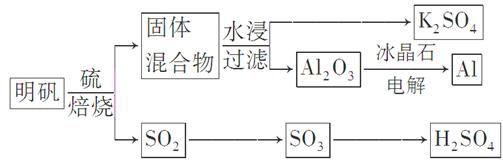 焙烧明矾的化学方程式为:4KAl(SO4)2·12H2O+3S=2K2SO4+2Al2O3+9SO2↑+48H2O
焙烧明矾的化学方程式为:4KAl(SO4)2·12H2O+3S=2K2SO4+2Al2O3+9SO2↑+48H2O
请回答下列问题:
(1)在焙烧明矾的反应中,还原剂是________。
(2)从水浸后的滤液中得到K2SO4晶体的方法是________。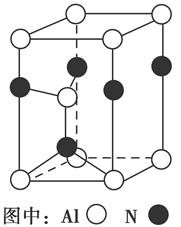
(3)Al2O3在一定条件下可制得AlN,其晶体结构如右图所示,该晶体中Al的配位数是________。
(4)以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2,该电池反应的化学方程式是________。
(5)焙烧产生的SO2可用于制硫酸。已知25℃、101 kPa时:
2SO2(g)+O2(g) 2SO3(g) ΔH1=-197 kJ/mol;
2SO3(g) ΔH1=-197 kJ/mol;
H2O(g)=H2O(l) ΔH2=-44 kJ/mol;
2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l) ΔH3=-545 kJ/mol。
则SO3(g)与H2O(l)反应的热化学方程式是________。焙烧948 t明矾(M=474 g/mol),若SO2的利用率为96%,可生产质量分数为98%的硫酸________t。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
工业上用铝土矿(成分为氧化铝、氧化铁)制取铝的流程如下:
请回答下列问题。
(1)操作Ⅰ、操作Ⅱ、操作Ⅲ都用到的玻璃仪器有________________________________。
(2)写出由溶液B生成Al(OH)3的离子方程式:_________________________________________________________。
(3)工艺流程中涉及氧化还原反应的化学方程式为______________________________________________________________________。
(4)生产过程中,除NaOH、H2O可以循环使用外,还可以循环使用的物质有________(填化学式)。用此法制取铝的副产品是________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
某化学兴趣小组用铝土矿(主要成分为A12 O3,还含有SiO2及铁的氧化物)提取氧化铝作冶炼铝的原料,提取的操作过程如下: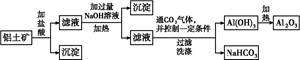
(1)在过滤操作中,除烧杯、玻璃棒外,还需用到的玻璃仪器有 ;洗涤沉淀的操作是 。
(2)实验室制备氢氧化铝的方案有多种。现提供铝屑、氢氧化钠溶液、稀硫酸三种药品,若制备等量的氢氧化铝,请你从药品用量最少的角度出发,设计出最佳实验方案(方案不必给出),写出此方案中发生反应的离子方程式: ,此方案中所用药品的物质的量之比是:n(Al)∶n(H2SO4)∶n(NaOH) = 。
(3)兴趣小组欲对铝土矿中铁元素的价态进行探究:取少量固体,加入过量稀硝酸,加热溶解;取少许溶液滴加KSCN溶液后出现红色。由此得出铁元素的价态为+3的结论。请指出该结论是否合理并说明理由 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
某工业废渣的主要成分为SiO2、Fe2O3、Al2O3、MgO。现根据下列方案对其进行处理以回收废渣中的金属元素。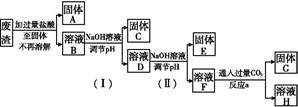
回答下列问题。
(1)固体A的化学式为 。
(2)反应a的化学反应方程式为 。
(3)25 ℃时,溶液中金属离子的物质的量浓度与溶液pH的关系如图所示: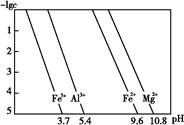
①调节pH(Ⅰ)的pH为 ;
②溶液D加入氢氧化钠溶液的同时调节pH(Ⅱ)所发生反应的离子方程式为 ;
③从图中数据计算可得Mg(OH)2的溶度积Ksp[Mg(OH)2]约为 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
用含少量铁的氧化铜制取氯化铜晶体(CuCl2·xH2O)。有如下操作:
已知:在pH为4~5时,Fe3+几乎完全水解而沉淀,而此时Cu2+却几乎不水解。
(1)氧化剂A可选用 (填编号,下同)。
①Cl2 ②H2O2 ③HNO3 ④KMnO4
(2)要得到较纯的产品,试剂B可选用 。
①NaOH ②FeO ③CuO ④Cu2(OH)2CO3
(3)从滤液经过结晶得到氯化铜的方法是 (按实验先后顺序填编号)。
①过滤 ②冷却 ③蒸发浓缩 ④蒸发至干
(4)为了测定制得的氯化铜晶体(CuCl2·xH2O)中x值,某兴趣小组设计了两种实验方案:
方案一:称取m g晶体灼烧至质量不再减轻为止,冷却、称量所得无水CuCl2的质量为n g。
方案二:称取m g晶体,加入足量10%的氢氧化钠溶液、过滤、洗涤后用小火加热至质量不再减轻为止,冷却、称量所得固体的质量为n g。
①方案一中灼烧CuCl2·xH2O得到无水CuCl2,应在 (填仪器名称)中进行。
方案二中配制一定量10%的氢氧化钠溶液,其操作步骤是计算、称量、 。
②试评价上述两种实验方案,其中可行的方案是 ,另一种方案不可行的理由是 ,若用方案二,计算得x= (用含m、n的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
铁和铁的化合物用途广泛。请回答下列问题:
(1)写出在潮湿空气中钢铁锈蚀时正极反应的电极反应式:_______________________。
将生锈的铁屑放入H2SO4溶液中充分溶解后,在溶液中并未检测出Fe3+,用离子方程式说明原因:______________________________________。
(2)爱迪生蓄电池的反应式为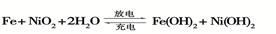
①爱迪生蓄电池的正极是 ,该电池工作一段时间后必须充电,充电时生成Fe的反应类型是______。
②高铁酸钠(Na2FeO4)是一种新型净水剂。用如图装置可以制取少量高铁酸钠。写出在用电解法制取高铁酸钠时,阳极的电极反应式___________________________________。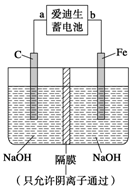
③你认为高铁酸钠作为一种新型净水剂的理由错误的是______。
a.高铁酸钠溶于水形成一种胶体,具有较强的吸附性
b.高铁酸钠在消毒杀菌时被还原生成Fe3+,Fe3+水解产生氢氧化铁胶体能吸附悬浮杂质
c.高铁酸钠具有强氧化性,能消毒杀菌
d.高铁酸钠具有强还原性,能消毒杀菌
(3)某FeO、Fe2O3混合物中,铁、氧的物质的量之比为4︰5,其中Fe2+与Fe3+物质的量之比为___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com