
实验室制备硝基苯的方法是将苯与浓硫酸和浓硝酸的混合液加热到55~60 ℃反应,已知苯与硝基苯的基本物理性质如下表所示:
| 熔点 | 沸点 | 状态 | |
| 苯 | 5.51 ℃ | 80.1 ℃ | 液体 |
| 硝基苯 | 5.7 ℃ | 210.9 ℃ | 液体 |
(1)要配制浓硫酸和浓硝酸的混合酸的注意事项是___________________ ________________________________________________。
(2)分离硝基苯和水的混合物的方法是 ;分离硝基苯和苯的方法是__________________________________________________。
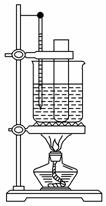
(3)某同学用如图装置制取硝基苯:
①用水浴加热的优点是__________________________________________;
②指出该装置的两处缺陷____________________________________________________;
___________________________________________________。
 解析 (1)试剂的混合顺序是:把浓硫酸缓缓注入到浓硝酸中并及时搅拌冷却,最后逐滴加入苯,边加边振荡,使混酸与苯混合均匀。
解析 (1)试剂的混合顺序是:把浓硫酸缓缓注入到浓硝酸中并及时搅拌冷却,最后逐滴加入苯,边加边振荡,使混酸与苯混合均匀。
(2)硝基苯和水互不相溶,可用分液的方法分离。硝基苯和苯互溶,沸点相差较大,可考虑用蒸馏的方法分离。
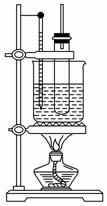
(3)①水浴加热可以使反应物受热均匀,并且温度容易控制。②两处缺陷分别是:盛放反应物的试管不能接触烧杯底部;为了防止苯、硝酸的挥发应在试管口加一个长的直玻璃管,起到冷凝回流作用,如图。
答案 (1)将浓H2SO4沿烧杯内壁缓缓注入浓HNO3中,并用玻璃棒不断搅拌 (2)分液 蒸馏 (3)①使反应体系受热均匀,容易控制温度 ②试管底部不能与烧杯底部接触 试管口缺少一个带有长直玻璃导管的橡皮塞


 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:
在t℃时,某NaOH稀溶液中,c(H+)=10-amol/L,c(OH-)=10-bmol/L,已知a+b=12,则:
⑴该温度下,水的离子积常数Kw= 。
⑵在该温度下,将100mL0.1mol/L的稀硫酸与100mL0.4mol/L的NaOH溶液混合后,溶液的pH= ,此时该溶液中由水电离的c(OH-)= 。
⑶该温度下,若100体积pH1=a的某强酸溶液与1体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是 。
⑷该温度下,pH=3的硫酸溶液和pH=9的NaOH溶液等体积混合后,混合溶液的pH (填>7、=7、<7);pH=3的醋酸溶液和pH=9的NaOH溶液等体积混合后,混合溶液的pH (填>7、=7、<7)。
查看答案和解析>>
科目:高中化学 来源: 题型:
根据原子结构及元素周期律的知识,下列推断正确的是 ( )
A.同主族元素含氧酸的酸性随核电荷数的增加而减弱
B.核外电子排布相同的微粒化学性质也相同
C.Cl‾、S2‾、Ca2+、K+半径逐渐减小
D.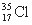 与
与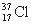 得电子能力相同
得电子能力相同
查看答案和解析>>
科目:高中化学 来源: 题型:
某些化学反应可用下式表示: A + B → C+ D + H2O 。 请回答下列问题(反应可以是固体之间的反应,也可以是在水溶液中进行的反应):
(1)若C是一种碱性气体,常用作制冷剂。则C为 (填化学式下同)。实验室制取C气体的化学方程式为 。
(2)若A为非金属固态单质,C、D均为气体且都能使澄清石灰水变浑浊且C能使溴水褪色。则A为 。写出C与溴水反应的化学方程式 。
(3) 若A为紫红色金属,D为红棕色气体。则A为 。D与水反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关聚乙烯的说法正确的是( )
A.聚乙烯是通过加聚反应生成的
B.聚乙烯具有固定的元素组成,因而具有固定的熔、沸点
C.聚乙烯塑料袋因有毒,不可以装食品
D.聚乙烯因性质稳定,故不易造成污染
查看答案和解析>>
科目:高中化学 来源: 题型:
已知25 ℃、101 kPa下,石墨、金刚石燃烧的化学方程式分别为:C(石墨) + O2(g) = CO2(g),1 moL C(石墨) 完全燃烧放热393.51 kJ;C(金刚石) + O2(g) = CO2(g),1 moL C(金刚石) 完全燃烧放热 395.41 kJ。据此推理所得到的下列结论中,正确的是( )
A.金刚石比石墨稳定 B.石墨转化为金刚石是物理变化
C.石墨的能量比金刚石的能量高 D.由石墨制备金刚石一定是吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
有a、b、c、d四种金属。将a与b连接起来,浸入电解质溶液中,a溶解。将a、d分别投入等浓度的盐酸中,d比a反应强烈。将铜浸入b的盐溶液里,无明显变化。如果把铜浸入c的盐溶液里,有金属c析出。据此判断它们的活动性顺序由强到弱的为( )
A.a > c > d > b B.d > a > b > c
C.d > b > a > c D.b > a > d > c
查看答案和解析>>
科目:高中化学 来源: 题型:
根据下列事实:①X+Y2+=X2++Y;②Z+H2O(冷)=Z(OH)2+H2↑;③Z2+氧化性比X2+弱;④由Y、W电极组成的电池,电极反应为W2++2e-=W、Y-2e-=Y2+,可知X、Y、Z、W的还原性由强到弱的顺序为
A. X > Z > Y > W B. Z > W > X > Y
C. Z > Y > X > W D. Z > X > Y > W
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素X、Y、Z原子序数之和为28,X+与Z2-具有相同的核外电子层结构,Y、Z在同一周期。下列推测正确的是( )
A.元素Y的最高化合价为+7
B.三种元素的原子半径rZ>rY>rX
C.Z的单质比Y的单质更易与H2反应
D.化合物X2Z2中阴阳离子个数之比为1∶2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com