
| A. | 所得溶液中存在等式:c(NH4+)+c(Na+)=c(Cl-)+c(OH-) | |
| B. | 所得溶液显碱性,且c(NH4+)<c(NH3•H2O) | |
| C. | 溶液中存在等式:c(NH4+)+c(NH3•H2O)=c(Cl-) | |
| D. | 溶液中c(Na+)=0.1mol•L-1 |
分析 0.1mol•L-1NaOH和0.2mol•L-1NH4Cl溶液等体积混合后,反应生成NH3•H2O,溶液中含有等浓度NaCL、NH4Cl和NH3•H2O,溶液中存在NH3•H2O?NH4++OH-,一水合氨电离大于铵根离子水解溶液呈碱性,
A.溶液中存在电荷守恒;
B.上述分析可知溶液显碱性;
C.溶液中存在物料守恒分析,n(N)=2n(Cl);
D.钠离子物质的量不变,溶液体积增大一倍,浓度减小一半;
解答 解:0.1mol•L-1NaOH和0.2mol•L-1NH4Cl溶液等体积混合后,反应生成NH3•H2O,溶液中含有等浓度NaCL、NH4Cl和NH3•H2O,溶液中存在NH3•H2O?NH4++OH-,一水合氨电离大于铵根离子水解溶液呈碱性,
A.溶液中存在电荷守恒,c(NH4+)+c(Na+)+c(H+)=c(Cl-)+c(OH-),故A错误;
B.0.1mol•L-1NaOH和0.2mol•L-1NH4Cl溶液等体积混合后得到含有等浓度NaCL、NH4Cl和NH3•H2O的混合溶液,一水合氨电离大于铵根离子水解溶液溶液显碱性,c(NH4+)>c(NH3•H2O),故B错误;
C.溶液中存在物料守恒分析,n(N)=n(Cl),c(NH4+)+c(NH3•H2O)=c(Cl-),故C正确;
D.钠离子物质的量不变,溶液体积增大一倍,浓度减小一半,溶液中c(Na+)=0.05mol•L-1,故D错误;
故选C.
点评 本题考查了电解质溶液反应后的酸碱性比较,电荷守恒、物料守恒的分析判断,注意弱电解质电离和离子水解的理解应用,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 甲烷的电子式为: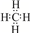 ,分子中各原子都达到“八电子”稳定结构 ,分子中各原子都达到“八电子”稳定结构 | |
| B. | CHCl3只有一种结构,说明甲烷是以碳原子为中心的正四面体结构 | |
| C. | CH4比SiH4分子稳定,说明碳元素比硅元素非金属性强 | |
| D. | CH3Cl的四个价键的长度和强度相同,夹角相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(Ca2+)=c(CO32-) | |
| B. | c(Ca2+)=c(CO32-)=$\sqrt{{K}_{sp}CaC{O}_{3}}$ | |
| C. | c(Ca2+)≠c(CO32-),c(Ca2+)•c(CO32-)=Ksp(CaCO3) | |
| D. | c(Ca2+)≠c(CO32-),c(Ca2+)•c(CO32-)≠Ksp(CaCO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  闻气味 | B. |  倾倒液体 | C. |  取固体药品 | D. |  稀释浓硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.10mol/L | B. | 0.20mol/L | C. | 0.30mol/L | D. | 0.40mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
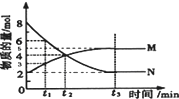 在一定温度下,4L密闭容器内某一反应中气体M、气体N的物质的量随时间变化的曲线如图:
在一定温度下,4L密闭容器内某一反应中气体M、气体N的物质的量随时间变化的曲线如图:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜片为负极,其质量逐渐减少 | B. | 锌片为负极,锌片上产生大量气泡 | ||
| C. | 负极反应式为:Zn-2e-═Zn2+ | D. | 正极反应式为:Cu-2e-═Cu2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com