
实验室测定水体中氯离子的含量时常使用AgNO3溶液滴定法,已知在25 ℃时几种银盐的Ksp:
| 难溶盐 | AgCl | AgBr | AgI | Ag2CrO4 | Ag2CO3 |
| Ksp | 1.8×10-10 | 5.4×10-13 | 8.3×10-17 | 1.9×10-12 | 8.1×10-12 |
| 颜色 | 白色 | 淡黄色 | 黄色 | 砖红色 | 白色 |
可用作滴定Cl-指示剂的是 ( )。
A.K2CrO4 B.Na2CO3
C.NaBr D.NaI
解析 测定水体中的Cl-,选用AgNO3溶液滴定,当Cl-消耗完后,Ag+应与指示剂反应,生成一种有色的沉淀。则选择的该指示剂的阴离子应在Cl-后面沉淀,显然不能选择NaBr和NaI,另Ag2CO3为白色沉淀,无法与AgCl沉淀区别开来。故只能选择K2CrO4。(说明:当Ag+的浓度相同时,Cl-在CrO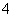 前沉淀。计算如下:设两者达到沉淀溶解平衡时,溶液中c(Ag+)=x mol/L,AgCl(s)Ag+(aq)+Cl-(aq),x2=1.8×10-10,x=1.34×10-5 mol/L。Ag2CrO4(s)2Ag+(aq)+CrO
前沉淀。计算如下:设两者达到沉淀溶解平衡时,溶液中c(Ag+)=x mol/L,AgCl(s)Ag+(aq)+Cl-(aq),x2=1.8×10-10,x=1.34×10-5 mol/L。Ag2CrO4(s)2Ag+(aq)+CrO (aq),(2x)2x=1.9×10-12,x=7.8×10-5 mol/L。由此可知CrO
(aq),(2x)2x=1.9×10-12,x=7.8×10-5 mol/L。由此可知CrO 沉淀时需要的Ag+浓度更大。)
沉淀时需要的Ag+浓度更大。)
答案 A


科目:高中化学 来源: 题型:
将下列仪器组装为一套实验室蒸馏工业酒精的装置,并进行蒸馏。
| (三) | (一) | (五) | (二) | (六) | (四) |
|
|
|
|
|
|
|
(1)A、B、C三种仪器的名称分别是A.________;B.________;C.________。
(2)将以上仪器按(一)→(六)顺序(用字母a,b,c……表示)连接。
e接i;( )接( );k接l;( )接( );( )接( )。
(3)A仪器中,c口是________,d口是________(填“进水口”或“出水口”)。
(4)蒸馏时,温度计水银球应放在________处。
(5)在B中注入工业酒精后,加几片碎瓷片的目的是________。
(6)给B加热,收集到78 ℃左右的馏分是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
25 ℃时,下列有关溶液中微粒的物质的量浓度关系正确的是 ( )。
A.0.1 mol·L-1 CH3COONa溶液与0.1 mol·L-1 HCl溶液等体积混合:c(Na+ )=c(Cl-)>c(CH3COO- )>c(OH- )
B.0.1 mol·L-1 NH4Cl溶液与0.1 mol·L-1氨水等体积混合(pH>7):c(NH3·H2O)>c(NH )>c(Cl-)>c(OH- )
)>c(Cl-)>c(OH- )
C.0.1 mol·L-1 Na2CO3溶液与0.1 mol·L-1 NaHCO3溶液等体积混合: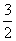 c(Na+)=c(CO
c(Na+)=c(CO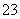 )+c(HCO
)+c(HCO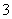 )+c(H2CO3)
)+c(H2CO3)
D.0.1 mol·L-1 Na2C2O4溶液与0.1 mol·L-1 HCl溶液等体积混合(H2C2O4为二元弱酸): 2c(C2O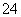 )+c(HC2O
)+c(HC2O )+c(OH-)=c(Na+)+c(H+)
)+c(OH-)=c(Na+)+c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
在pH为4~5的环境中,Cu2+、Fe2+不能生成沉淀,而Fe3+几乎完全沉淀。工业上制取CuCl2是将浓盐酸用蒸汽加热到80 ℃左右,再慢慢加入粗氧化铜(含杂质FeO),充分搅拌使之溶解,欲除去溶液中的杂质离子,下列方法正确的是 ( )。
A.加入纯Cu将Fe2+还原
B.向溶液中加入(NH4)2S使Fe2+沉淀
C.直接加水加热使杂质离子水解除去
D.在溶液中通入Cl2,再加入CuO粉末调节pH为4~5
查看答案和解析>>
科目:高中化学 来源: 题型:
T1、T2两种温度下BaSO4在水中的沉淀溶解平衡曲线如图所示,请回答下列问题:
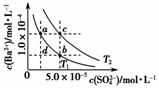
(1)T1________T2(填“>”、“<”或“=”),T2时Ksp(BaSO4)=________。
(2)根据T1温度时BaSO4的沉淀溶解平衡曲线,判断下列说法正确的是________(填序号)。
A.加入Na2SO4可由a点变为b点
B.在T1曲线上方区域(不含曲线)的任意一点时,均有BaSO4沉淀生成
C.蒸发溶剂可能由d点变为T1曲线上a、b之间的某一点(不含a、b)
D.升温可由b点变为d点
(3)沉淀的生成、溶解和转化在无机物制备和提纯及科研等领域有着广泛应用。已知25 ℃时,Ksp(BaSO4)=1×10-10,Ksp(BaCO3)=1×10-9。
①医学上进行消化系统的X射线透视时,常使用BaSO4作内服造影剂。胃酸酸性很强(pH约为1),但服用大量BaSO4仍然是安全的,BaSO4不溶于酸的原因是___________________________________________________________
__________________________________________________________________
(用沉淀溶解平衡原理解释)。万一误服了少量BaCl2,应尽快用大量0.5 mol
·L-1 Na2SO4溶液洗胃,如果忽略洗胃过程中Na2SO4溶液浓度的变化,残留在胃液中的Ba2+浓度仅为________ mol·L-1。
②长期使用的锅炉需要定期除水垢,否则会降低燃料的利用率。水垢中含有CaSO4,可先用Na2CO3溶液处理,使之转化为疏松、易溶于酸的CaCO3,而后用酸除去。CaSO4转化为CaCO3的离子方程式为_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
合成氨工业中,原料气(N2、H2、混有少量CO、NH3)在进入合成塔之前,常用醋酸二氨合铜(Ⅰ)溶液来吸收CO,其反应为CH3COO[Cu(NH3)2]+CO+NH3
CH3COO[Cu(NH3)3]·CO(正反应为放热反应)。
(1)必须除去CO的原因是_______________________________________。
(2)醋酸二氨合铜(Ⅰ)溶液吸收原料气中CO的适宜条件是
____________________________________________________。
(3)吸收CO后的醋酸铜(Ⅰ)氨溶液经适当处理又可再生,恢复其吸收CO的能力而循环使用,其再生的条件是______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
若按图甲装置进行实验,图乙中x、y分别表示流入电极的电子、某产物的物质的量。若将甲装置中的溶液改为等体积、等物质的量浓度的CuSO4和NaCl溶液的混合液,电解过程中溶液的pH随时间t变化的示意图如丙所示。则下列叙述中正确的是( )
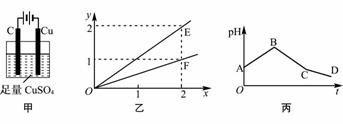
A. E表示反应生成Cu的物质的量 B. F表示反应生成H2SO4的物质的量
C. BC段阳极产物是Cl2 D. CD段电解的物质是水
查看答案和解析>>
科目:高中化学 来源: 题型:
室温时,盐酸和硫酸的混合溶液20mL,向混合物中逐滴加入0.05mol·L-1Ba(OH)2溶液时,生成的BaSO4和pH的变化如图所示(不考虑溶液混合时体积的变化)。下列说法正确的是
A.图中A点对应溶液的pH:a=1
B.生成沉淀的最大质量m=2.33g
C.原混合液中c(HCl)=0.2mol·L-1
D.当V[Ba(OH)2(aq)]=30mL时,有关离子浓度大小:
c(Cl-)>c(Ba2+)>c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com