
过滤后的粗盐水中仍含有可溶性的CaCl2、MgCl2、Na2SO4 等杂质,通过以下实验步骤,可制得纯净的食盐水:① 加入稍过量的Na2CO3溶液;② 加入稍过量的NaOH溶液;③ 加入稍过量的BaCl2 溶液;④滴入稀盐酸至无气泡产生;⑤ 过滤。正确的操作顺序是
A.③⑤②①④ B.③②①⑤④ C.②③①④⑤ D.①②③⑤④
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案科目:高中化学 来源: 题型:
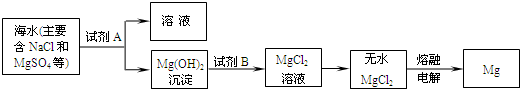
查看答案和解析>>
科目:高中化学 来源: 题型:
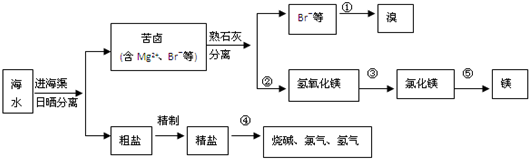
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源:2012-2013学年甘肃省兰州一中高二上学期期中考试化学试卷(带解析) 题型:单选题
过滤后的粗盐水中仍含有可溶性的CaCl2、MgCl2、Na2SO4等杂质,通过以下实验步骤,可制得纯净的食盐水:①加入稍过量的Na2CO3溶液;②加入稍过量的NaOH溶液;③加入稍过量的BaCl2 溶液;④滴入稀盐酸至无气泡产生;⑤过滤。正确的操作顺序是
| A.③⑤②①④ | B.③②①⑤④ | C.②③①④⑤ | D.①②③⑤④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com