
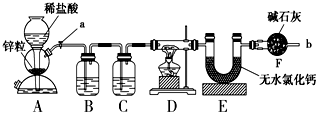
分析 装置A是制备氢气的发生装置,通过装置B中的水除去氢气中的氯化氢,通过装置C中的浓硫酸干燥氢气,通过装置D还原FeO和Fe2O3的混合物,生成的水蒸气进入装置E吸收,称量质量变化得到生成水的质量计算氧化铁的质量,装置F是防止空气中的水蒸气进入装置E影响测定结果的准确性,
(1)依据装置中气体压强变化和液面变化分析判断装置气密性;
(2)Zn先与CuSO4反应生成Cu附着在Zn表面,Zn(负极)、Cu(正极)与稀盐酸(电解质溶液)组成很多微小原电池;
(3)氢气是可燃性气体加热或点燃前需要进行验纯;
(4)A中产生的H2中混有HCl和水蒸气,必须通过洗气逐一除去,防止干扰后续实验;
(5)D装置发生的反应是氢气还原氧化亚铁、氧化铁的反应,生成了铁和水;
(6)根据氧化铁、氧化亚铁的总质量及U型管的质量增加7.2g为水的质量列式计算;
(7)若无干燥管F,空气中的水蒸气被E吸收则所测生成水的质量增大,氧元素物质的量偏大,Fe2O3的质量也将偏大;
(8)若反应后得到的残留固体中还有少量FeO,E吸收则所测生成水的质量减小,氧元素物质的量偏小.
解答 解:(1)检查装置A的气密性,需要关闭开关a,在球形漏斗中加入水到下端液面高于容器中的液面,一段时间后液面不变证明气密性完好;
故答案为:关闭a,从球形漏斗口加水,待水从漏斗管上升与容器中的水面形成一段水柱,停止加水,静置片刻,如水柱不下降,证明其气密性良好;
(2)装置A发生的反应有时要向其中加入少量CuSO4溶液,锌和硫酸铜溶液反应生成铜附着在锌表面,在稀硫酸中形成原电池反应加快反应速率,
故答案为:加快氢气产的速率;Zn先与CuSO4反应生成Cu附着在Zn表面,Zn(负极)、Cu(正极)与稀盐酸(电解质溶液)组成很多微小原电池,发生原电池反应,加快了反应速率;
(3)氢气是可燃性气体,装置中需要充满氢气后方可进行加热反应,所以需要对氢气进行验纯,避免混有空气加热发生爆炸,在F处收集氢气验纯;
故答案为:收集氢气验纯;
(4)由于A中产生的H2中混有HCl和水蒸气,必须通过洗气逐一除去,防止干扰后续实验,所以B的作用是除去氢气中的氯化氢,C的浓硫酸,用于干燥氢气,
故答案为:除去氢气中的氯化氢;浓硫酸;干燥氢气;
(5)装置D中发生的是氧化亚铁、氧化铁与氢气的反应,反应方程式为:3H2+Fe2O32Fe+3H2O,H2+FeO$\frac{\underline{\;高温\;}}{\;}$Fe+H2O,
故答案为:3H2+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3H2O,H2+FeO$\frac{\underline{\;高温\;}}{\;}$Fe+H2O;
(6)U型管的质量增加的7.2g是水,物质的量是 $\frac{7.2g}{18g/mol}$=0.4mol,
设FeO、Fe2O3物质的量分别为X、Y,则:X+3Y=0.4
根据质量可列式:72X+160Y=23.2
解得Y=0.1,X=0.1,
所以氧化铁的质量为:160g/mol×0.1mol=16g,
故答案为:16;
(7)干燥管F的作用防空气中水蒸气对实验干扰,若无干燥管F,空气中的水蒸气被E吸收则所测生成水的质量增大,导致氧的含量增大,Fe2O3的质量将偏大,
故答案为:防止空气中的水蒸气等气体进入E中;偏大.
(8)若反应后得到的残留固体中还有少量FeO,E吸收则所测生成水的质量减小,氧元素物质的量偏小,依据(6)中金属可知设此时生成水质量为m,
72X+160Y=23.2
X+3Y=$\frac{m}{18}$
Y=$\frac{56m}{18}$-23.2,m越小,Y越小,
测得的Fe2O3质量将偏小,
故答案为:偏小.
点评 本题考查了测定FeO和Fe2O3固体混合物中Fe2O3的质量,是一道综合实验题,解题的关键是掌握各种装置的作用,并能根据相关的数据进行计算,此题对训练学生思维能力有一定帮助,本题难度中等.


 一线名师权威作业本系列答案
一线名师权威作业本系列答案科目:高中化学 来源: 题型:选择题
| A. | 加热条件下,1 mol Cl2与足量铁粉充分反应,转移的电子数为3NA | |
| B. | 1 L 1 mol/L的Na2CO3溶液中所含Na+ 离子数为NA | |
| C. | 标准状况下,11.2 L H2O中含有的电子数为5NA | |
| D. | 1 mol CO2和O2的混合气体中所含氧原子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
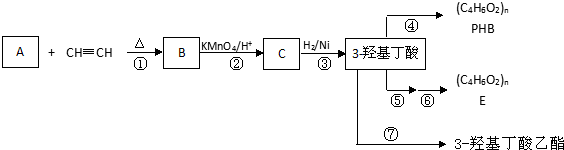
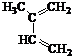 +
+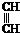 $\stackrel{△}{→}$
$\stackrel{△}{→}$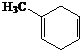
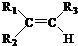 $\stackrel{KMnO_{4}/H+}{→}$
$\stackrel{KMnO_{4}/H+}{→}$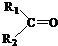 +
+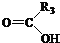
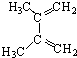 ;理论上B也可以由1,3-丁二烯与烃F来合成,则F的名称(系统命名法):2-丁炔;C中含有的官能团的名称是羰基和羧基.
;理论上B也可以由1,3-丁二烯与烃F来合成,则F的名称(系统命名法):2-丁炔;C中含有的官能团的名称是羰基和羧基.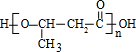 ;它与E不互为(填“互为”或“不互为”)同分异构体.
;它与E不互为(填“互为”或“不互为”)同分异构体.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单质的沸点:Z>X | |
| B. | 原子序数:Z>X>W | |
| C. | 原子的最外层电子数:Y>W>Z | |
| D. | 标准状况下,5.6LW的单质中含有0.5mol原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
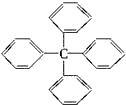
| A. | 此物质分子式为C25H18,属于苯的同系物 | |
| B. | 其一氯代物共有四种 | |
| C. | 此分子最多有13个碳原子在一个平面上 | |
| D. | 该物质能使溴水因化学反应而褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
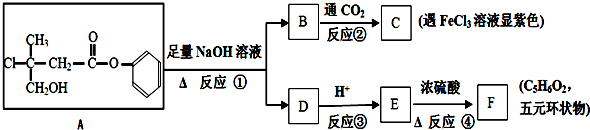
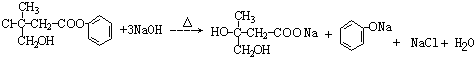 .
.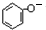 +CO2+H2O→
+CO2+H2O→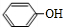 +HCO3-.
+HCO3-. .
.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
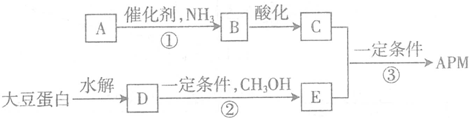
 ,C中所含官能团的名称为羧基、氨基.
,C中所含官能团的名称为羧基、氨基. .
.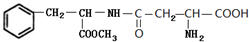 和
和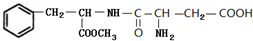 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在NH4+和[Cu(NH3)4]2+中都存在配位键 | |
| B. | 12g金刚石中含有的C-C键的个数为2NA | |
| C. | 配位数为4的配合物均为正四面体结构 | |
| D. | 向含有0.1mol[Co(NH3)4Cl2]Cl的水溶液中加入足量AgNO3溶液只能生成0.1molAgCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使酚酞变红色的溶液:Na+、Cu2+、Fe2+、NO3- | |
| B. | 使PH试纸变红的溶液中:Na+、Mg2+、SO42-、NH4+ | |
| C. | c(H+)=0.1mol•L-1的溶液:Na+、NH4+、SO42-、F- | |
| D. | 与铁粉反应放出H2的无色溶液:Na+、Cl-、HCO3-、SO42- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com