
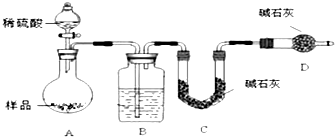
���� [����һ]̼�����Ʋ��ȶ��������ֽ⣬���ݼ���ǰ����������仯�����ݲ�������̼�����Ƶ��������������̼���Ƶ�����������
��1��̼���������ȷֽ�����̼���ơ�ˮ�Ͷ�����̼��
��2�����Ⱥ��ر�֤̼��������ȫ�ֽ⣻
[������]̼���ƺ�̼�����ƶ�������������Ӧ����̼�ᱵ�������������ɳ���������������̼���Ƶ�����������
��1�����ݹ��˲�����������������
��2����ȡ�ϲ���Һ�������ӳ����������Ƿ����ɳ�����
[������]��3���ɲⶨ������ʵ���֪��A�з���Na2CO3+H2SO4=H2O+CO2��+Na2SO4��2NaHCO3+H2SO4=Na2SO4+2H2O+2CO2����B��ΪŨ��������ˮ�����������̼������Cװ�����ն�����̼��Dװ�÷�ֹ�����еĶ�����̼��ˮ����Cװ�ø��ź����ⶨ��
��4����Ϸ�Ӧ������ϵ��Ԫ���غ����õ����ʵ����������������ʺ�����
��5��������̼���岻��ȫ������Cװ�ñ����գ���Ҫ����һ��װ�ö�����̼�������װ��C��װ�ã�
��� �⣺[����һ]��1��̼���������ȷֽ�����̼���ơ�ˮ�Ͷ�����̼����Ӧ����ʽΪ��2NaHCO3$\frac{\underline{\;\;��\;\;}}{\;}$Na2CO3+H2O+CO2����
�ʴ�Ϊ��2NaHCO3$\frac{\underline{\;\;��\;\;}}{\;}$Na2CO3+H2O+CO2����
��2��ʵ��ԭ���Ǹ��ݼ���ǰ����������仯������̼�����ƣ���Ӧ��֤̼��������ȫ�ֽ⣬���Ⱥ�����̼��������ȫ�ֽ⣬
�ʴ�Ϊ����֤NaHCO3�ֽ���ȫ��
[������]��1������ʱ���ò������������ʴ�Ϊ����������
��2����ȡ�ϲ���Һ�������ӳ����������Ƿ����ɳ������������Ϊ��ȡ�ϲ���Һ�������Թ��У���������������Һ�����������ɣ��������ȫ��
�ʴ�Ϊ��ȡ�����ϲ���Һ��һ֧�Թ��У��μ�Ba��OH��2��Һ���۲��Ƿ��а�ɫ�������ɣ�
[������]��3��B��ΪŨ��������ˮ�����������̼�������е�ˮ�����Ͷ�����̼�ᱻ��ʯ�����գ���D�����������տ����е�ˮ�����Ͷ�����̼����ȷ��Cװ����������������ȷ�ԣ���Һ©�������������������ᣬ�����ӷ��������Ƶö�����̼�����к��Ȼ��⣬Ũ����������Ȼ��⣬���Ȼ��ⱻ��ʯ�����գ����²������̼����ƫ�ߣ�������̼���ƺ�̼�����ƣ�̼�����Ʋ���������̼�࣬��ᵼ��̼������ƫ�̼࣬����ƫС��
�ʴ�Ϊ��Ũ�����ֹ�����е�ˮ������������̼����Cװ�ã����ܣ�
��4����NaHCO3��Na2CO3�����ʵ����ֱ�Ϊx��y����
Na2CO3+H2SO4=H2O+CO2��+Na2SO4��
x x
2NaHCO3+H2SO4=Na2SO4+2H2O+2CO2��
y y
$\left\{\begin{array}{l}{106x+84y=17.90\\;}\\{44x+44y=8.80}\end{array}\right.$
���x=0.05mol
y=0.15mol
����Ʒ��Na2CO3����������Ϊ$\frac{0.05mol��106g/mol}{17.90g}$��100%=29.6%��
�ʴ�Ϊ��29.6%��
��5��ʵ��װ�û�����һ������ȱ��Ϊװ���еĶ�����̼���ܱ�Cȫ�����գ��������һ��װ�ý�A��B�е�CO2ȫ������C�����գ�
�ʴ�Ϊ��ȱ��һ�����ϲ���������̼�����װ�ã�
���� ���⿼��̼���ƺ����IJⶨʵ�飬Ϊ��Ƶ���㣬����ʵ��װ�õ����ü�ʵ��Ŀ��Ϊ���Ĺؼ������ط��������㼰ʵ���������ۺϿ��飬��Ŀ�Ѷ��еȣ�


 ���ɿ��õ�Ԫ����AB��ϵ�д�
���ɿ��õ�Ԫ����AB��ϵ�д� С�����ϵ�д�
С�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
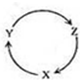 �±����������У���������ͼ����һ��ת����ϵ��ѡ���ǣ�������
�±����������У���������ͼ����һ��ת����ϵ��ѡ���ǣ������� | X | Y | Z | |
| A | N2 | NO2 | NH4NO3 |
| B | Al | Al2O3 | NaAlO2 |
| C | Cu | CuO | CuCl2 |
| D | Si | SiO2 | H2SiO3 |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | c��H+����� | B�� | c��OH-����� | C�� | c��Cl-��=c��CH3COO-�� | D�� | c��Cl-����c��CH3COO-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢� | B�� | �٢ڢ� | C�� | �٢ۢ� | D�� | �٢ڢۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | SO2����Ư���� | B�� | SO2Ϊ���������� | C�� | SO2���л�ԭ�� | D�� | SO2���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����һ�ַ�Ӧ�� | B�� | �����¶� | ||
| C�� | ��ƽ����ϵ����ѹǿ | D�� | ʹ�ô��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com