
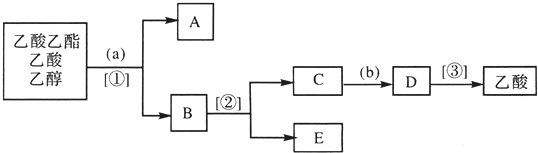
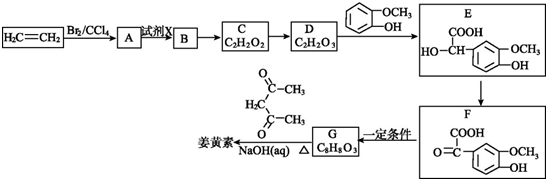
·ÖĪö ÓÉ·ÖĄėŅŅĖįŅŅõ„”¢ŅŅĖį”¢ŅŅ“¼µÄ»ģŗĻĪļµÄĮ÷³ĢĶ¼æÉÖŖ£¬aĪŖ±„ŗĶĢ¼ĖįÄĘČÜŅŗ£¬¢ŁĪŖ·ÖŅŗ£¬ŌņµĆµ½AĪŖŅŅĖįŅŅõ„£¬BĪŖŅŅ“¼ŗĶŅŅĖįÄĘ£¬¢ŚĪŖÕōĮó£¬ŌņEĪŖŅŅ“¼£¬CĪŖŅŅĖįÄĘ£¬bĪŖŃĪĖį£¬·¢ÉśĒæĖįÖĘČ”ČõĖįµÄ·“Ó¦£¬DĪŖ“×ĖįŗĶĀČ»ÆÄĘ£¬Č»ŗóÕōĮóµĆµ½ŅŅĖį£¬¼“¢ŪĪŖÕōĮó£¬ŅŌ“ĖĄ“½ā“š£®
½ā“š ½ā£ŗŅŅĖį³ŹĖįŠŌÄÜÓė¼īČÜŅŗ»ņĢ¼ĖįŃĪČÜŅŗ·“Ó¦£¬Éś³ÉŅ×ČÜÓŚĖ®µÄŅŅĖįŃĪ£¬¾¢Ł·ÖŅŗµÄµ½AŅŅĖįŅŅõ„ÓėBŅŅ“¼ŗĶŅŅĖįÄĘŗĶ¹żĮæµÄĢ¼ĖįÄĘČÜŅŗ£»ŌŁ¾¢ŚÕōĮó³żČ„ŅŅ“¼£¬µĆµ½CŅŅĖįÄĘŗĶĢ¼ĖįÄĘČÜŅŗ£¬¼ÓČėbĻ”ĮņĖįĖį»Æ£¬ŌŁ¾¢ŪÕōĮóµĆµ½ŅŅĖį£®
£Ø1£©ÓÉÉĻŹö·ÖĪöæÉÖŖ£¬aĪŖ±„ŗĶµÄNa2CO3ČÜŅŗ£¬bĪŖĻ”H2SO4£¬¹Ź“š°øĪŖ£ŗ±„ŗĶµÄNa2CO3ČÜŅŗ£»Ļ”H2SO4£»””
£Ø2£©ÓÉÉĻŹö·ÖĪöæÉÖŖ£¬¢Ł¢Ś¢Ū²Ł×÷·Ö±šĪŖ·ÖŅŗ”¢ÕōĮó”¢ÕōĮ󣬹Ź“š°øĪŖ£ŗ·ÖŅŗ£»ÕōĮó£»ÕōĮó£»
£Ø3£©A”¢B”¢C”¢D”¢E·Ö±šĪŖŅŅĖįŅŅõ„£¬ŅŅ“¼”¢ŅŅĖįÄĘ¼°¹żĮæµÄĢ¼ĖįÄĘČÜŅŗ£¬ŅŅĖįÄĘČÜŅŗŗĶNa2CO3ČÜŅŗ£¬ŅŅĖįŗĶĮņĖįÄĘČÜŅŗ£Ø¼°H2SO4£©£¬ŅŅ“¼£¬
¹Ź“š°øĪŖ£ŗŅŅĖįŅŅõ„£»ŅŅ“¼”¢ŅŅĖįÄĘ¼°¹żĮæµÄĢ¼ĖįÄĘČÜŅŗ£»ŅŅĖįÄĘČÜŅŗŗĶNa2CO3ČÜŅŗ£»ŅŅĖįŗĶĮņĖįÄĘČÜŅŗ£Ø¼°H2SO4£©£»ŅŅ“¼£®
µćĘĄ ±¾Ģāæ¼²éĪļÖŹµÄ·ÖĄė”¢Ģį“æµČ»ł±¾·½·ØŃ”ŌńÓėÓ¦ÓĆ£¬ĪŖøßĘµæ¼µć£¬ĢāÄæÄŃ¶Č²»“ó£¬×¢ŅāĪļÖŹµÄŠŌÖŹµÄŅģĶ¬¼°Į÷³ĢÖŠµÄ»ģŗĻĪļ·ÖĄė·½·ØĪŖ½ā“šøĆĄąĢāÄæµÄ¹Ų¼ü£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1 mol NaCl ·Ö×Ó | |
| B£® | ÖŹ×ÓŹżĪŖ 35”¢ÖŠ×ÓŹżĪŖ 45 µÄäåŌ×Ó£ŗ${\;}_{35}^{45}$ Br | |
| C£® | ĮņĄė×ӵĽį¹¹Ź¾ŅāĶ¼£ŗ | |
| D£® | NH4+ µÄµē×ÓŹ½£ŗ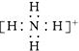 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
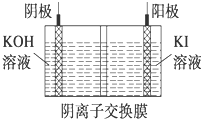 µā±»³ĘĪŖ”°ÖĒĮ¦ŌŖĖŲ”±£¬æĘѧŗĻĄķµŲ²¹³äµāæÉ·ĄÖĪµāȱ·¦²”£¬KI”¢KIO3ŌųĻČŗóÓĆÓŚ¼ÓµāŃĪÖŠ£®
µā±»³ĘĪŖ”°ÖĒĮ¦ŌŖĖŲ”±£¬æĘѧŗĻĄķµŲ²¹³äµāæÉ·ĄÖĪµāȱ·¦²”£¬KI”¢KIO3ŌųĻČŗóÓĆÓŚ¼ÓµāŃĪÖŠ£®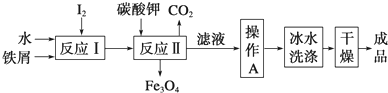
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ¼ŗ¶žĖį
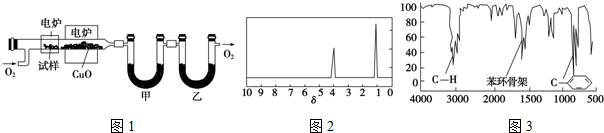
¼ŗ¶žĖį ŹĒŅ»ÖÖ¹¤ŅµÉĻ¾ßÓŠÖŲŅŖŅāŅåµÄÓŠ»ś¶žŌŖĖį£¬ŌŚ»Æ¹¤Éś²ś”¢ÓŠ»śŗĻ³É¹¤Ņµ”¢Ņ½Ņ©”¢Č󻬼ĮÖĘŌģµČ·½Ćę¶¼ÓŠÖŲŅŖ×÷ÓĆ£¬Äܹ»·¢Éś³ÉŃĪ·“Ó¦”¢õ„»Æ·“Ó¦µČ£¬²¢ÄÜÓė¶žŌŖ“¼Ėõ¾Ū³Éøß·Ö×Ó¾ŪŗĻĪļµČ£¬¼ŗ¶žĖį²śĮæ¾ÓĖłÓŠ¶žŌŖōČĖįÖŠµÄµŚ¶žĪ»£®ŹµŃéŹŅŗĻ³É¼ŗ¶žĖįµÄ·“Ó¦ŌĄķŗĶŹµŃé×°ÖĆŹ¾ŅāĶ¼ČēĻĀ£ŗ
ŹĒŅ»ÖÖ¹¤ŅµÉĻ¾ßÓŠÖŲŅŖŅāŅåµÄÓŠ»ś¶žŌŖĖį£¬ŌŚ»Æ¹¤Éś²ś”¢ÓŠ»śŗĻ³É¹¤Ņµ”¢Ņ½Ņ©”¢Č󻬼ĮÖĘŌģµČ·½Ćę¶¼ÓŠÖŲŅŖ×÷ÓĆ£¬Äܹ»·¢Éś³ÉŃĪ·“Ó¦”¢õ„»Æ·“Ó¦µČ£¬²¢ÄÜÓė¶žŌŖ“¼Ėõ¾Ū³Éøß·Ö×Ó¾ŪŗĻĪļµČ£¬¼ŗ¶žĖį²śĮæ¾ÓĖłÓŠ¶žŌŖōČĖįÖŠµÄµŚ¶žĪ»£®ŹµŃéŹŅŗĻ³É¼ŗ¶žĖįµÄ·“Ó¦ŌĄķŗĶŹµŃé×°ÖĆŹ¾ŅāĶ¼ČēĻĀ£ŗ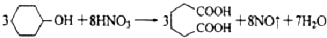
| ĪļÖŹ | ĆÜ¶Č£Ø20”ę£© | ČŪµć | ·Šµć | ČܽāŠŌ | Ļą¶Ō·Ö×ÓÖŹĮæ |
| »·¼ŗ“¼ | 0.962g/cm3 | 25.9”ę | 160.8”ę | 20”ꏱĖ®ÖŠČܽā¶Č3.6g£¬æÉ»ģČÜÓŚŅŅ“¼”¢±½ | 100 |
| ŅŅ¶žĖį | 1.36g/cm3 | 152”ę | 337.5”ę | ŌŚĖ®ÖŠµÄČܽā¶Č£ŗ15”ꏱ£¬1.44g£¬25”ꏱ2.3g£¬Ņ×ČÜÓŚŅŅ“¼£¬²»ČÜÓŚ±½ | 146 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
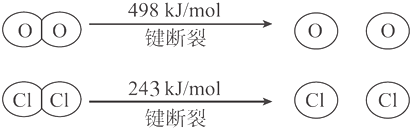
| A£® | 12kJ | B£® | 32kJ | C£® | 115.6kJ | D£® | 127.6kJ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

| ŹµŃé²½Öč | Ō¤ĘŚĻÖĻóŗĶ½įĀŪ |
| ²½Öč1£ŗȔɣĮæŠü×ĒŅŗ£¬¹żĀĖ£¬³ä·ÖĻ“µÓŗó£¬Č”ĀĖŌüÓŚŹŌ¹ÜÖŠ£¬£ŗ¼ÓČė¹żĮæ2mol/LµÄŃĪĖįČÜŅŗ£¬³ä·ÖÕńµ“£¬ŌŁµĪ¼Ó¼øµĪ0.1mol/LĀČ»Æ±µČÜŅŗ | ÓŠ°×É«³ĮµķÉś³ÉĖµĆ÷Šü×ĒŅŗÖŠ»ģÓŠCu4£ØOH£©6SO4£® |
| ²½Öč2£ŗĮķȔɣĮæŠü×ĒŅŗÓŚŹŌ¹ÜÖŠ£¬½«ŹŌ¹Ü·ÅČė×°ÓŠ·ŠĖ®µÄŠ”ÉÕ±ÖŠĖ®Ō”¼ÓČČŅ»¶ĪŹ±¼äČ”³öŹŌ¹Ü¹Ū²ģ | ŹŌ¹ÜÖŠÓŠŗŚÉ«¹ĢĢåÉś³É£¬ĖµĆ÷Šü×ĒŅŗÖŠ»ģÓŠCu£ØOH£©2£® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
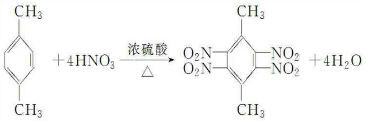 £®
£®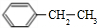 ”¢
”¢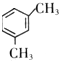 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
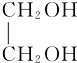 +O2$”ś_{”÷}^{Cu}$OHC-CHO+2H2O£®
+O2$”ś_{”÷}^{Cu}$OHC-CHO+2H2O£®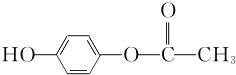 £®
£® £®
£®²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com