
| A、FeO |
| B、Fe2O3 |
| C、Fe3O4 |
| D、FeCO3 |


 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源: 题型:
| A、定容摇匀后,有少量溶液外流,则NaClO的物质的量浓度偏小 |
| B、容量瓶用蒸馏水洗净后必须烘干才能用于溶液的配制 |
| C、所配得的NaClO消毒液在空气中光照,久置后溶液中NaClO的物质的量浓度减小 |
| D、需要称量的NaClO固体的质量为142.8 g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、32克O2和O3 的混合气体中含有的氧原子个数为2NA | ||
| B、Na2O2与水反应,当有2 mol的Na2O2作氧化剂,转移的电子数目为2NA | ||
C、CO2通过Na2O2,使其增重b克,反应中转移的电子数为
| ||
| D、标况下.22.4LHCL 溶于水后溶液中含NA个HCl分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、AlCl3溶液中加入足量的氨水:Al3++3OH-=Al(OH)3↓ |
| B、铝粉投入到NaOH溶液中:2Al+2OH-=2AlO 2-+H2↑ |
| C、钠和冷水反应:2Na+2H2O=2Na++2OH-+H2↑ |
| D、氢氧化钡溶液与硫酸反应:SO42-+Ba2+=BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向碳酸氢钙溶液中加入过量氢氧化钠:Ca2++2HCO3-+2OH-═CaCO3↓+2H2O+CO32- |
| B、氧化铁可溶于氢碘酸:Fe2O3+6H+═2Fe3++3H2O |
| C、AlCl3溶液中加入过量的浓氨水:Al3-+4NH3?H2O═AlO2-+4NH4-+2H2O |
| D、Na2S溶液呈碱性:S2-+H2O═HS-+OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、7.8 g Na2O2含有的阴离子数目为0.2NA |
| B、标准状况下,2.24 L H2O含有的分子数等于0.1NA |
| C、0.1 mol钠和O2在一定条件下反应完全生成Na2O和Na2O2混合物时,失去电子数为0.1NA |
| D、1 L 0.5 mol?L-1 Na2CO3溶液中含有的CO32-数目为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
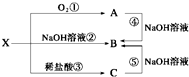 (1)写出下列物质的化学式:A:
(1)写出下列物质的化学式:A:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com