
【题目】钒被称为“工业味精”“工业维生素”,在发展现代工业、国防等方面发挥着至关重要的作用。某高铬型钒渣含Fe2O3、Fe3O4、SiO2、Al2O3、V2O5、Cr2O3等物质,从中分离提取钒铬的工艺流程如下:
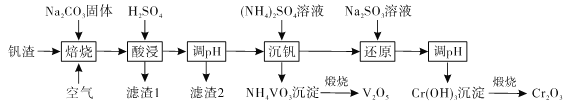
回答下列问题:
(1)“焙烧”时会生成NaVO3和Na2CrO4,生成Na2CrO4的化学方程式是_________。
(2)滤渣1中主要含_______。滤渣2的主要成分是Fe(OH)3和Al(OH)3,对应调pH应不低于_____。(常温下,当溶液中离子浓度小于1×10-6mol/L时认为沉淀完全, Ksp[Fe(OH)3]=4.0×10-38、Ksp[Al(OH)3]=1.0×10-33)
(3)“沉钒”所用0.1mol/L (NH4)2SO4溶液中,离子浓度由大到小的顺序是_______。
(4)“还原”时溶液的pH在2.5左右,此时控制酸度应选用_______(填标号)。
A.稀盐酸 B.稀硫酸 C.稀硝酸 D.硫酸铵
(5)NH4VO3、Cr(OH)3煅烧时发生反应的类型是否相同?___________。
(6)工业上可用电解还原法处理含Cr2O72- 的酸性废水。用铁板作阳极,电解过程中,废水pH逐渐上升,Cr3+、Fe3+都以氢氧化物沉淀析出,达到废水净化的目的。
①其中阳极的电极反应式是___________。
②电解过程中,废水pH上升的原因是___________________。
【答案】2Cr2O3+3O2+4Na2CO3![]() 4Na2CrO4+4CO2 H2SiO3 5 c(NH4+)>c(SO42-)>c(H+)>c(OH-) B 相同 Fe-2e-= Fe2+ 阳极放电生成的Fe2+与Cr2O72-反应消耗H+,阴极H+放电生成氢气
4Na2CrO4+4CO2 H2SiO3 5 c(NH4+)>c(SO42-)>c(H+)>c(OH-) B 相同 Fe-2e-= Fe2+ 阳极放电生成的Fe2+与Cr2O72-反应消耗H+,阴极H+放电生成氢气
【解析】
钒渣含Fe2O3、Fe3O4、SiO2、Al2O3、V2O5、Cr2O3等物质,通入空气条件下,和碳酸钠固体混合一起培烧,二氧化硅与碳酸钠反应生成了硅酸钠,Fe3O4被氧化成 Fe2O3 “焙烧”时V2O5会生成NaVO3,Cr2O3在通入空气条件下被氧化和碳酸钠固体反应生成Na2CrO4,加入硫酸,硅酸钠变成硅酸沉淀,Fe2O3、Al2O3、NaVO3、Na2CrO4溶于硫酸,溶液中含有Al3+、Fe3+、VO3-、CrO42-,调pH值使Al3+、Fe3+转化成Fe(OH)3和Al(OH)3沉淀,用 (NH4)2SO4溶液“沉钒”,加亚硫酸钠将+6价的铬还原成+3价的Cr3+。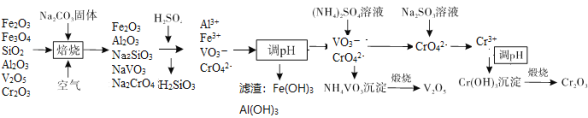
(1)+3价的的铬氧化成+6价,读图确定反应物有Cr2O3、O2、Na2CO3 “焙烧”时Cr2O3生成Na2CrO4的化学方程式是:2Cr2O3+3O2+4Na2CO3 4Na2CrO4+4CO2;
4Na2CrO4+4CO2;
(2)加入硫酸,硅酸钠变成硅酸沉淀,故滤渣1中主要含硅酸;根据题中数据Ksp[Fe(OH)3]=4.0×10-38、Ksp[Al(OH)3]=1.0×10-33,同一类型的物质Ksp越小越难溶,使Al3+、Fe3+转化成Fe(OH)3和Al(OH)3沉淀且沉淀完全, pH计算以Ksp[Al(OH)3]带入计算:Ksp[Al(OH)3]=1.0×10-33=c(Al3+)×c3(OH-),c(Al3+)=1×10-6molL—1,解得c(OH-)=1×10-9molL—1,pH=5,对应调pH应不低于5;
(3)(NH4)2SO4溶液中,NH4+发生水解,溶液显酸性,NH4+发生水解浓度会减小,但发生水解的NH4+毕竟少数,NH4+离子浓度仍大于c(SO42-),(NH4)2SO4溶液中离子由大到小的顺序是c(NH4+)>c(SO42-)>c(H+)>c(OH—);
(4)A. CrO42—氧化性很强,会把盐酸氧化;
B.硫酸是非氧化性酸,比较稳定,B项正确;
C.硝酸具有强氧化性会消耗亚硫酸钠,C项错误;
D.硫酸铵水解溶液呈酸性,但程度小达不到酸度要求,溶液的pH值不能达到2.5,D项错误;
答案选B;
(5)2NH4VO3![]() V2O5 +2NH3 +H2O,2Cr(OH)3
V2O5 +2NH3 +H2O,2Cr(OH)3![]() Cr2O3+3H2O,都是分解反应,反应类型相同;
Cr2O3+3H2O,都是分解反应,反应类型相同;
(6)①Fe板作阳极,为活性电极,Fe失电子发生氧化反应生成亚铁离子,阳极反应为Fe-2e-=Fe2+;
②阳极电解产生的Fe2+具有还原性,Cr2O72-具有强氧化性,能将Cr2O72-还原成Cr3+,由离子反应方程式:Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O可知,处理过程中消耗氢离子,溶液的酸性减弱,溶液pH增大;电解时,阴极H+放电发生还原反应,2H++2e-=H2↑,溶液中的H+减少,促进水的电离,氢氧根离子浓度增大,溶液pH增大。


科目:高中化学 来源: 题型:
【题目】已知钼(Mo)的晶胞如图所示,钼原子半径为a pm,相对原子质量为M,以NA表示阿伏加德罗常数的值。

(1)钼晶体的堆积方式为_______________,晶体中粒子的配位数为________________。
(2)构成钼晶体的粒子是________(填“原子”,“分子”或“离子”),晶胞中所含的该种粒子数为___________。
(3)金属钼的密度为______________g·cm-3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气溶于水达到平衡后,若其他条件不变,只改变某一条件,下列叙述正确的是
A.再通入少量氯气,c(H+)/c(ClO-)减小
B.通入少量SO2,溶液漂白性增强
C.加入少量固体NaOH,一定有c(Na+)=c(Cl-)+c(ClO-)
D.加入少量水,水的电离平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z为短周期内除稀有气体外的4种元素,它们的原子序数依次增大,其中只有Y为金属元素。Y和W的最外层电子数都是1,Y、Z两元素原子的质子数之和为W、X两元素质子数之和的3倍,且X与Z同主族。由此可知:
(1)写出元素符号:W为_________,Z为_________
(2)W2X是由_________键组成的分子,其电子式为_________
(3)写出Y的最高价氧化物对应水化物与Z的最高价氧化物对应水化物反应的离子方程式_________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质既能跟稀硫酸反应,又能跟氢氧化钠溶液反应的是
①KHCO3 ②(NH4)2CO3③Al2O3④Al(OH)3
A.全部B.只有①③④C.只有③④D.只有②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用下图所示装置可以模拟铁的电化学腐蚀。下列说法中,正确的是
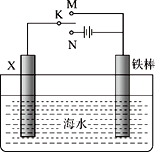
A. 若X为碳棒,开关K置于M处可以减缓铁的腐蚀
B. 若X为铜棒,开关K置于N处可以加快铁的腐蚀
C. 若X为碳棒,开关K置于M处,则为牺牲阳极的阴极保护法
D. 若X为碳棒,开关K置于N处,则为外加电流的阴极保护法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组设计如图装置(部分夹持装置已略去),以探究潮湿的Cl2与Na2CO3反应得到固体物质的成分。
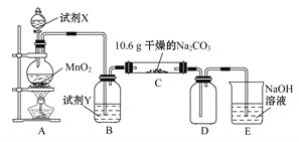
(1)试剂X的化学式________。A中制取Cl2的离子方程式____________________。
(2)试剂Y的名称为______________。
(3)通入一定量潮湿的Cl2反应后,经检测,D中只有Cl2O一种气体,C中除含一种氯盐外,同时含有NaHCO3等,某同学对C中所得固体残渣的成分进行探究。
①提出合理假设。
假设1:存在两种成分:NaHCO3和____________________________;
假设2:存在三种成分:NaHCO3和__________________________。
②设计方案,进行实验。写出实验步骤以及预期现象和结论。
限选实验试剂和仪器:蒸馏水、稀硝酸、BaCl2溶液、澄清石灰水、AgNO3溶液、试管、小烧杯。
实验步骤 | 预期现象和结论 |
步骤1:取C中的少量固体样品于试管中,滴加足量蒸馏水至固体溶解,然后将所得溶液分别置于A、B试管中 | |
步骤2:向A试管中滴加BaCl2溶液 | __________________ |
步骤3:______________ | __________________ |
(4)已知Cl2O与水反应生成次氯酸,则D中Cl2O进入E反应的化学方程式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中学化学常见的有机化合物A(C6H6O)是重要的化工原料,在工业上能合成紫外线吸收剂BAD和治疗心脏病药物的中间体F,合成路线如下:
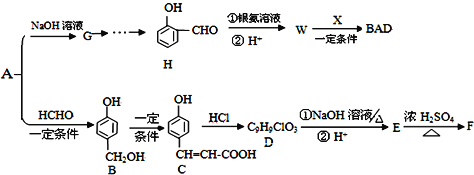
已知:BAD的结构简式为: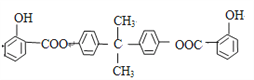
F的结构简式为: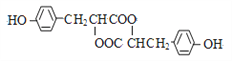
试回答:
(1)H中含有的官能团名称是____________________。
(2)写出X的结构简式____________________________________,推测B的核磁共振氢谱中显示有__________种不同化学环境的氢原子。
(3)写出反应类型A→B______________;W→BAD______________。
(4)1mol C可以和______________mol Br2反应。
(5)C→D的过程中可能有另一种产物C1,请写出在加热条件下C1与足量稀NaOH水溶液反应的化学方程式:__________________________。
(6)B与HCHO在一定条件下反应生成高分子化合物的原理,与酚醛树脂的制备原理相似。请写出该反应的化学方程式___________________。
(7)W的同分异构体有多种,写出所有符合以下要求的W的同分异构体:________________。
①与FeCl3溶液反应,溶液呈紫色; ②能发生银镜反应;③苯环上的一氯代物只有两种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼氢化钠(NaBH4)是有机合成中常用的还原剂。一种制备硼氢化钠工艺如下(部分条件和产物省略):
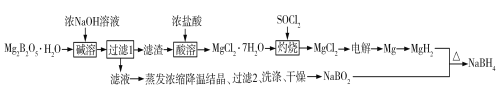
已知:MgH2、NaBH4遇水蒸气剧烈反应并放出H2。
回答下列问题:
(1)Mg2B2O5H2O中B的化合价为_______________。MgH2和NaBO2必须在干燥条件下合成硼氢化钠,其原因是_____________________________________________。
(2)难溶的Mg2B2O5与浓氢氧化钠溶液反应的离子方程式为__________。
(3)SOCl2溶于水能产生两种气体,其中一种气体能使品红溶液褪色,则灼烧时加入SOCl2的目的是______________________________。
(4)已知镁—H2O2酸性燃料电池反应为Mg+H2O2+H2SO4![]() MgSO4+2H2O。常温下,电解质溶液为200 mL 0.1 mol·L1硫酸溶液。
MgSO4+2H2O。常温下,电解质溶液为200 mL 0.1 mol·L1硫酸溶液。
①写出正极的电极反应式:______________________________。
②若电路中有0.038 mol转移电子时,则溶液pH约为_____(忽略体积变化,不考虑H2O2电离)。
(5)“有效氢”是衡量含氢还原剂的还原能力指标,定义为1 g含氢还原剂的还原能力与多少克H2相当。NaBH4的“有效氢”等于_________________(结果保留2位小数)。
(6)工业上,可以利用NaBO2、HCHO和生石灰在加热下生成NaBH4和难溶的盐,写出化学方程式________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com