
ŹŅĪĀĻĀ£¬½«0.05 mol Na2CO3¹ĢĢåČÜÓŚĖ®Åä³É100mLČÜŅŗ£¬ĻņČÜŅŗÖŠ¼ÓČėĻĀĮŠĪļÖŹ”£ÓŠ¹Ų½įĀŪÕżČ·µÄŹĒ
| ¼ÓČėµÄĪļÖŹ | ½įĀŪ | |
| A | 50mL 1 mol”¤L£1H2SO4 | ·“Ó¦½įŹųŗó£¬c(Na+)=c(SO42£) |
| B | 0.05molCaO | ČÜŅŗÖŠ |
| C | 50mL H2O | ÓÉĖ®µēĄė³öµÄc(H+)”¤c(OH”Ŗ)²»±ä |
| D | 0.1molNaHSO4¹ĢĢå | ·“Ó¦ĶźČ«ŗó£¬ČÜŅŗpH¼õŠ”£¬c(Na+)²»±ä |
”¾“š°ø”æB
”¾½āĪö”æ
ŹŌĢā·ÖĪö£ŗŹŅĪĀĻĀ£¬½«0.05 mol Na2CO3¹ĢĢåČÜÓŚĖ®Åä³É100mLČÜŅŗ£¬ČÜŅŗÖŠ“ęŌŚCO32”Ŗ+H2O HCO3”Ŗ+OH”ŖČÜŅŗ³Ź¼īŠŌ£»AĻī¼ÓČė50mL 1 mol”¤L£1H2SO4£¬H2SO4ÓėNa2CO3Ē”ŗĆ·“Ó¦£¬Ōņ·“Ó¦ŗóµÄČÜŅŗČÜÖŹĪŖNa2SO4£¬¹Źøł¾ŻĪļĮĻŹŲŗć·“Ó¦½įŹųŗóc(Na+)=2c(SO42£)£¬¹ŹAĻī“ķĪó£»ĻņČÜŅŗÖŠ¼ÓČė0.05molCaO£¬ŌņCaO+ H2O=Ca(OH)2£¬Ōņc(OH”Ŗ)Ōö“ó£¬ĒŅCa2++CO32”Ŗ=CaCO3”ż£¬Ź¹CO32”Ŗ+H2O
HCO3”Ŗ+OH”ŖČÜŅŗ³Ź¼īŠŌ£»AĻī¼ÓČė50mL 1 mol”¤L£1H2SO4£¬H2SO4ÓėNa2CO3Ē”ŗĆ·“Ó¦£¬Ōņ·“Ó¦ŗóµÄČÜŅŗČÜÖŹĪŖNa2SO4£¬¹Źøł¾ŻĪļĮĻŹŲŗć·“Ó¦½įŹųŗóc(Na+)=2c(SO42£)£¬¹ŹAĻī“ķĪó£»ĻņČÜŅŗÖŠ¼ÓČė0.05molCaO£¬ŌņCaO+ H2O=Ca(OH)2£¬Ōņc(OH”Ŗ)Ōö“ó£¬ĒŅCa2++CO32”Ŗ=CaCO3”ż£¬Ź¹CO32”Ŗ+H2O HCO3”Ŗ+OH”ŖĘ½ŗā×óŅĘ£¬c(HCO3”Ŗ)¼õŠ”£¬¹Ź
HCO3”Ŗ+OH”ŖĘ½ŗā×óŅĘ£¬c(HCO3”Ŗ)¼õŠ”£¬¹Ź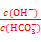 Ōö“󣬹ŹBĻīÕżČ·£»CĻī¼ÓČė50mL H2O£¬ČÜŅŗĢå»ż±ä“ó£¬CO32”Ŗ+H2O
Ōö“󣬹ŹBĻīÕżČ·£»CĻī¼ÓČė50mL H2O£¬ČÜŅŗĢå»ż±ä“ó£¬CO32”Ŗ+H2O HCO3”Ŗ+OH”ŖĘ½ŗāÓŅŅĘ£¬µ«c(OH”Ŗ)¼õŠ”£¬Na2CO3ČÜŅŗÖŠH+”¢OH”Ŗ¾łÓÉĖ®µēĄė£¬¹ŹÓÉĖ®µēĄė³öµÄc(H+)”¤c(OH”Ŗ)¼õŠ”£¬¹ŹCĻī“ķĪó£»DĻī¼ÓČė0.1molNaHSO4¹ĢĢ壬NaHSO4ĪŖĒæĖįĖįŹ½ŃĪµēĄė³öH+ÓėCO32”Ŗ·“Ó¦£¬Ōņ·“Ó¦ŗóČÜŅŗĪŖNa2SO4ČÜŅŗ£¬ČÜŅŗ³ŹÖŠŠŌ£¬¹ŹČÜŅŗpH¼õŠ”£¬ŅżČėĮĖNa+£¬¹Źc(Na+)Ōö“ó£¬DĻī“ķĪó£»±¾ĢāŃ”B”£
HCO3”Ŗ+OH”ŖĘ½ŗāÓŅŅĘ£¬µ«c(OH”Ŗ)¼õŠ”£¬Na2CO3ČÜŅŗÖŠH+”¢OH”Ŗ¾łÓÉĖ®µēĄė£¬¹ŹÓÉĖ®µēĄė³öµÄc(H+)”¤c(OH”Ŗ)¼õŠ”£¬¹ŹCĻī“ķĪó£»DĻī¼ÓČė0.1molNaHSO4¹ĢĢ壬NaHSO4ĪŖĒæĖįĖįŹ½ŃĪµēĄė³öH+ÓėCO32”Ŗ·“Ó¦£¬Ōņ·“Ó¦ŗóČÜŅŗĪŖNa2SO4ČÜŅŗ£¬ČÜŅŗ³ŹÖŠŠŌ£¬¹ŹČÜŅŗpH¼õŠ”£¬ŅżČėĮĖNa+£¬¹Źc(Na+)Ōö“ó£¬DĻī“ķĪó£»±¾ĢāŃ”B”£
æ¼µć:ŃĪĄąĖ®½āĘ½ŗāÓ¦ÓĆ”£


 ĘߊĒĶ¼ŹéæŚĖćĖŁĖćĢģĢģĮ·ĻµĮŠ“š°ø
ĘߊĒĶ¼ŹéæŚĖćĖŁĖćĢģĢģĮ·ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÓĆO2½«HCl×Ŗ»ÆĪŖCl2£¬æÉĢįøߊ§Ņę£¬¼õÉŁĪŪČ¾£¬
£Ø1£©“«Ķ³ÉĻøĆ×Ŗ»ÆĶعżČēÓŅĶ¼ĖłŹ¾µÄ“߻ƼĮŃ»·ŹµĻÖ£¬

ĘäÖŠ£¬·“Ó¦¢ŁĪŖ£ŗ2HCl(g) + CuO(s) 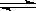 H2O(g)+CuCl2(g) ”÷H1
H2O(g)+CuCl2(g) ”÷H1
·“Ó¦¢ŚÉś³É1molCl2 (g)µÄ·“Ó¦ČČĪŖ”÷H2£¬Ōņ×Ü·“Ó¦µÄČČ»Æѧ·½³ĢŹ½
(g)µÄ·“Ó¦ČČĪŖ”÷H2£¬Ōņ×Ü·“Ó¦µÄČČ»Æѧ·½³ĢŹ½
ĪŖ , (·“Ó¦ČČÓĆ”÷H1ŗĶ”÷H2±ķŹ¾)”£
£Ø2£©ŠĀŠĶRuO2“߻ƼĮ¶ŌÉĻŹöHCl×Ŗ»ÆĪŖCl2µÄ×Ü·“Ó¦¾ßÓŠøüŗĆµÄ“ß»Æ»īŠŌ£¬
¢ŁŹµŃé²āµĆŌŚŅ»¶ØŃ¹ĒæĻĀ£¬×Ü·“Ó¦µÄHClĘ½ŗā×Ŗ»ÆĀŹĖęĪĀ¶Č±ä»ÆµÄØ»HCl”ŖTĒśĻßČēĶ¼12£¬
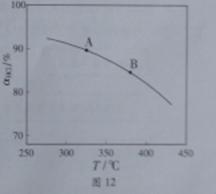
Ōņ×Ü·“Ó¦µÄ”÷H 0 ,£ØĢī”°£¾”±”¢”°©”±»ņ”°£¼”±£©£»A”¢BĮ½µćµÄĘ½ŗā³£ŹżK(A)ÓėK(B)ÖŠ½Ļ“óµÄŹĒ ”£
¢ŚŌŚÉĻŹöŹµŃéÖŠČōŃ¹ĖõĢå»żŹ¹Ń¹ĒæŌö“󣬻³öĻąÓ¦Ø»HCl”ŖTĒśĻߵď¾ŅāĶ¼£¬²¢¼ņŅŖĖµĆ÷ĄķÓÉ£ŗ ”£
¢ŪĻĀĮŠ“ėŹ©ÖŠÓŠĄūÓŚĢįøßØ»HClµÄÓŠ ”£
 A”¢Ōö“ón(HCl) B”¢Ōö“ón(O2)
A”¢Ōö“ón(HCl) B”¢Ōö“ón(O2)
C”¢ Ź¹ÓĆøüŗĆµÄ“ß»Æ¼Į D”¢ŅĘČ„H2O
Ź¹ÓĆøüŗĆµÄ“ß»Æ¼Į D”¢ŅĘČ„H2O
£Ø3£©Ņ»¶ØĢõ¼žĻĀ²āµĆ·“Ó¦¹ż³ĢÖŠn(Cl 2)µÄŹż¾ŻČēĻĀ£ŗ
2)µÄŹż¾ŻČēĻĀ£ŗ
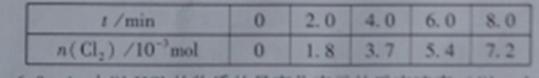
¼ĘĖć2.0”«6.0minÄŚŅŌHClµÄĪļÖŹµÄĮæ±ä»Æ±ķŹ¾µÄ·“Ó¦ĖŁĀŹ£ØŅŌmol”¤min-1ĪŖµ„Ī»£¬Š“³ö¼ĘĖć¹ż³Ģ£©”£
£Ø4£©Cl2ÓĆĶ¾ ¹ć·ŗ£¬Š“³öÓĆCl2ÖʱøĘÆ°×·ŪµÄ»Æѧ·½³ĢŹ½”£
¹ć·ŗ£¬Š“³öÓĆCl2ÖʱøĘÆ°×·ŪµÄ»Æѧ·½³ĢŹ½”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠÓŠ¹ŲNaClOŗĶNaCl»ģŗĻČÜŅŗµÄŠšŹöÕżČ·µÄŹĒ£ŗ
A£®øĆČÜŅŗÖŠ£¬H+”¢NH4+”¢SO42-”¢Br-æÉŅŌ“óĮæ¹²“ę
B£®øĆČÜŅŗÖŠ£¬Ag+”¢K+”¢NO3-”¢CH3CHOæÉŅŌ“óĮæ¹²“ę
C£®ĻņøĆČÜŅŗÖŠµĪČėÉŁĮæFeSO4ČÜŅŗ£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗ
2Fe2++ClO-+2H+=== Cl-+2Fe3++H2O
D£®ĻņøĆČÜŅŗÖŠ¼ÓČėÅØŃĪĖį£¬Ćæ²śÉś1molCl2£¬×ŖŅʵē×ÓŌ¼ĪŖ6.02”Į1023øö
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
Ä³ŃŠ¾æŠ”×齫“æ¾»µÄSO2ĘųĢåĶØČė0.1mol·L-1µÄBa£ØNO3£©2ČÜŅŗÖŠ£¬µĆµ½ĮĖBaSO4³Įµķ£¬ĪŖĢ½¾æÉĻŹöČÜŅŗÖŠŗĪÖÖĪ¢Į£ÄÜŃõ»ÆĶØČėµÄSO2£¬øĆŠ”×éĶ»³öĮĖČēĻĀ¼ŁÉč:
¼ŁÉč Ņ»£ŗČÜŅŗÖŠµÄNO3-
Ņ»£ŗČÜŅŗÖŠµÄNO3-
¼ŁÉ趞£ŗČÜŅŗÖŠČܽāµÄO2
£Ø1£© ŃéÖ¤¼ŁÉč
øĆŠ”×éÉę¼°ŹµŃéŃéÖ¤ĮĖ¼ŁÉčŅ»£¬ĒėŌŚĻĀ±ķæհד¦ĢīŠ“Ļą¹ŲŹµŃéĻÖĻó
| ŹµŃé²½Öč | ŹµŃéĻÖĻó | ½įĀŪ |
| ŹµŃé1£ŗŌŚŹ¢ÓŠ²»ŗ¬O2µÄ25ml0.1mol/LBaCl2ČÜŅŗµÄÉÕ±ÖŠ£¬»ŗĀżĶØČė“æ¾»µÄSO2ĘųĢå | ¼ŁÉčŅ»³ÉĮ¢ | |
| ŹµŃé2£ŗŌŚŹ¢ÓŠ²»ŗ¬O2µÄ25ml0.1mol/LBa£ØNO3£©2ČÜŅŗµÄÉÕ±ÖŠ£¬»ŗĀżĶØČė“æ¾»µÄSO2ĘųĢå |
£Ø2£©ĪŖÉīČėŃŠ¾æøĆ·“Ó¦£¬øĆŠ”×黹²āµĆÉĻŹöĮ½øöŹµŃéÖŠČÜŅŗµÄpHĖęĶØČėSO2Ģå»żµÄ±ä»ÆĒśĻßČėĻĀĶ¼
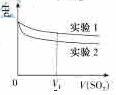
ŹµŃé1ÖŠČÜŅŗpH±äŠ”µÄŌŅņŹĒ____;V1Ź±£¬ŹµŃé2ÖŠČÜŅŗpHŠ”ÓŚŹµŃé1µÄŌŅņŹĒ£ØÓĆĄė×Ó·½³ĢŹ½±ķŹ¾£©_________”£
£Ø2£© ŃéÖ¤¼ŁÉ趞
ĒėÉč¼ĘŹµŃéŃéÖ¤¼ŁÉ趞£¬Š“³öŹµŃé²½Öč£¬Ō¤ĘŚĻÖĻóŗĶ½įĀŪ”£
| ŹµŃé²½Öč”¢Ō¤ĘŚĻÖĻóŗĶ½įĀŪ£Ø²»ŅŖĒ󊓾ßĢå²Ł×÷¹ż³Ģ£© |
£Ø3£© Čō¼ŁÉ趞³ÉĮ¢£¬ĒėŌ¤²ā£ŗŌŚĻąĶ¬Ģõ¼žĻĀ£¬·Ö±šĶØČė×ćĮæµÄO2ŗĶKNO3£¬Ńõ»ÆĻąĶ¬µÄH2SO3ČÜŅŗ£ØČÜŅŗĢå»ż±ä»ÆŗöĀŌ²»¼Ę£©£¬³ä·Ö·“Ó³ŗóĮ½ČÜŅŗµÄpHĒ°Õß_______(Ģī“óÓŚ»ņŠ”ÓŚ)ŗóÕߣ¬ĄķÓÉŹĒ
___________
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
FeCl3 ¾ßÓŠ¾»Ė®×÷ÓĆ£¬µ«øÆŹ“Éč±ø£¬¶ų¾ŪŗĻĀČ»ÆĢśŹĒŅ»ÖÖŠĀŠĶµÄŠõÄż¼Į£¬“¦ĄķĪŪĖ®±ČFeCl3 øߊ§£¬ĒŅøÆŹ“ŠŌŠ””£Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©FeCl3 ¾»Ė®µÄŌĄķŹĒ ”£FeCl3 ČÜŅŗøÆŹ“øÖĢśÉč±ø£¬³żH£«×÷ÓĆĶā£¬ĮķŅ»Ö÷ŅŖŌŅņŹĒ£ØÓĆĄė×Ó·½³ĢŹ½±ķŹ¾£© ”£
£Ø2£©ĪŖ½ŚŌ¼³É±¾£¬¹¤ŅµÉĻÓĆNaClO3 Ńõ»ÆĖįŠŌFeCl2 ·ĻŅŗµĆµ½FeCl3 ”£
¢ŁČōĖįŠŌFeCl2 ·ĻŅŗÖŠc(Fe2£«)=2.0”Į10-2mol”¤L-1, c(Fe3£«)=1.0”Į10-3mol”¤L-1, c(Cl£)=5.3”Į10-2mol”¤L-1,ŌņøĆČÜŅŗµÄPHŌ¼ĪŖ ”£
¢ŚĶź³ÉNaClO3 Ńõ»ÆFeCl2 µÄĄė×Ó·½³ĢŹ½£ŗ
| |
 ClO3-+
ClO3-+
|
 Fe2£«+
Fe2£«+ | |
 =
= | |
 Cl£+
Cl£+ | |
 Fe3£«+
Fe3£«+ | |
 .
. £Ø3£©FeCl3 ŌŚČÜŅŗÖŠ·ÖČż²½Ė®½ā£ŗ
Fe3£«+H2O  Fe(OH)2++H£« K1
Fe(OH)2++H£« K1
Fe(OH)2++H2O Fe(OH)2++H£« K2
Fe(OH)2++H£« K2
Fe(OH)++H2O Fe(OH)3+H£« K3
Fe(OH)3+H£« K3
ŅŌÉĻĖ®½ā·“Ó¦µÄĘ½ŗā³£ŹżK1”¢K2”¢K3Óɓ󵽊”µÄĖ³ŠņŹĒ ”£
ĶعżæŲÖĘĢõ¼ž£¬ŅŌÉĻĖ®½ā²śĪļ¾ŪŗĻ£¬Éś³É¾ŪŗĻŃõ»ÆĢś£¬Ąė×Ó·½³ĢŹ½ĪŖ£ŗ
xFe3++yH2O Fex(OH)y(3x-y)++yH+
Fex(OH)y(3x-y)++yH+
 ÓūŹ¹Ę½ŗāÕżĻņŅʶÆæɲÉÓƵķ½·ØŹĒ£ØĢīŠņŗÅ£© ”£
ÓūŹ¹Ę½ŗāÕżĻņŅʶÆæɲÉÓƵķ½·ØŹĒ£ØĢīŠņŗÅ£© ”£
a.½µĪĀ b.¼ÓĖ®Ļ”ŹĶ c.¼ÓČėNH4Cl d.¼ÓČėNaHCO3
ŹŅĪĀĻĀ£¬Ź¹ĀČ»ÆĢśČÜŅŗ×Ŗ»ÆĪŖøßÅØ¶Č¾ŪŗĻĀČ»ÆĢśµÄ¹Ų¼üĢõ¼žŹĒ ”£
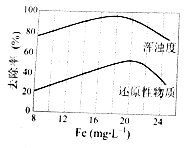
£Ø4£©Ģģ½ņijĪŪĖ®“¦Ąķ³§ÓĆĀČ»ÆĢś¾»»ÆĪŪĖ®µÄ½į¹ūČēĻĀĶ¼ĖłŹ¾”£ÓÉĶ¼ÖŠŹż¾ŻµĆ³öĆæÉżĪŪĖ®ÖŠĶ¶·Å¾ŪŗĻĀČ»ÆĢś[ŅŌFe(mg”¤L-1)±ķŹ¾]µÄ×ī¼Ń·¶Ī§Ō¼ĪŖ mg”¤L-1”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŹŅĪĀĻĀĻņ10mL0.1 mol·L£1NaOHČÜŅŗÖŠ¼ÓČė0.1 mol·L£1µÄŅ»ŌŖĖįHAČÜŅŗpHµÄ±ä»ÆĒśĻßČēĶ¼ĖłŹ¾”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®aµćĖłŹ¾ČÜŅŗÖŠc(Na+)>c(A—)>c(H+)>c(HA)
B£®a”¢bĮ½µćĖłŹ¾ČÜŅŗÖŠĖ®µÄµēĄė³Ģ¶ČĻąĶ¬
C£®pH=7Ź±£¬c(Na+)= c(A—)+ c(HA)
D£®bµćĖłŹ¾ČÜŅŗÖŠc(A—)> c(HA)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠ¹ŲÓŚÓŅĶ¼ĖłŹ¾×Ŗ»Æ¹ŲĻµ£ØX“ś±ķĀ±ĖŲ£©µÄĖµ·Ø“ķĪóµÄŹĒ
A£®2H(g)+2X(g)£½2HX(g) ¦¤H3£¼0
B£®¦¤H1£½¦¤H2 + ¦¤H3
C£®Cl”¢Br”¢IµÄ·Ē½šŹōŠŌŅĄ“Ī¼õČõ£¬ĖłŅŌĶ¾¾¶¢ņĪüŹÕµÄČČĮæ
°“Cl”¢Br”¢IµÄĖ³ŠņŅĄ“ĪŌö¶ą
D£®Ķ¾¾¶¢ńÉś³ÉHCl·Å³öµÄČČĮæ±ČÉś³ÉHBrµÄ¶ą£¬ĖµĆ÷HCl
±ČHBrĪȶØ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
»ÆѧÓėÉś»ī”¢Éś²ś”¢»·¾³µČÉē»įŹµ¼ŹĆÜĒŠĻą¹Ų”£ĻĀĮŠŠšŹöÕżČ·µÄŹĒ(””””)
A£®Ļ”µÄŹ³ŃĪĖ®ÄÜɱĖĄH7N9ĒŻĮ÷øŠ²”¶¾
B£®µÓĀŚ”¢ĖÜĮĻ”¢¹āµ¼ĻĖĪ¬¶¼ŹĒÓŠ»śøß·Ö×Ó²ÄĮĻ
C£®ÓƵē¶Ę³§µÄ·ĻĖ®Ö±½Ó¹ąøČÅ©Ģļ£¬æÉĢįøßĖ®µÄĄūÓĆĀŹ
D£®ĶāŠĪĖĘŗ£Ćą”¢ĆܶȊ””¢ÓŠ“ÅŠŌµÄĢ¼ÓėŹÆÄ«»„ĪŖĶ¬ĖŲŅģŠĪĢå
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com