
| A.新制的氯水在光照下颜色变浅 |
| B.Fe(SCN)3溶液中加入6mol/L NaOH溶液后颜色变浅 |
| C.在合成氨的反应中,降温或加压有利于氨的合成 |
| D.H2、I2、HI平衡混合气加压后颜色变深 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:单选题
 2NO2 △H<0 ,反应中NO的转化率与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达到平衡状态,且v(正)>v(逆)的点是 ( )
2NO2 △H<0 ,反应中NO的转化率与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达到平衡状态,且v(正)>v(逆)的点是 ( ) 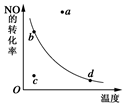
| A.a点 | B.b点 | C.c点 | D.d点 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 B(g); △H < O在测定A的相对分子质量时,下列条件中测定结果误差最小的是( )
B(g); △H < O在测定A的相对分子质量时,下列条件中测定结果误差最小的是( )| A.温度150℃、压强5.05×104 Pa | B.温度150℃、压强4.04×105 Pa |
| C.温度25℃、压强1.0 1 × 105 Pa | D.温度0℃、压强5.05×104 Pa |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

A.2SO3(g) 2SO2(g)+O2(g) ΔH>0 2SO2(g)+O2(g) ΔH>0 |
B.N2(g)+3H2(g) 2NH3(g) ΔH<0 2NH3(g) ΔH<0 |
C.4NH3(g)+5O2(g) 4NO(g)+6H2O(g) ΔH<0 4NO(g)+6H2O(g) ΔH<0 |
D.H2(g)+CO(g) C(s)+H2O(g) ΔH>0 C(s)+H2O(g) ΔH>0 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.K值越大,表示化学反应速率越大 |
| B.对任一可逆反应,温度升高,则K值增大 |
| C.一般情况下K值越大,可逆反应进行的越彻底 |
| D.加入催化剂或增大反应物的浓度时,K值均增大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 4NO2(g)+ O2(g),△H﹥0.反应物和部分生成物的物质的量随反应时间变化的曲线如图所示,下列说法正确的是
4NO2(g)+ O2(g),△H﹥0.反应物和部分生成物的物质的量随反应时间变化的曲线如图所示,下列说法正确的是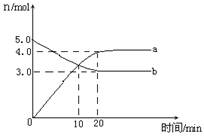
| A.10min时,反应达到平衡 |
| B.该温度下反应的平衡常数为8 |
| C.0~20min内平均反应速率v(N2O5)=0.05mol?L-1?min-1 |
| D.曲线a表示NO2的物质的量随反应时间的变化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
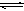 ?aZ(g)+W(g) ΔH=-QkJ/mol(Q>0)
?aZ(g)+W(g) ΔH=-QkJ/mol(Q>0)| A.2 mol X、1 mol Y、1 mol Ar | B.a mol Z、1 mol W |
| C.1 mol X、0.5 mol Y、0.5a mol Z、0.5 mol W | D.2 mol X、1 mol Y、1 mol Z |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.一定增大 | B.一定减小 | C.一定不变 | D.不能确定 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 H2(g) + CO2(g) △H= a kJ·mol-1 的平衡常数随温度的变化如下表:
H2(g) + CO2(g) △H= a kJ·mol-1 的平衡常数随温度的变化如下表: | 温度/℃ | 400 | 500 | 850 |
| 平衡常数 | 9.94 | 9 | 1 |
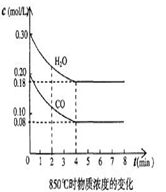
| 时间(min) | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com