���
�⣺��1��H
2��g����ȼ���ȡ�HΪ-285.8kJ?mol
-1���÷�Ӧ���Ȼ�ѧ����ʽΪ��2H
2��g��+O
2��g���T2H
2O��l������H=-571.68kJ?mol
-1��ˮ�ֽ���Ȼ�ѧ����ʽΪ��2H
2O��l���T2H
2��g��+O
2��g������H=+571.68kJ?mol
-1���ɴ��Ȼ�ѧ����ʽ��֪ÿ2molˮ��������571.6kJ���������������18gˮ�ֽ������ĵ�����Ϊ��
��571.6kJ=285.8 kJ���ʴ�Ϊ��285.8��
��2��CO��g����CH
3OH��l����ȼ���ȡ�H�ֱ�Ϊ-285.8kJ?mol
-1��-283.0kJ?mol
-1��-726.5kJ?mol
-1�������ǵ��Ȼ�ѧ����ʽ�ֱ�Ϊ��
��2CO��g��+O
2��g���T2CO
2��g������H
1=-466kJ?mol
-1��CH
3OH��g��+O
2��g���TCO
2��g��+2H
2O��l������H
2=-726.5kJ?mol
-1Һ̬�״�����ȫȼ������һ����̼�����Һ̬ˮ���ɿ�����������-�١�
�õ�����Ӧ��Ҳ���ڡ�H
2-
��H
1=-443.55kJ?mol
-1�������Ȼ�ѧ����ʽ��дΪ��CH
3OH��g��+O
2��g���TCO��g��+2H
2O��l����H=-443.55kJ?mol
-1��
�ʴ�Ϊ��CH
3OH��g��+O
2��g���TCO��g��+2H
2O��l����H=-443.55kJ?mol
-1��
��3����A����Ӧ�����Ƿ�Ӧ��ij���ʵ�Ũ���ڵ�λʱ���ڵı仯����v��CH
3OH��=
=
mol?L
-1?min
-1����A����
B��T
2��T
1��T
2ƽ��ʱ���״��������٣���˵�����淴ӦCO
2+3H
2?CH
3OH+H
2O���淴Ӧ�����ƶ���������ӦΪ���ȷ�Ӧ����B��ȷ��
C�����ݷ�ӦCO
2��g��+3H
2��g��?CH
3OH��g��+H
2O��g���Ƿ��ȷ�Ӧ��֪�������¶ȣ�ƽ�����淴Ӧ�����ƶ����÷�Ӧ��T
1ʱ��ƽ�ⳣ����T
2ʱ�Ĵ�C����
D������A��ķ�Ӧ��ϵ��T
1�䵽T
2�������¶ȣ��״������ʵ�����С��ƽ�����淴Ӧ�����ƶ�����D��ȷ��
�ʴ�Ϊ��BD��
�ڸ��ݿ��淴Ӧ�ﵽƽ��״̬��һ���������淴Ӧ������ȣ�����ֵ�Ũ�ȡ��ٷֺ������ٱ仯����֪��
A��H
2�İٷֺ������ֲ��䣬��Ӧ����ƽ��״̬����A��ȷ��
B��������CO
2Ũ����H
2Ũ��֮���ڷ�Ӧ������ʼ��Ϊ1��3���ʲ�����Ϊ��Ӧ�Ƿ���ƽ��״̬���жϱ�־����B����
C���÷�Ӧ�ں��������½��У���Ӧǰ�����������ʼ�ղ��䣬Ҳ����˵��Ӧ�����У��ܶ�û�б仯����������л��������ܶȱ��ֲ��䲻����Ϊƽ��״̬���жϱ�־����C����
D��CO
2����������CH
3OH�������ʶ���ָ����Ӧ���ʣ������ж����淴Ӧ�����Ƿ���ȣ�Ҳ�Ͳ���˵����Ӧ�Ƿ���ƽ��״̬����D����
�ʴ�Ϊ��A��
��4�����ݻ�ѧ��Ӧ��Ԫ���غ㣬���ƶϳ�CO
2��4H
2��Ӧ����2H
2O�⣬����һ������Ӧ����CH
4���ʴ�Ϊ��CH
4��
��5����ȼ�ϵ����ԭ��ص�һ�֣�����ʧ���ӷ���������Ӧ�������õ��ӷ�����ԭ��Ӧ���ڼ״�ȼ�����ɶ�����̼��ˮ�ķ�Ӧ�У��״��ǻ�ԭ���������������������Լ״������������õ��ӷ�Ӧ�������ڸ�������ʧ���ӷ�Ӧ���������Խ����У������������ɴ��������ӣ������ʲ���缫��Ӧ�����Լ״�ȼ�ϵ�صĸ�����ӦʽΪCH
3OH+H
2O-6e
-=CO
2+6H
+��������ӦʽO
2+4H
++4e
-=2H
2O���ʴ�Ϊ��O
2+4H
++4e
-=2H
2O��CH
3OH+H
2O-6e
-=CO
2+6H
+��

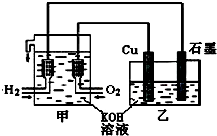
 ����̫���ֽܷ�ˮ����H2���ڴ���������H2��CO2��Ӧ�ϳ�CH3OH����������ֱ���Լ״�Ϊȼ�ϵ�ȼ�ϵ�أ���֪��
����̫���ֽܷ�ˮ����H2���ڴ���������H2��CO2��Ӧ�ϳ�CH3OH����������ֱ���Լ״�Ϊȼ�ϵ�ȼ�ϵ�أ���֪��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
 ������ͼװ����ȡCu2O���ҵ��ܷ�Ӧ��ѧ����ʽΪ��2Cu+H2O=Cu2O+H2��������˵����ȷ���ǣ�������
������ͼװ����ȡCu2O���ҵ��ܷ�Ӧ��ѧ����ʽΪ��2Cu+H2O=Cu2O+H2��������˵����ȷ���ǣ�������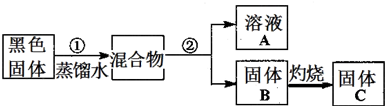
 ����β���dz�����Ҫ������Ⱦ��о���������β����Ϊ������������Ҫ����
����β���dz�����Ҫ������Ⱦ��о���������β����Ϊ������������Ҫ����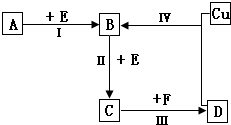 ������λ�ڶ����ڵ��������ڡ���������ķǽ���Ԫ��X��Y����֪��Ԫ������������ˮ�����Ϊǿ�ᣮ������ͼת����ϵ����Ӧ���������ֲ�������ȥ�����ش��������⣺
������λ�ڶ����ڵ��������ڡ���������ķǽ���Ԫ��X��Y����֪��Ԫ������������ˮ�����Ϊǿ�ᣮ������ͼת����ϵ����Ӧ���������ֲ�������ȥ�����ش��������⣺