
下列过程中需要吸收热量的是:
① N2→2N ② 2Cl→Cl2 ③ SO3+ H2O = H2SO4
④ Zn +2 HCl = ZnCl2 + H2↑ ⑤ 2KOH + H2SO4 = 2H2O +K2SO4
⑥ 2NH4Cl +Ba(OH)2·8H2O = BaCl2 + 2NH3↑ +10H2O
⑦ 食物腐败
A.①⑥ B.①③⑥ C.③④⑥⑦ D.②③④⑤⑦
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
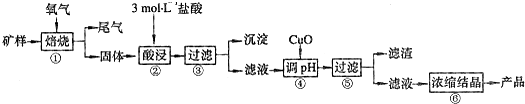
| ||
| ||
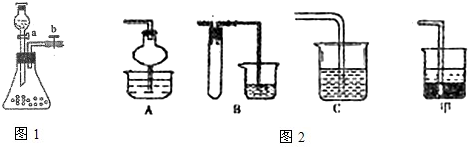
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 溶解度/g/100g水 | 18.5 | 20.8 | 26.3 | 32.8 | 40.1 | 48.4 | 52.4 | 50.9 | 43.7 |
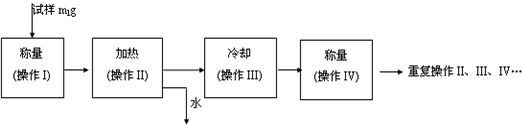
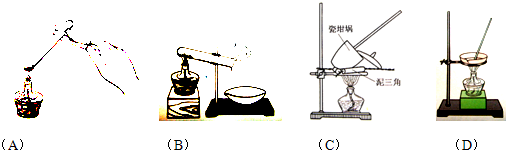
查看答案和解析>>
科目:高中化学 来源: 题型:

| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe3+ | 1.9 | 3.2 |
| Fe2+ | 7.0 | 9.0 |
| Mg2+ | 9.5 | 11.0 |



查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铝热反应属于吸热反应 | B、若某反应的反应物的总能量大于生成物的总能量,则该反应为吸热反应 | C、吸热反应是指需要加热才能进行的反应 | D、H2与Cl2的反应过程中,旧的共价键断裂吸收能量,新的共价键生成放出能量 |
查看答案和解析>>
科目:高中化学 来源:专项题 题型:填空题


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com