
在常温下,今将Na2S和NaHS两种盐[设n(Na2S)/n(NaHS)=k,0<k≤3],溶于水得稀溶液,下列有关溶液中微粒的浓度关系正确的是
A.若k=1,则:c(HS-)> c(S2-)>c(H+)>c(OH-)
B.若k=2,则:c(OH-)=c(H+)+c(HS-)+2c(H2S)
C.k为任意值时:c(Na+)+c(H+)=c(HS-)+2c(S2-)+c(OH-)
D.若满足:3c(H+)+2c(HS-)+5c(H2S)=3c(OH-)+c(S2-),则可确定k=3
科目:高中化学 来源:2014-2015学年四川省广安市高三二诊理综化学试卷(解析版) 题型:选择题
下列说法正确的是
A.分馏、蒸馏、煤的液化都是物理变化,干馏、裂化、裂解都是化学变化
B.乙烯和聚乙烯均能和溴水发生加成反应而使溴水褪色
C.需要加热的反应不一定是吸热反应
D.根据是否具有丁达尔效应, 将分散系分为溶液、浊液和胶体
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省德州市高三下学期3月一模化学试卷(解析版) 题型:实验题
(17分)用含少量铁的氧化物的氧化铜制取硫酸铜晶体( CuSO4.xH2O)。其流程如下:
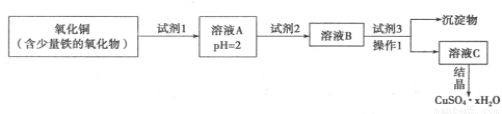
已知:在pH为4~5时,Fe3+几乎完全水解而沉淀,而此时Cu2+却几乎不水解。
(1)溶液A中可能含有Fe2+,确定该溶液中Fe2+存在的试剂是_______(填序号)
A.H2O2 B.NaOH C.K3[Fe(CN)6] D.KSCN
(2)欲用(1)中选择的检验试剂测定溶液A中Fe2+的浓度,实验前,首先要配制一定物质的量浓度的检验试剂的溶液250mL,配制时需要的仪器除天平、玻璃棒、烧杯、药匙、250mL容量瓶外,还需_______,下列滴定方式中,最合理的是_______(夹持部分略去)
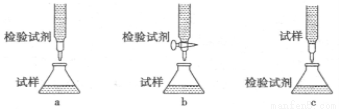
判断达到滴定终点的方法是__________________________________.
写出滴定反应的离子方程式__________________________________.
(3)试剂1为________,试剂2的作用为________,操作1的名称为________。
(4)要得到较纯的产品,试剂3可选用________。
a.NaOH
b.CuO
c.FeO
d.Cu(OH)2
e.Cu2(OH)2CO3
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东肥城市高三一模理综化学试卷(解析版) 题型:选择题
下表中的实验操作能达到实验目的或能得出相应结论的是
选项 | 实验操作 | 实验目的或结论 |
A | 向一定浓度的Na2SiO3溶液中通入适量CO2气体 | H2SiO3的酸性比H2CO3的酸性强 |
B | 取少量KClO3晶体溶于适量的蒸馏水,再加入硝酸酸化的AgNO3溶液 | 检验KClO3中的氯元素 |
C | 向某溶液中滴加Ba(NO3)2溶液产生白色沉淀,再加稀盐酸沉淀消失 | 说明原溶液中一定含有CO32— 或 SO32— |
D | 将混有Ca(OH)2杂质的Mg(OH)2样品,放入水中搅拌成浆状后,加入足量饱和氯化镁溶液充分搅拌、过滤,沉淀用蒸馏水洗涤 | 除去Mg(OH)2样品中的Ca(OH)2 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年宁夏银川市高三下学期第一次模考理综化学试卷(解析版) 题型:填空题
【化学——选修3:物质结构与性质】(15分)
I.S4N4的结构如图:
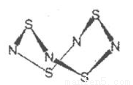
(1)S4N4的晶体类型是__ _。
(2)用干燥的氨作用于S2Cl2的CCl4,溶液中可制S4N4。化学反应方程为:6S2Cl2+16NH3= S4N4 +S8+12NH4Cl
①上述反应过程中,没有破坏或形成的微粒间作用力是__ _。
a.离子键
b.极性键
c.非极性键
d.金属键
e.配位键
f.范德华力
②S2Cl2中,S原子轨道的杂化类型是 __ __。
II.二甘氨酸合铜(II)是最早被发现的电中性内配盐,它的结构如图:
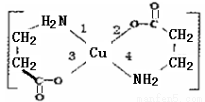
(3)基态Cu2+的最外层电子排布式为_ _。
(4)二甘氨酸合铜(II)中,第一电离能最大的元素与电负性最小的非金属元素可形成多种微粒,其中一种是5核10电子的微粒,该微粒的空间构型是 _ 。
(5)lmol二甘氨酸合铜(II)含有的二键数目是 _ 。
(6)二甘氨酸合铜(II)结构中,与铜形成的化学键中一定属于配位键的是 ______(填写编号)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年宁夏银川市高三下学期第一次模考理综化学试卷(解析版) 题型:选择题
下列各组物质发生化学反应时,由于反应物的量不同而生成不同产物的是
①CO2与NaOH溶液 ②NaHCO3溶液与盐酸 ③AgNO3溶液与氨水
④C与O2 ⑤AlCl3溶液与氨水
A.除③外 B.除②外 C.除②③⑤外 D.除②⑤外
查看答案和解析>>
科目:高中化学 来源:2014-2015浙江省湖州市高三上学期期末考试化学试卷(解析版) 题型:推断题
(8分)常见有机物A、B、C、D、E、G间的转化关系如下图所示(以下变化中,某些反应条件及产物未标明)。B是天然有机高分子化合物,C、D可发生银镜反应,在相同条件下,G蒸气密度是氦气的22倍。
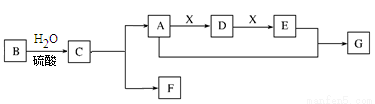
(1)B的分子式为 、G、的结构简式为 。
(2)E中官能团的名称 。
(3)A的同分异构体的结构简式 。
(4)A→D反应的化学方程式: 、其反应类型是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015宁夏银川市高二下学期3月月考化学试卷(解析版) 题型:填空题
(8分) Q、W、X、Y、Z元素为前四周期元素,且原子序数依次增大,Q元素的阳离子核外无电子,W元素原子的最外层电子数是次外层电子数的2倍,Y是地壳中含量最多的元素,Z的价电子排布式为3d64s2。
(1)Z位于元素周期表第________周期第________族,
(2)W的第一电离能________(填“大于”或“小于”)X的第一电离能。
(3)Z基态原子的价电子排布图为______________________________________,Z的单质与过量的X 的最高价氧化物对应的水化物的稀溶液反应的离子方程式为____________________。
(4)已知:①WQ4(g)+4XY2(g)=4XY(g)+WY2(g)+2Q2Y(g) ΔH=-574 kJ/mol
②WQ4(g)+4XY(g)=2X2(g)+WY2(g)+2Q2Y(g) ΔH=-1 160 kJ/mol
此温度下若用4.48 L(已折算成标准状况下)WQ4还原XY2至X2。整个过程中放出的热量为___kJ。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省丽水市高三第一次模拟理综化学试卷(解析版) 题型:实验题
(15分)硫代硫酸钠俗称保险粉,又名“大苏打”。可用于照相业作定影剂、纸浆漂白作脱氯剂,也可用于氰化物、砷、汞、铅、铋、碘等中毒的治疗,也是一种常用的实验试剂。
I.已知:Na2S2O3 + H2SO4 = Na2SO4 + S↓+ SO2 + H2O,某研究小组依据该反应探究外界条件对反应速率的影响,设计实验如下:
实验 编号 | 实验温度 /℃ | Na2S2O3 | H2SO4 | 蒸馏水体积 /mL | ||
体积/mL | 浓度/ mol·L-1 | 体积/mL | 浓度/ mol·L-1 | |||
① | 25 | 10 | 0.1 | 10 | 0.1 | 0 |
② | 25 | 5 | 0.1 | 10 | 0.1 | 5 |
③ | 25 | 5 | 0.2 | 10 | 0.2 | 5 |
④ | 50 | 5 | 0.1 | 10 | 0.1 | 5 |
⑤ | 50 | 10 | 0.2 | 5 | 0.2 | 5 |
下列有关说法正确的是
A.实验①和②探究其他条件不变时Na2S2O3浓度对相关反应速率的影响
B.实验①和③溶液变浑浊的时间相同
C.其他条件不变时,探究温度对化学反应速率的影响,应选择实验③和⑤
D.该同学在实验中采用的研究方法是实验比较法
II.实验室用SO2通入Na2S和Na2CO3的混合溶液中来制备硫代硫酸钠。反应原理为:
2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2
本实验对Na2S纯度要求较高,利用图1所示的装置可将工业级的Na2S提纯。已知Na2S常温下微溶于酒精,加热时溶解度迅速增大,杂质不溶于酒精。提纯过程为:将已称量好的工业级Na2S放入圆底烧瓶中,加入一定质量的酒精和少量水。按图1所示装配所需仪器,向冷凝管通入冷却水,同时水浴加热。待烧瓶中固体不再减少时,停止加热。将烧瓶取下,立即趁热过滤,再冷却结晶,过滤。将所得固体洗涤、干燥,得到Na2S·9H2O晶体。
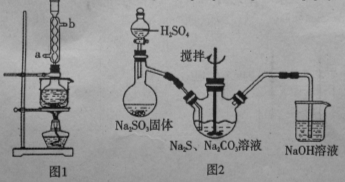
(1)在提纯过程中“趁热过滤”操作的目的是 ;
(2)用图2所示装置制取Na2S2O3,其中盛放Na2SO3固体的玻璃仪器名称是 ,NaOH溶液的作用是 。
(3)保险粉样品中Na2S2O3·5H2O的纯度(质量分数)可通过氧化还原滴定法测定,相关反应方程式为
2Na2S2O3+I2=2NaI+Na2S4O6。
准确称取W g样品于锥形瓶中,用适量蒸馏水溶解,并滴加淀粉溶液作指示剂。用0.1000 molL1碘的标准溶液进行滴定。
请回答:
①到达滴定终点的标志 ;
②滴定起始和终点的液面位置如图,则消耗碘的标准溶液体积为 mL,产品的纯度为 (设Na2S2O35H2O相对分子质量为M)。
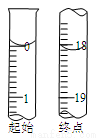
③若滴定时振荡不充分,刚看到溶液局部变色就停止滴定,则会使样品中Na2S2O3·5H2O的纯度的测量结果 (填“偏高”、“偏低”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com