
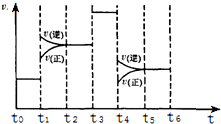
 化学反应3A2(g)+C2(g)?2CA3(g).当反应达到平衡时不断改变条件(不改变A2、C2和CA3的量),如图是反应速率与时间的关系图,其中表示平衡混合物中CA3含量最高的一段时间是
化学反应3A2(g)+C2(g)?2CA3(g).当反应达到平衡时不断改变条件(不改变A2、C2和CA3的量),如图是反应速率与时间的关系图,其中表示平衡混合物中CA3含量最高的一段时间是

 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A、气体甲可能为CO2 或者SO2 |
| B、沉淀丙中一定含有BaCO3,可能含有BaSO4 |
| C、该溶液中肯定存在的离子有K+、AlO2-、SO32-、SO42-、NO2- |
| D、只根据实验①能得出溶液中一定没有Fe3+、Ag+、Ba2+,K+是否存在无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、纯水在25℃和80℃时的pH值 |
| B、25℃时,pH=3的盐酸和AlCl3溶液中,水电离的氢离子的浓度 |
| C、耐火材料CaO和MgO的熔点 |
| D、1L pH=2的盐酸和醋酸溶液中,分别投入足量锌粒,放出H2的物质的量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将一小块铜片放入盛有浓硫酸的试管中加热反应后的溶液呈蓝色 |
| B、将一小块钠放入盛有水的烧杯中,钠在水面上游动,同时看到烧杯内的溶液变为红色 |
C、 如图,一段时间后给烧杯内的溶液中加入黄色的K3[Fe(CN)6]溶液,可看到Fe电极附近有蓝色沉淀生成 |
| D、向盛有少量Mg(OH)2沉淀悬浊液的试管中滴加氯化铵溶液,可看到沉淀溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 起始 n(A)/mol | 起始 n(B)/mol | 起始 n(C)/mol | 起始 n(D)/mol | 达到平衡时放出(或吸收)的热量 |
| 0 | 1.6 | 8 | 足量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质 | 杂质 | 除杂所用试剂和方法 | |
| A | KCl溶液 | I2 | 酒精,萃取 |
| B | KNO3 | K2SO4 | Ba(NO3)2溶液,过滤 |
| C | NaNO3 | CaCO3 | 加稀盐酸溶解、过滤、蒸发结晶 |
| D | H2 | CO2 | 依次通过盛有NaOH溶液和浓硫酸的洗气瓶 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
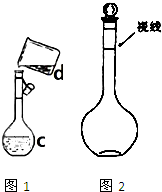 现需配制0.1mol/LNaOH溶液450mL,图1是某同学转移溶液的示意图.
现需配制0.1mol/LNaOH溶液450mL,图1是某同学转移溶液的示意图.查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
| A | 碳酸钠溶液可用于治疗胃酸过多 | Na2CO3可与盐酸反应 | Ⅰ对,Ⅱ对,有 |
| B | 铝制炊具最好不要盛放酸性、或碱性较强的液体食物 | 因为Al和Al2O3既可以与酸反应、又可以与碱反应 | Ⅰ对,Ⅱ错,无 |
| C | 铁是地壳中含量最高的金属元素 | 铁是人类最早使用的金属材料 | Ⅰ对,Ⅱ对,有 |
| D | 过氧化钠可用作航天员的供氧剂 | Na2O2能与CO2和H2O反应生成O2 | Ⅰ对,Ⅱ对,有 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com