
下列有关NA的说法正确的是( )
A.标准状况下,22.4L SO3中含有的分子数为NA个
B.2L 0.5 mol·L-1亚硫酸溶液中含有的H+离子数为2NA
C.过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.2NA
D.密闭容器中2mol NO和1mol O2充分反应,产物的分子数为2NA
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案科目:高中化学 来源:2017届山西省协作体高三上学期开学考试化学试卷(解析版) 题型:实验题
废弃物的综合利用既有利于节约资源,又有利于保护环境。实验室利用废旧电池的铜帽(Cu、Zn 总含量约为99%)回收Cu并制备ZnO 的部分实验过程如下:
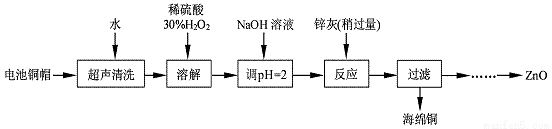
(1)写出铜帽溶解时铜与加入的稀硫酸、30%H2O2反应的离子反应方程式: ;铜帽溶解完全后,需加热(至沸)将溶液中过量的H2O2除去。
(2)为确定加入锌灰(主要成分为Zn、ZnO,杂质为铁及其氧化物)的量,实验中需测定除去H2O2 后溶液中Cu2+的含量。实验操作为:准确量取一定体积的含有Cu2+的溶液于带塞锥形瓶中,加适量水稀释,调节溶液pH=3~4,加入过量的KI,用Na2S2O3标准溶液滴定至终点。上述过程中反应的离子方程式如下:
2Cu2++4I-=2CuI(白色)↓+I2 2S2O32-+I2=2I-+S4O62-
①滴定选用的指示剂为 ,滴定终点观察到的现象为 ;
②某同学称取1.0g电池铜帽进行实验,得到100.00mL含有Cu2+的溶液,量取20.00mL上述含有Cu2+的溶液于带塞锥形瓶中,加适量水稀释,调节溶液pH=3~4,加入过量的KI,用0.1000mol/L Na2S2O3标准溶液滴定至终点。再重复操作实验3次,记录数据如下:
实验编号 | 1 | 2 | 3[ | 4 |
V(Na2S2O3)(mL) | 28.32 | 25.31 | 25.30 | 25.32 |
计算电池铜帽中Cu的质量分数为 ,(结果保留四位有效数字)若滴定前溶液中的H2O2没有除尽,则所测定c (Cu2+)将会 (填“偏高”、“偏低”或“无影响”);
(3)常温下,若向50mL 0.0001mol/L CuSO4溶液中加入50mL0.00022mol/LNaOH溶液,生成了沉淀。已知KSP[Cu (OH)2] =2.0×10-20(mol/L)3,计算沉淀生成后溶液中c(Cu2+)= mol/L;
(4)已知pH>11 时Zn(OH)2 能溶于NaOH溶液生成[Zn(OH)4]2-。下表列出了几种离子生成氢氧化物沉淀的pH(开始沉淀的pH 按金属离子浓度为1.0 mol·L-1计算)。
开始沉淀的pH | 沉淀完全的pH | |
Fe3+ | 1.1 | 3.2 |
Fe2+ | 5.8 | 8.8 |
Zn2+ | 5.9 | 8.9 |
实验中可选用的试剂:30%H2O2、1.0 mol·L-1HNO3、1.0 mol·L-1NaOH。由除去铜的滤液制备ZnO的实验步骤依次为:①向滤液中加入适量30% H2O2,使其充分反应;
② ;③过滤;
④ ;⑤过滤、洗涤、干燥;⑥900℃煅烧。
查看答案和解析>>
科目:高中化学 来源:2017届江西省南五校高三上学期第一次模拟考试化学试卷(解析版) 题型:填空题
为有效控制雾霾,各地积极采取措施改善大气质量。有效控制空气中氮氧化物、碳氧化物和硫氧化物显得尤为重要。
(1)在汽车排气管内安装催化转化器,可将汽车尾气中主要污染物转化为无毒的大气循环物质。
已知:① N2(g) + O2(g)  2NO(g) △H1=+180.5 kJ·mol-1
2NO(g) △H1=+180.5 kJ·mol-1
② C和CO的燃烧热(△H)分别为-393.5 kJ·mol-1和-283 kJ·mol-1
则2NO(g) + 2CO(g)  N2(g) + 2CO2(g)的△H=_____kJ·mol-1
N2(g) + 2CO2(g)的△H=_____kJ·mol-1
(2)将0.20 mol NO和0.10 mol CO充入一个容积为1L的密闭容器中,反应过程中物质浓度变化如图所示。
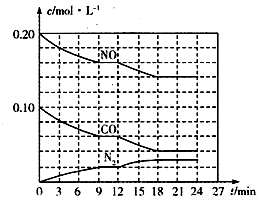
①CO在0-9min内的平均反应速率v(CO)=________mol·L-1·min-1(保留两位有效数字);第12 min时改变的反应条件可能为________。
A.升高温度 B.加入NO C.加催化剂 D.降低温度
②该反应在第24 min时达到平衡状态,CO2的体积分数为________(保留三位有效数字),化学平衡常数值为________(保留两位有效数字)。
(3)烟气中的SO2可用某浓度NaOH溶液吸收,若将一定量的SO2气体通入到300mL NaOH的溶液中,再在所得溶液中逐滴加入稀盐酸至过量,产生的气体与反应的HCl两者物质的量的关系如图所示(气体的溶解和HCl的挥发忽略,NaHSO3水溶液为酸性):
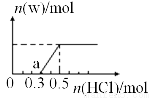
①O点溶液中所含溶质的化学式为_________________;
②a点溶液中各离子溶度大小关系为______________;
查看答案和解析>>
科目:高中化学 来源:2017届广东省汕头市高三上学期入学考理综化学试卷(解析版) 题型:选择题
在常温下,发生下列几种反应:
2KMnO4 + 16HCl = 2KCl + 2MnCl2 + 5Cl2↑ +8H2O
Cl2 + 2NaBr = 2NaCl + Br2 Br2 + 2FeBr2 = 2FeBr3
根据上述反应,下列结论正确的是( )
A.还原性强弱顺序为:Br—>Fe2+>Cl—
B.氧化性强弱顺序为:MnO4—>Cl2>Br2>Fe3+
C.反应·中,当生成1molCl2 时,被氧化的HCl为3.2mol
D.溶液中可发生反应:2Fe3+ + 2Cl— = 2Fe2+ + Cl2↑
查看答案和解析>>
科目:高中化学 来源:2017届广东省茂名市高三上学期8月月考化学试卷(解析版) 题型:实验题
某化学小组的同学利用如图所示装置进行某些气体的制备、性质等实验(图中夹持装置有省略)。

请回答:
(1)根据上述实验装置,为制备干燥NH3,可选用的发生、净化装置为 接 。其中发生装置中可以选用的药品为 (填选项字母)
a.碱石灰和浓氨水 b.浓H2SO4和浓氨水 c.碱石灰和氯化铵 d.生石灰和氯化铵
(2)根据上述实验装置,用MnO2和浓盐酸制备纯净、干燥的Cl2,可选用的发生、净化装置为 接E、接E,第一个E装置的药品是 。
(3)利用装置F可探究Cl2与 NH3 的反应。
已知Cl2与 NH3可发生反应:3Cl2+2NH3=N2+6HCl
①实验时打开开关1、3,关闭2,先向烧瓶中通入 (气体名称),然后关闭1、3,打开2,向烧瓶中缓慢通入一定量的另一种气体。
②实验一段时间后烧瓶内出现的现象为: 。
③装置F中烧杯内发生反应的离子方程式为 。
④请设计一个实验方案(操作过程、实验现象)鉴定烧瓶内最终产物的阳离子,其方案为 。
(4)一定条件下,Cl2 与CH4在装置F中发生反应,其有机产物有 。(填化学式)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年新疆石河子二中高二(下)期末化学试卷(解析版) 题型:实验题
氢化阿托醛(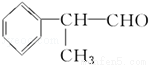 )是一种重要的化工原料,其合成路线如下:
)是一种重要的化工原料,其合成路线如下:
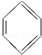
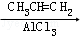

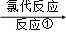 [A]
[A]
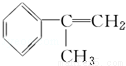

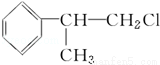
 [D](Mr=136)
[D](Mr=136)
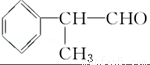
(1)在合成路线上①~⑤反应中,属于消去反应的为 (填反应序号).
(2)写出反应③、④的化学方程式: .
(3)在一定条件下,D与有机物X发生酯化反应生成E(Mr=164),则X的结构简式为 ,
写出满足下述两个条件的E的两种同分异构体的结构简式: .
a.属于羧酸 b.苯环上的一氯取代物只有一种结构.
查看答案和解析>>
科目:高中化学 来源:2015-2016学年新疆石河子二中高二(下)期末化学试卷(解析版) 题型:选择题
用分液漏斗可以分离的一组混合物是( )
A.溴苯和水 B.甘油和水 C.乙醇和乙二醇 D.乙酸和乙醇
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省高二(下)期末化学试卷(解析版) 题型:选择题
把一定质量的铁完全溶解于某浓度的硝酸中收集到0.3mol NO2和0.2mol NO.向反应后的溶液中加入足量NaOH溶液充分反应,经过滤、洗涤后,把所得沉淀加热至质量不再减少为止.得到固体质量不可能为( )
A.18 g B.24 g C.30 g D.36 g
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省益阳市国基实验学校高二(上)期中化学试卷(解析版) 题型:选择题
区分羊毛织品和尼龙布最简单的方法是( )
A.灼烧并闻气味 B.观察外观
C.放在水中比较柔软性 D.手摸,凭手感区分
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com