
【题目】图中的A为直流电源,B为渗透饱和氯化钠溶液和酚酞溶液的滤纸,C为电镀槽,接通电路后,发现B上的c点显红色。请填空:
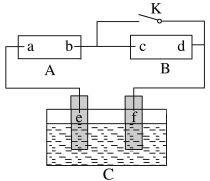
(1)电源A中a点为________极。
(2)滤纸B上发生氧化反应的电极反应方程式为:____________________。
(3)欲在电镀槽中实现铁上镀锌,接通K点,使c、d两点短路:
①电极e上发生的反应为:__________________;
②在此过程中电解液的浓度(填“始终不变”、“略微增大”、“略微减小”)___________;
③电镀槽中盛放的电镀液可以是________或________(只要求填两种电解质溶液)。
【答案】正 2Cl--2e-= Cl2↑ Zn-2e-=Zn2+ 始终不变 硫酸锌溶液 氯化锌溶液
【解析】
(1)A为直流电源,B为浸透饱和氯化钠溶液和酚酞试液的滤纸,C为电镀槽,接通电路后,发现B上的c点显红色,说明c点有氢氧根离子生成,所以c是阴极、d是阳极,则a是正极、b是负极,e是阳极、f是阴极;
(2)滤纸B上,阴极上氢离子放电生成氢气、同时电极附近有氢氧根离子生成,阳极上氯离子放电生成氯气;
(3)电镀时,镀层金属作阳极、镀件作阴极,含镀层金属的阳离子作电解质溶液。
(1)A为直流电源,B为浸透饱和氯化钠溶液和酚酞试液的滤纸,C为电镀槽,接通电路后,发现B上的c点显红色,说明c点有氢氧根离子生成,因此c电极是阴极、d电极是阳极,则a是正极、b是负极;
(2)滤纸B上,阴极上H+离子放电生成H2、同时阴极附近有OH-离子生成,在阳极上Cl-离子放电生成Cl2,所以c点的电极反应式为:2H++2e-=H2,d点的电极反应式为:2Cl--2e-=Cl2;
(3)①电镀时,镀层金属作阳极,镀件作阴极,含镀层金属的阳离子作电解质溶液,所以若在电镀槽中实现铁上镀锌,接通K点,使c、d两点短路,由于a为正极,b为负极,则e为阳极Zn,锌失电子发生氧化反应,电解反应为Zn-2e-=Zn2+,f为阴极Fe,在阴极上锌离子得;
②电子发生还原反应,由于在反应过程中溶液中Zn2+物质的量不变,溶液的体积不变,所以在此过程中电解液的浓度始终不变;
③电解液可以为ZnSO4或ZnCl2或Zn(NO3)2等溶液。


 高中必刷题系列答案
高中必刷题系列答案科目:高中化学 来源: 题型:
【题目】实验室欲用NaOH固体配制1.0mol·L-1的NaOH溶液480mL。
(1)配制时,必须使用的玻璃仪器有___。
(2)要完成本实验该同学应称出NaOH__g。
(3)某同学欲称量NaOH的质量,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图,烧杯的实际质量为__g。(砝码一个20克、一个10克)
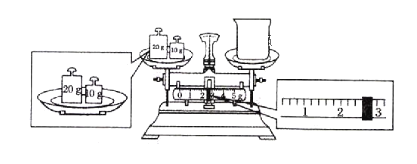
(4)使用容量瓶前必须进行的一步操作是__。
(5)在配制过程中,其他操作都是正确的,下列操作会引起误差偏高的是__。
①没有洗涤烧杯和玻璃棒
②定容时俯视刻度线
③未冷却到室温就将溶液转移到容量瓶并定容
④定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】热化学碘硫循环可用于大规模制氢气,HI分解和SO2水溶液还原I2均是其中的主要反应。回答下列问题:
(1)碘硫热化学循环中,SO2的水溶液还原I2的反应包括:SO2+I2+2H2O![]() 3H++HSO4- +2I- 、I-+I2
3H++HSO4- +2I- 、I-+I2![]() I3-。若起始时n(I2)=n(SO2)=1mo1,I- 、I3- 、H+ 、HSO4-的物质的量随(
I3-。若起始时n(I2)=n(SO2)=1mo1,I- 、I3- 、H+ 、HSO4-的物质的量随(![]() )的变化如图所示:
)的变化如图所示:
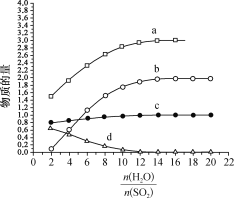
图中表示的微粒:a为_____________,d为____________________。
(2)起始时 HI的物质的量为1mo1,总压强为0.1MPa下,发生反应 HI(g) ![]()
![]() H2(g)+
H2(g)+![]() I2(g) 平衡时各物质的物质的量随温度变化如图所示:
I2(g) 平衡时各物质的物质的量随温度变化如图所示:
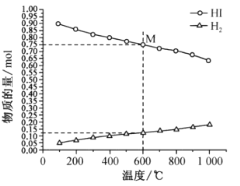
①该反应的△H __________________ (“>”或“<”)0。
②600℃时,平衡分压p(I2)= ______MPa,反应的平衡常数Kp=_____________ (Kp为以分压表示的平衡常数)。
(3)反应 H2(g)+I2(g) ![]() 2HI(g)的反应机理如下:
2HI(g)的反应机理如下:
第一步:I2![]() 2I(快速平衡)
2I(快速平衡)
第二步:I+H2![]() H2I(快速平衡)
H2I(快速平衡)
第三步:H2I+I ![]() 2HI (慢反应)
2HI (慢反应)
①第一步反应_____________ (填 “放出”或“吸收”)能量。
②只需一步完成的反应称为基元反应,基元反应如aA+dD = gG+hH 的速率方程,v= kca(A)cd(D),k为常数;非基元反应由多个基元反应组成,非基元反应的速率方程可由反应机理推定。H2(g)与I2(g)反应生成 HI(g)的速率方程为v= ________(用含k1、k-1、k2…的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂-空气电池由于具有较高的比能量而成为未来电动汽车的希望。其原理模型如图所示,下列说法不正确的是
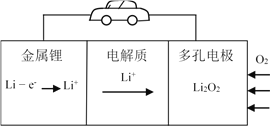
A. 可以用LiOH溶液做电解质溶液
B. 锂既是负极材料又是负极反应物
C. 正极反应为2Li+ + O2 + 2e- ![]() Li2O2
Li2O2
D. 正极采用多孔碳材料是为了更好的吸附空气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,重水(D2O)的离子积为 1.6×10ˉ15,也可用与 pH 一样的定义来规定其酸碱度:pD=-lgc(D+),下列叙述正确的是(均为 25℃条件下)
A.重水和水两种液体,D2O 的电离度大于 H2O
B.在 100mL0.25mol·Lˉ1DCl 重水溶液中,加入 50mL0.2mol·Lˉ1NaOD 重水溶液,反应后溶液的 pD=1
C.0.01 mol·Lˉ1NaOD 重水溶液,其 pD=12
D.NH4Cl 溶于 D2O 中生成的一水合氨和水合氢离子的化学式为 NH3·D2O 和 HD2O+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁、铝及其化合物在生产和生活中有着广泛的应用。
(1)某研究性学习小组设计了如图所示装置探究钢铁的腐蚀与防护。
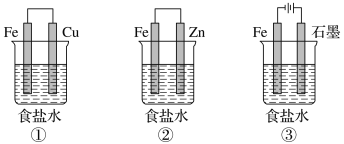
为防止金属Fe被腐蚀,可以采用上述________(填装置序号)装置原理进行防护;装置③中阴极产物为:_____________________。
(2)用甲烷或其他有机物、氧气为原料可设计成原电池,以CnH2nOn、O2为原料,硫酸溶液为电解质设计成燃料电池,则负极的电极反应式为:_________________。
(3)图1是在金属锌板上贴上一张用某溶液浸湿的滤纸,图2是NaBH4/H2O2燃料电池。
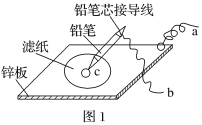
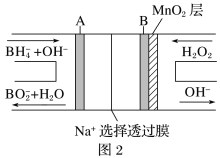
图2电池负极区的电极反应为:_______________;若用硫酸钠和酚酞的混合溶液浸湿滤纸,用导线将a、b直接相连,则滤纸出现________色,c位置的电极反应式为____________________,若用KI淀粉溶液浸湿滤纸,用导线将a、b与A、B电极相连,铅笔芯c点处出现蓝色,则b接的是___________(填A或B)电极。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某有机物K的合成路线如下所示:
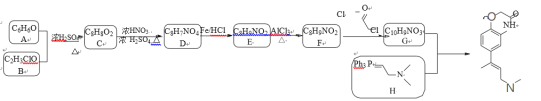
已知:①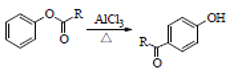
②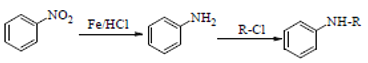
③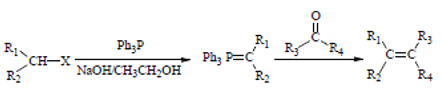
(Ph表示苯基,R、R1、R2、R2、R3表示烃基或氢原子)
(1)下列说法正确的是_________
A.有机物K的分子式为C14H17N2O2
B.可用FeCl3溶液来帮助判断反应E→F是否完全
C.已知RCOCl的性质与酯相似,1mol有机物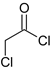 最多能与3molNaOH反应
最多能与3molNaOH反应
D.发生反应E→F,其有机物的水溶性增强
(2)写出有机物B的结构简式_________。
(3)写出F→G的化学方程式_________。
(4)请设计以乙醇和Ph3P为原料合成正丁烷的合成路线_________(用流程图表示,无机试剂任选)。
(5)写出化合物D(C8H7NO4)可能的同分异构体的结构简式_________。
须同时符合:①能使FeCl3溶液显紫色,1mol有机物能与足量银氨溶液反应生成4molAg;②1H-NMR谱显示分子中有4种氢原子;③分子中无N-O键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯酸钾和亚硫酸氢钾溶液能发生氧化还原反应:ClO3-+3HSO3-=3SO42-+Cl-+3H+
已知该反应的速率随c(H+)的增大而加快。下列为用ClO3-在单位时间内物质的量浓度变化表示的该反应v-t图。下列说法中不正确的是
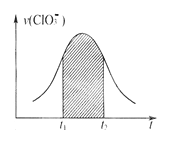
A. 反应开始时速率增大可能是c(H+)所致
B. 纵坐标为v(Cl-)的v-t曲线与图中曲线完全重合
C. 纵坐标为v(H+)的v-t曲线与图中曲线完全重合
D. 后期反应速率下降的主要原因是反应物浓度减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,电离常数:
化学式 | CH3COOH | H2CO3 | HCN |
电离常数 | 1.8×10-5 | K1:4.3×10-7 K2:5.6×10-11 | 4.9×10-10 |
请回答下列问题:
(1)物质的量浓度为0.1mol·L-1的下列四种物质:
a.Na2CO3 b.NaCN c.CH3COONa d.NaHCO3
pH由大到小的顺序是____(填标号)。
(2)25℃时,在0.5mol·L-1的醋酸溶液中由醋酸电离出的c(H+)约是由水电离出的c(H+)的__倍。
(3)写出向氰化钠溶液中通入少量二氧化碳的离子方程式:______。
(4)25℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中c(CH3COO-)-c(Na+)=___(填准确数值)。c(CH3COO-)/c(CH3COOH)=____。
(5)25℃时,将amol·L-1的醋酸与bmol·L-1氢氧化钠等体积混合,反应后溶液恰好显中性,用a、b表示醋酸的电离常数为____。
(6)某温度时,纯水的pH=6。该温度下0.01mol/LNaOH溶液的pH=___,向该温度下的纯水中加入少量的碳酸钠固体,使溶液pH为9,则水电离出的c(OH-)=____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com