
| A. | 氢氧化钠溶液、碳酸钠溶液、氯化钡溶液 | |
| B. | 氢氧化钠溶液、氯化钡溶液、碳酸钠溶液 | |
| C. | 氯化钡溶液、碳酸钠溶液、氢氧化钠溶液 | |
| D. | 碳酸钠溶液、氯化钡溶液、氢氧化钠溶液 |
分析 除钙离子用碳酸根,除镁离子用氢氧根,除硫酸根用钡离子,因为加入的试剂都是过量的,所以后加的试剂要把先加的试剂所带入的杂质除掉,主要是碳酸钠要在氯化钡之后加入,这样可以除去多余的钡离子.
解答 解:A.先加过量的碳酸钠,再加过量的氯化钡溶液,多余的钡离子不能被除去,故不能达到目的,故A错误;
B.先加氢氧化钠,除去镁离子,再加氯化钡,除去硫酸根,再加碳酸钠,除去钙离子和多余的钡离子,故B正确;
C.先加氯化钡,除去硫酸根,再加氢氧化钠,除去镁离子,再加碳酸钠,除去多余的钡离子和钙离子最后加氢氧化钠除去氯化镁,故C正确;
D.先加过量的碳酸钠,再加过量的氯化钡溶液,多余的钡离子不能被除去,故D错误.
故选BC.
点评 本题考查了除杂的原则,试剂必须过量,最后能除去,除杂时不仅要能把杂质除掉,还不能引入新杂质,而且方法要简便易行,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 18gD2O中含有的中子数为10 NA(设NA为阿伏加德罗常数的数值) | |
| B. | 电解精炼铜时,每转移1mol电子,阳极溶解铜的质量为32g | |
| C. | 恒温恒容下,某可逆反应X(g)+Y(g)?Z(g)+W(s)△H>0达平衡后再加入X,该反应的△H增大 | |
| D. | 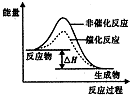 如图表示某放热反应分别在有、无催化剂的情况下反应过程中的能量变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(SO3)=0.4 mol•L-1 | B. | c(SO2)=c(SO3)=0.15 mol•L-1 | ||
| C. | c(SO2)=0.25 mol•L-1 | D. | c(SO2)+c(SO3)=0.5 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硅胶 | B. | 硫酸亚铁 | C. | 食盐 | D. | 石灰石 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.0gH218O与D2O的混合物中所含中子数为NA | |
| B. | 一定条件下,1 mol N2与足量H2反应生成NH3,转移电子6NA | |
| C. | 1L0.1 mol•L-1(NH4)2SO4溶液中含有0.2NA个NH4+ | |
| D. | 50mL12mol/L盐酸与足量MnO2共热,转移的电子数为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 需要加热才发生的化学反应,反应物的总能量可能高于生成物的总能量 | |
| B. | 已知:H2(g)+F2(g)═2HF(g)△H=-270 kJ•mol-1,则1 mol氢气与1 mol氟气反应生成2 mol液态氟化氢放出的热量小于270 kJ | |
| C. | 500℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为N2(g)+3H2(g)═2NH3(g)△H=-38.6 kJ•mol-1 | |
| D. | 已知:C(s,金刚石)═C(s,石墨)△H=-1.5 kJ•mol-1,说明金刚石更稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在12 g单层石墨中,含六元环的数目为1NA | |
| B. | 50mL 18.4mol•L-1浓硫酸与足量铜加热充分反应,生成SO2分子的数目为0.46 NA | |
| C. | 42 g由乙烯和环丙烷组成的混合气体中,碳氢键的数目为6NA | |
| D. | 1mol过氧化钠与足量CO2充分反应,转移的电子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加水时,平衡向逆反应方向移动 | |
| B. | 加入少量NaOH固体,平衡向正反应方向移动 | |
| C. | 加入少量0.1 mol•L-1盐酸,溶液中c(H+)减小 | |
| D. | 加入少量CH3COONa固体,平衡向正反应方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com