
【题目】胶体区别于其他分散系的本质特征是( )
A.胶体的分散质能通过滤纸空隙,而浊液的分散质不能
B.胶体能产生丁达尔效应
C.胶体分散质粒子直径在1nm~100nm之间
D.胶体在一定条件下能稳定存在
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值。下列说法正确的是
A. 常温常压下,17g甲基(—14CH3)所含的中子数为8NA
B. 1.0L0.1mol/LNaAlO2溶液中含有的氧原子数为0.2NA
C. 1molNa2O和BaO2的混合物中含有的阴、阳离子总数为3NA
D. 标准状况下,1L己烷完全燃烧后生成的气态产物分子数为![]() NA
NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物结构简式如图,下列关于该有机物的说法正确的是
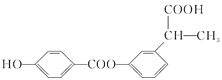
A. 1 mol 该有机物含有 6 mol 碳碳双键
B. 1 mol 该有机物完全燃烧可生成9 mol H2O
C. 1 mol 该有机物可电离生成2 mol H+
D. 1 mol 该有机物最多可与6 mol H2 发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,表中列出11种元素在周期表中的位置,按要求回答下列各题:
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ⑥ | ⑧ | ||||||
3 | ① | ③ | ⑤ | ⑦ | ⑨ | |||
4 | ② | ④ | ⑩ |
(1)这11种元素中,化学性质最不活泼的元素是______(填元素符号,下同),得电子能力最强的原子是______,失电子能力最强的单质与水反应的化学方程式是___________________,常温下单质为液态的非金属单质是____________。
(2)元素④的离子结构示意图为__________________。
(3)⑥⑦⑧气态氢化物的化学式分别为________、________、________,其中以
(4)写出③的单质置换出⑥的单质的化学方程式:__________________。
①和⑤两种元素最高价氧化物对应的水化物相互反应的离子方程式为_____________。
②和⑨两种元素最高价氧化物对应的水化物相互反应的离子方程式为_____________。
②的最高价氧化物对应水化物的水溶液与⑤的最高价氧化物反应的化学方程式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为模拟海水制备 MgO,某同学设计并完成了如下实验:
模拟海水中离子c(mol/L) | Na+ | Mg2+ | Ca2+ | Cl― | HCO3 |
0.439 | 0.050 | 0.011 | 0.560 | 0.001 |
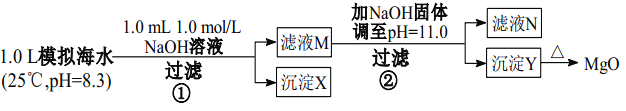
下列说法正确的是
A. 模拟海水呈碱性,可说明 HCO3-的电离能力大于水解能力
B. 沉淀物 X 为 CaCO3,沉淀物 Y 为 Mg(OH)2
C. MgCO3的溶解度比 Mg(OH)2 的小
D. 滤液 M 中存在 Mg2+,不存在 Ca2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用化学用语作答
(1)书写电子式:H2____________N2_________CH4_________NaOH_________
(2)用电子式表示物质的形成过程
MgCl2_______________________________________
H2O_______________________________________
(3)两种含10电子的粒子反应生成两种10电子的粒子的离子方程式______________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家正在研究温室气体CH4和CO2的转化和利用。请回答下列问题:
(1)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用____________形象化描述。在基态14C原子中,核外存在___________对自旋相反的电子。
(2)CH4和CO2所含的三种元素电负性从小到大的顺序为__________________________。
(3)一定条件下,CH4和CO2都能与H2O形成笼状结构(如下图所示)的水合物晶体,其相关参数见下表。CH4与H2O形成的水合物俗称“可燃冰”。
参数 分子 | 分子直径/nm | 分子与H2O的结合能E/kJ·mol-1 |
CH4 | 0.436 | 16.40 |
CO2 | 0.512 | 29.91 |
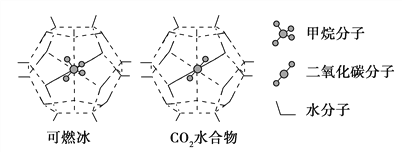
①下列关于CH4和CO2的说法正确的是________(填序号)。
a.CO2分子中含有2个σ键和2个π键
b.CH4分子中含有极性共价键,是极性分子
c.因为碳氢键键能小于碳氧键,所以CH4熔点低于CO2
d.CH4和CO2分子中碳原子的杂化类型分别是sp3和sp
②为开采深海海底的“可燃冰”,有科学家提出用CO2置换CH4的设想。已知上图中笼状结构的空腔直径为0. 586 nm,根据上述图表所提供的数据分析,提出该设想的依据是______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃,两种酸的电离常数如下右表。下列说法正确的是
酸 | Ka1 | Ka2 |
H2SO3 | 1.3×10-2 | 6.3×10-6 |
H2CO3 | 4.2×10-7 | 5.6×10-11 |
A. H2CO3的电离方程式为H2CO3![]() 2H++CO
2H++CO![]()
B. 酸性强弱顺序为H2SO3>H2CO3>HSO>HCO
C. 0.2 mol/L Na2CO3溶液中离子浓度大小顺序为:c(Na+)>c(CO![]() )>c(HCO)>c(OH-)>c(H+)
)>c(HCO)>c(OH-)>c(H+)
D. 足量SO2气体通入NaHCO3溶液中,反应的离子方程式为SO2+HCO==HSO+CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列鉴别物质的方法能达到目的的是
A. 用氨水鉴别MgCl2溶液和A1C13溶液
B. 用澄淸石灰水鉴别Na2CO3溶液和NaHCO3溶液
C. 用CaCl2溶液鉴别Na2CO3溶液和NaHCO3溶液
D. 用淀粉溶液鉴别加碘盐和未加碘盐
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com