
【题目】已知N2(g)+3H2(g)2NH3(g);△H=﹣92.4kJmol﹣1 . 请回答: 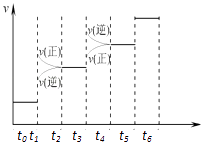
(1)当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如右图所示.图中tl时引起平衡移动的条件可能是 . 其中表示平衡混合物中NH3的含量最高的一段时是 .
(2)温度为T℃时,将2mol H2和1mol N2放入0.5L密闭容器中,充分反应后测得N2的转化率为50%.则平衡时 H2的浓度 .
(3)当温度升高时,反应的化学平衡常数K值(增大、减小、无影响).
(4)已知单质硫的燃烧热为296kJmol﹣1 , 写出其燃烧的燃烧热方程式: .
(5)已知中和热为57.3kJmol﹣1 , 写出NaOH和H2SO4反应的热化学方程式: .
【答案】
(1)增大压强;t2﹣t3
(2)1mol/L
(3)减小
(4)S(s)+O2(g)=SO2(g)△H=﹣296kJ?mol﹣1
(5)![]() H2SO4(aq)+NaOH(aq)=
H2SO4(aq)+NaOH(aq)= ![]() Na2SO4(aq)+H2O(l);△H=﹣57.3kJ/mol
Na2SO4(aq)+H2O(l);△H=﹣57.3kJ/mol
【解析】解:N2(g)+3H2(g)2NH3(g)△H=﹣92.4kJ/mol;反应是放热反应,反应前后气体体积减小,
(1.)由反应速率与时间关系图象可知,t1时正逆反应速率都增大,平衡正向移动,引起平衡移动的条件可能是增大压强;t3时刻正逆反应速率均迅速增大,但是平衡逆向进行,所以氨气的百分含量是减小的,即表示平衡混合物中NH3的含量最高的一段时间是t2﹣t3 ,
所以答案是:增大压强;t2﹣t3;
(2.)
N2(g) | + | 3H2(g) | 2NH2(g) | ||
开始 | 2mol/L | 4mol/L | 0 | ||
反应 | 1mol/L | 3mol/L | 2mol/L | ||
平衡 | 1mol/L | 1mol/L | 2mol/L |
平衡时氢气浓度=1mol/L,
所以答案是:1mol/L;
(3.)已知N2(g)+3H2(g)2NH3(g);△H=﹣92.4kJmol﹣1 , 反应是放热反应,升温平衡逆向进行,平衡常数减小,
所以答案是:减小;
(4.)单质硫的燃烧热为296KJmol﹣1 , 所以热化学方程式为:S(s)+O2(g)═SO2(g)△H=﹣296kJ/mol,
所以答案是:S(s)+O2(g)=SO2(g)△H=﹣296kJmol﹣1;
(5.)HCl和NaOH反应的中和热△H=﹣57.3kJmol﹣1 , H2SO4和NaOH反应的中和热是指反应生成1mol水放出57.3kJ的热量,反应的热化学方程式为 ![]() H2SO4(aq)+NaOH(aq)=
H2SO4(aq)+NaOH(aq)= ![]() Na2SO4(aq)+H2O(l);△H=﹣57.3kJ/mol,所以答案是:
Na2SO4(aq)+H2O(l);△H=﹣57.3kJ/mol,所以答案是: ![]() H2SO4(aq)+NaOH(aq)=
H2SO4(aq)+NaOH(aq)= ![]() Na2SO4(aq)+H2O(l);△H=﹣57.3kJ/mol.
Na2SO4(aq)+H2O(l);△H=﹣57.3kJ/mol.
【考点精析】认真审题,首先需要了解化学平衡状态本质及特征(化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效)),还要掌握化学平衡的计算(反应物转化率=转化浓度÷起始浓度×100%=转化物质的量÷起始物质的量×100%;产品的产率=实际生成产物的物质的量÷理论上可得到产物的物质的量×100%)的相关知识才是答题的关键.


 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案科目:高中化学 来源: 题型:
【题目】磷酸铁锂电池具有高效率输出、可快速充电、对环境无污染等优点,其工作原理如图。M电极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种
能传导Li+的高分子材料,隔膜只允许Li+通过,电池反应式
为LixC6+Li1-xFePO4 ![]() LiFePO4+6C。下列说法正确的是( )
LiFePO4+6C。下列说法正确的是( )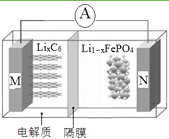
A.放电时Li+从右边移向左边
B.放电时M是负极,电极反应式为:C6x--xe-=6C
C.充电时N极连接电源的正极,电极反应式为:LiFePO4-xe-=Li1-xFePO4+xLi+
D.充电时电路中通过0.5mol电子,消耗36gC
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,不正确的是
A.H、D、T互为同位素
B.NaHCO3、HCOONa均含有离子键和共价键
C.常温常压下,22.4 L CCl4含有NA个CCl4分子
D.常温下,23 g NO2含有NA个氧原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20mL的某稀H2S04溶液中滴入0.1mol/L氨水,溶液中水电离出氢离子浓度随滴人氨水体积变化如图.下列分析正确的是( ) 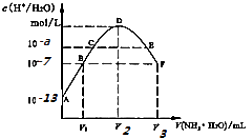
A.稀硫酸的浓度为0.1mol/L
B.C点溶液pH=14﹣a
C.E溶液中存在:c(NH4+)>c(SO42﹣)>c(H+)>c(OH﹣)
D.B到D,D到F所加氨水体积一定相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知二甲醚是一种重要的清洁燃料,可以通过CH3OH分子间脱水制得:2CH3OH(g)CH3OCH3(g)+H2O(g)△H=23.5kJmol﹣1 . 在T1℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示.请回答下列问题: 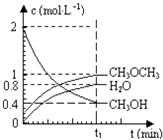
(1)该条件下反应平衡常数表达式K= . 在t1℃时,反应的平衡常数为 . 用CH3OH表示的化学反应速率 .
(2)相同条件下,若改变起始浓度,某时刻各组分浓度依次为c(CH3OH)=0.4molL﹣1、c(H2O)=0.6molL﹣1、c(CH3OCH3)=1.2molL﹣1 , 此时正、逆反应速率的大小:v (正)v (逆)(填“>”、“<”或“=”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语正确的是( )
A.醛基的结构简式﹣COH
B.丙烯分子的结构简式为:CH3CHCH2
C.四氯化碳分子的电子式为: ![]()
D.2﹣乙基﹣1,3﹣丁二烯的键线式: ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于某些氧化物的说法正确的是( )
A. NO2、Na2O2都能与水发生氧化还原反应
B. NO、CO2均可用向上排空气法收集
C. CO2、SO2可用澄清石灰水鉴别
D. CO2、SO3都可由相应单质在O2中燃烧生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有人设计了如图所示的实验装置来探究钠与水反应(铁架台等仪器略去).实验前在橡胶塞下端打一个小孔穴,将一大小适中的钠块固定于针头下端,向上抽动针头使钠块藏于孔穴内.在玻璃反应管内装入适量水(使钠块不与水接触).实验时,拔去橡胶乳头,按住橡胶塞,将针头缓缓向上拔起使钠与水接触,反应管内的液体被产生的气体压出,流入置于下方的烧杯中,气体则被收集在反应管内.
(1)钠与水反应的离子方程式为 .
(2)实验中“钠块熔化为闪亮的小球”说明;向烧杯中的溶液中滴加 , 溶液变红,说明钠与水反应生成碱性物质.
(3)如果实验前加入反应管内水的体积为a mL,欲使水最终全部被排出,则所取金属钠的质量至少为g.(设当时实验条件下气体摩尔体积为V mL/mol,写出简要步骤)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】FeCO3与砂糖混用可以作补血剂,实验室里制备FeCO3的流程如图所示.下列说法错误的是( ) 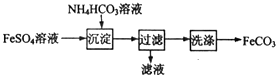
A.可利用KSCN溶液检验FeSO4溶液是否变质
B.沉淀过程中有CO2气体放出
C.过滤搡作的常用玻璃仪器有烧杯、漏斗和玻璃棒
D.产品FeCO3在空气中高温分解可得到纯净的FeO
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com