
为探究HClO的漂白性,有人设计了如下图所示的实验.

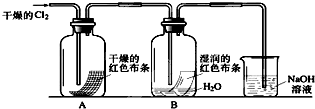
(1)通入Cl2后,从集气瓶A中干燥的红色布条的现象可得出的结论是________.
从集气瓶B中湿润的红色布条的现象可得出的结论是______________________.
(2)为了确证是HClO使湿润的红色布条褪色,你认为还应增加一个什么实验____________________________.
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
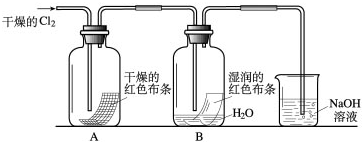 为了探究HClO的漂白性,某同学设计了如下的实验.
为了探究HClO的漂白性,某同学设计了如下的实验.查看答案和解析>>
科目:高中化学 来源: 题型:

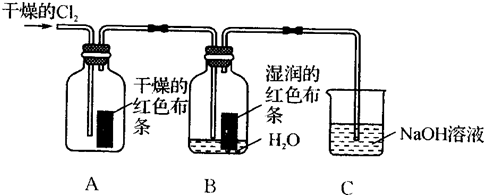
(1)通入Cl2后,从集气瓶A中干燥的红色布条的现象可得出的结论是________________。
从集气瓶B中湿润的红色布条的现象可得出的结论是________________________________。
(2)为了确证是HClO使湿润的红色布条褪色,你认为还应增加一个什么实验__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com