
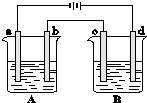
 如图所示的A、B两个电解池中的电极均为铂,在A池中加入0.05mol?L-1的CuCl2溶液,B池中加入0.1mol?L-1的AgNO3溶液,进行电解.a、b、c、d四个电极上所析出的物质的物质的量之比是( )
如图所示的A、B两个电解池中的电极均为铂,在A池中加入0.05mol?L-1的CuCl2溶液,B池中加入0.1mol?L-1的AgNO3溶液,进行电解.a、b、c、d四个电极上所析出的物质的物质的量之比是( )| A、1:1:2:1 |
| B、2:1:1:1 |
| C、2:2:4:1 |
| D、2:1:2:1 |
| ||
| ||


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、只有③ | C、②④ | D、①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用小苏打治疗胃酸过多 HCO3-+H+═CO2↑+H2O |
| B、往碳酸镁中滴加稀盐酸 CO32-+2H+═CO2↑+H2O |
| C、氯气通入冷水中 Cl2+H2O═Cl-+ClO-+2H+ |
| D、氢氧化钡溶液与稀硫酸反应 Ba2++SO42-+H++OH-═BaSO4↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、由于水中存在氢键,所以稳定性:H2O>H2S |
| B、由于磷化氢的相对分子质量比氨气的大,所以沸点:PH3>NH3 |
| C、若A2+2D-═2A-+D2,则氧化性D2>A2 |
| D、若R2-和M+的电子层结构相同,则离子半径R2->M+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在1L 0.1mol/L的NH4NO3溶液中含氮原子数目为0.2NA |
| B、标准状况下22.4 L CH3CH2OH中碳原子数为2NA |
| C、0.2 mol?L-1 NaHCO3溶液中含Na+数为0.2NA |
| D、标准状况下,22.4L Cl2与足量的铁粉完全反应转移电子数目为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
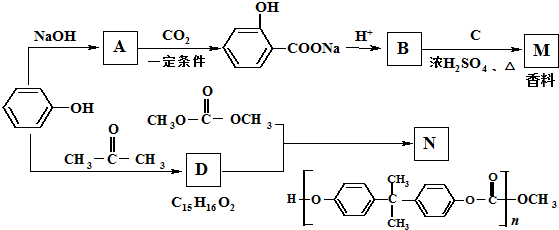
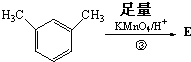 其中核磁共振氢谱显示其分子中含有4种不同的氢原子的为
其中核磁共振氢谱显示其分子中含有4种不同的氢原子的为查看答案和解析>>
科目:高中化学 来源: 题型:

| x |
| 2 |
| x |
| 2 |
| 1 |
| 2 |
| 3 |
| 2 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com