
| A. | sp3杂化轨道是由任意的1个s轨道和3个p轨道混合形成的四个sp3杂化轨道 | |
| B. | 乙炔分子中,每个碳原子都有两个未杂化的2p轨道形成π键 | |
| C. | 凡中心原子采取sp2杂化的分子,其分子构型都是平面三角形 | |
| D. | 凡AB2型的共价化合物,其中心原子A均采用sp杂化轨道成键 |
分析 A.原子中能量相近的某些轨道,在成键时,能重新组合成能量相等的新轨道为杂化轨道;
B.碳碳三键中含有一个σ键和两个π键,每个碳原子含有2个σ键且不含孤电子对,每个碳原子都有两个未杂化的2p轨道肩并肩重叠形成两个π键;
C.根据价层电子对互斥理论确定分子空间构型及中心原子杂化方式,价层电子对个数=配原子个数+孤电子对个数,n=3,sp2杂化,不含孤电子对其分子构型都是平面三角形,否则不是;
D.根据价层电子对互斥理论确定其杂化方式,如果价层电子对为2,则中心原子以sp杂化轨道成键,AB2型的共价化合物,其中心原子A不一定采用sp杂化轨道成键.
解答 解:A.sp3杂化轨道是指同一电子层内,1个s轨道和3个p轨道杂化,形成能量相等的四个sp3杂化轨道,故A错误;
B.乙炔分子的结构式H-C≡C-H,中心原子碳原子价层电子对个数=σ键个数+孤电子对个数=2+$\frac{1}{2}$×(4-2×2)=2,采取sp杂化,每个碳原子都有两个未杂化的2p轨道形成π键,故B正确;
C.中心原子采取sp2杂化的分子,n=3,sp2杂化,不含孤电子对其分子构型都是平面三角形,否则不是,如二氧化硫分子中,价层电子对数=2+$\frac{1}{2}$(6-2×2)=3,所以采取sp2杂化,含有一对孤电子对,所以立体构型为V型,故C错误;
D.AB2型的共价化合物,其中心原子A价层电子对为2,则中心原子以sp杂化轨道成键,如氯化铍分子中,铍原子含有两个共价单键,不含孤电子对,所以价层电子对数是2,中心原子以sp杂化轨道成键,AB2型的共价化合物,也有不采用sp杂化轨道成键,如二氧化硫分子中,价层电子对数=2+$\frac{1}{2}$(6-2×2)=3,所以采取sp2杂化,故D错误.
故选B.
点评 本题考查了杂化轨道、分子空间结构等,题目难度中等,注意把握杂化轨道理论的应用,注意判断中心原子的价层电子对以及孤对电子数的判断.


科目:高中化学 来源: 题型:解答题
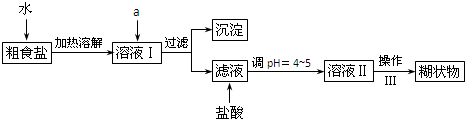
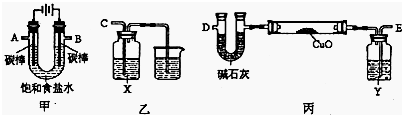
| 方案 质量 | 方案一 | 方案二 |
| U型管+固体 | 硬质玻璃管+固体 | |
| 反应前质量/g | a | c |
| 完全反应后质量/g | b | d |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
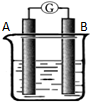 某研究性学习小组欲探究原电池的工作原理,按如图所示装置进行实验.
某研究性学习小组欲探究原电池的工作原理,按如图所示装置进行实验.| 序号 | A | B | 烧杯中的液体 |
| 1 | Mg | Al | 稀H2SO4 |
| 2 | Pt | Pt | NaOH溶液 |
| 3 | Pt | Pt | 熔融的Na2CO3 |
| 4 | Pb | PbO2 | 稀H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓解度:碳酸氢钠>碳酸钠 | |
| B. | 热稳定性:碳酸钠<碳酸氢钠 | |
| C. | 等质量时与足量酸反应产气量:碳酸钠>碳酸氢钠 | |
| D. | 一定的条件下可以相互转化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 牙膏品牌 | 两面针儿童牙膏 | 中华透明牙膏 | 珍珠防臭牙膏 |
| 摩擦剂 | 氢氧化铝 | 二氧化硅 | 碳酸钙 |
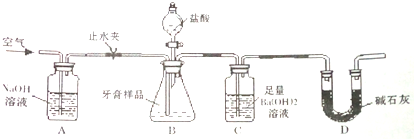
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 两个原子或多个原子之间的相互作用叫做共价键 | |
| B. | 阴、阳离子间通过静电引力而形成的化学键叫做离子键 | |
| C. | 分子晶体中一定含有共价键,离子晶体中一定含有离子键 | |
| D. | 氯化钠晶体中含有阳离子,氯化钠溶液中也含有阳离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜粉加入到Fe2(SO4)3溶液中:Cu+Fe3+═Cu2++Fe | |
| B. | 钠块投入到CuSO4溶液中:2Na+Cu2+═2Na++Cu↓ | |
| C. | Cl2通入到NaOH溶液中:Cl2+2OH-═Cl-+ClO-+H2O | |
| D. | 用NaOH溶液吸收少量CO2:OH-+CO2═HCO${\;}_{3}^{-}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应:N2(g)+O2(g)?2NO(g),曲线a表示该反应在温度T℃时N2的浓度随时间的变化,曲线b表示该反应在某一起始反应条件改变时N2的浓度随时间的变化.叙述正确的是( )
一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应:N2(g)+O2(g)?2NO(g),曲线a表示该反应在温度T℃时N2的浓度随时间的变化,曲线b表示该反应在某一起始反应条件改变时N2的浓度随时间的变化.叙述正确的是( )| A. | 温度T℃时,该反应的平衡常数K=$\frac{4({c}_{0}-{c}_{1})^{2}}{{c}_{{T}^{2}}}$ | |
| B. | 温度T℃时,混合气体的密度不变即达到平衡状态 | |
| C. | 曲线b对应的条件改变可能是加入了催化剂 | |
| D. | 若曲线b改变的条件是温度,则该正反应放热 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com