
在一定温度下,有a.盐酸 b.硫酸 c.醋酸三种酸:
(1)当三种酸物质的量浓度相同时,c(H+)由大到小的顺序是________。
(2)同体积、同物质的量浓度的三种酸,中和NaOH的能力由大到小的顺序是________。
(3)若三者c(H+)相同时,物质的量浓度由大到小的顺序是_____________________________________________________。
(4)当三者c(H+)相同且体积也相同时,分别放入足量的锌,相同状况下产生气体的体积由大到小的顺序是________。
(5)当c(H+)相同、体积相同时,同时加入形状、密度、质量完全相同的锌,若产生相同体积的H2(相同状况),则开始时反应速率的大小关系为________。反应所需时间的长短关系是_______________________________ _________________________________________。
(6)将c(H+)相同的三种酸均加水稀释至原来的100倍后,c(H+)由大到小的顺序是________。
解析 HCl===H++Cl- H2SO4===2H++SO CH3COOHH++CH3COO-
CH3COOHH++CH3COO-
(1)当三种酸物质的量浓度相同时,三种酸中c(H+)由大到小顺序为b>a>c。
(2)同体积、同物质的量浓度的三种酸,中和NaOH的能力盐酸和醋酸相同,因随着NaOH溶液的加入CH3COOH电离平衡右移,提供的氢离子和盐酸相同,而硫酸提供的H+是它们的2倍,故b>a=c。
(3)c(H+)相同时,醋酸溶液浓度最大,因醋酸为弱酸,电离程度小,硫酸浓度为盐酸的一半,故c>a>b。
(4)当三者c(H+)相同时,因HCl、H2SO4为强电解质,在溶液中完全电离,所以H+总的物质的量相同,故产生H2体积相同。CH3COOH为弱电解质,最终能提供的H+最多,生成H2体积最大。故c>a=b。
(5)开始时由于三者c(H+)相同,故在所给条件下开始生成氢气的速率相同。随着反应的不断进行,HCl、H2SO4中的H+不断减少,而CH3COOH能不断电离出H+,故产生等量H2时,醋酸所需时间最短,即所需时间a=b>c。
(6)由于HCl、H2SO4完全电离,加水稀释后,c(H+)减小的程度较大,CH3COOH部分电离,随着水的加入,使CH3COOH的电离程度增大,稀释相同的倍数,c(H+)减小的程度较小,故c>a=b。
答案 (1)b>a>c (2)b>a=c (3)c>a>b (4)c>a=b (5)a=b=c a=b>c (6)c>a=b


科目:高中化学 来源: 题型:
已知:在一定条件下,有如下反应可以发生
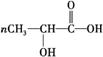

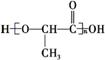 +(n-1)H2O
+(n-1)H2O
某一试剂瓶的标签严重破损,只能隐约看到其中一部分:
 结构简式
结构简式 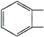
相对分子质量166
取该试剂瓶中的试剂,通过燃烧实验测得:16.6 g该物质完全燃烧得到39.6 g CO2与9 g H2O。进一步实验可知:①该物质能与碳酸氢钠溶液反应生成无色无味气体。②16.6 g该物质与足量金属钠反应可生成氢气2.24 L(已折算成标准状况)。请回答:
(1)该有机物的分子式为________,该有机物的结构可能有________种。
(2)若下列转化中的D是上述有机物可能结构中的一种,且可发生消去反应;E含两个六元环;F是高分子化合物;取C在NaOH水溶液中反应后的混合液,加入足量硝酸酸化后,再加入硝酸银溶液,出现白色沉淀。
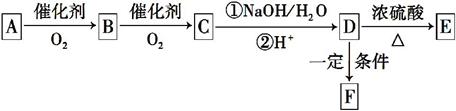
①A的结构简式为____________________________。
②写出A转化成B的化学方程式__________________________。
③写出由D制取F的化学方程式__________________________。
④反应类型:D→E__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
为测定镀锌铁皮锌镀层的厚度,将镀锌铁皮与足量盐酸反应,待产生的气泡明显减少时取出,洗涤,烘干,称重。关于该实验的操作对测定结果的影响判断正确的是
A.铁皮未及时取出,会导致测定结果偏小
B.铁皮未洗涤干净,会导致测定结果偏大
C.烘干时间过长,会导致测定结果偏小
D.若把盐酸换成硫酸,会导致测定结果偏大
查看答案和解析>>
科目:高中化学 来源: 题型:
SiO2是一种化工原料,可以制备一系列物质(如下图所示)。下列说法错误的是 ( )
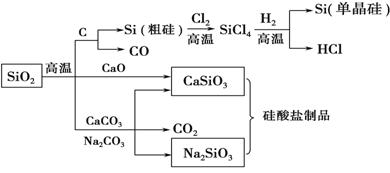
A.高炉炼铁时,加入石灰石将铁矿石中的脉石(主要成分为SiO2)转化为易熔的炉渣
B.纯净的二氧化硅和单晶硅都是信息产业的重要基础材料
C.用盐酸可除去石英砂(主要成分为SiO2)中少量的碳酸钙
D.图中所含反应都不属于氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
加热N2O5,依次发生的分解反应为①N2O5 N2O3+O2,②N2O3
N2O3+O2,②N2O3 N2O+O2;在2 L密闭容器中充入8 mol N2O5,加热到t ℃,达到平衡状态后O2为9 mol,N2O3为3.4 mol。则t ℃时反应①的平衡常数为( )
N2O+O2;在2 L密闭容器中充入8 mol N2O5,加热到t ℃,达到平衡状态后O2为9 mol,N2O3为3.4 mol。则t ℃时反应①的平衡常数为( )
A.10.7 B.8.5 C.9.6 D.10.2
查看答案和解析>>
科目:高中化学 来源: 题型:
日常生活中的许多现象与化学反应有关,下列现象与氧化还原反应无关的是( )
A.铜铸塑像上出现铜绿[Cu2(OH)2CO3] B.铁制菜刀生锈
C.大理石雕像被酸雨腐蚀毁坏 D.铝锅表面生成致密的氧化膜
查看答案和解析>>
科目:高中化学 来源: 题型:
某校学生课外活动小组的同学设计下图所示实验装置,用来验证一氧化碳具有还原性,回答下列问题:
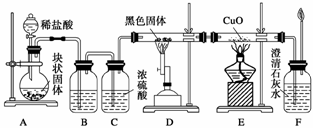
(1)写出装置A中所发生反应的离子方程式:________________________________。
(2)装置B中最适宜的试剂是____________________________________________。
(3)若实验中没有装置C,使装置B与装置D直接相连,会对实验造成的影响是
________________________________________________________________________
________________________________________________________________________。
(4)装置D中黑色固体为________(填名称),反应的化学方程式为_______________
________________________________________________________________________。
(5)按照如图装置进行实验时,首先进行的操作是___________________________。
(6)根据实验中的_________________________________________________现象,
可证明CO具有还原性,有关反应的化学方程式是____________________________。
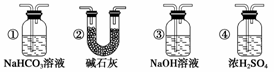
(7)若要根据装置F中澄清石灰水变浑浊的现象确认一氧化碳具有还原性,应在上图装置________与______之间连接下图中的________装置(填序号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
根据①~⑩元素的编号所在周期表中的位置,用相应的元素符号回答有关问题:
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 1 | ① | ② | ||||||
| 2 | ③ | ④ | ⑤ | ⑥ | ⑦ | |||
| 3 | ⑧ | ⑨ | ⑩ |
(1)能显+1价,还能显-1价的元素是_______________________________。
(2)最难形成简单离子的元素是______________________________________。
(3)单质具有半导体性质的元素是____________________________________。
(4)元素的气态氢化物既不和所有的酸作用,又不和所有的碱作用的是________________________。
(5)能跟氙、氪形成二元化合物的元素是_______________________________。
(6)最新发现的一种单质是由60个原子组成球状结构的分子。这种单质叫足球烯,它是由________元素组成的。
(7)其单质能和冷水剧烈反应的元素是________。
(8)a元素能以正化合价与b元素形成AB型化合物,该化合物常温下为固态且难溶于水,则a元素是________,b元素是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com