
某主族元素R的最高化合价与负化合价代数和为6.下列说法正确的是()
A. R的气态氢化物能燃烧
B. R的最高价氧化物为RO3
C. R一定是第ⅦA族元素
D. R的气态氢化物易溶于水显碱性
考点: 原子结构与元素的性质.
分析: 某主族元素R的最高化合价与负化合价代数和为6,设最高化合价为x,则最低化合价为x﹣8,则有x+x﹣8=6,解x=7,应位于第ⅦA族元素,则该元素的最高化合价为+7价,最低化合价为﹣1价,由于F元素没有最高正化合价,R不能F元素,结合对应物质的性质解答该题.
解答: 解:主族元素R的最高化合价与负化合价代数和为6,设最高化合价为x,则最低化合价为x﹣8,则有x+x﹣8=6,x=7,应位于第ⅦA族元素,则该元素的最高化合价为+7价,最低化合价为﹣1价,由于F元素没有最高正化合价,R不能F元素.
A.R为Cl、Br等元素,对应的氢化物不能再空气中燃烧,故A错误;
B.该元素的最高化合价为+7价,R的最高价氧化物为R2O7,故B错误;
C.该元素的最高化合价为+7价,说明原子的最外层有7个电子,应位于第ⅦA族元素,故C正确;
D.R为卤族元素,对应的氢化物溶于水呈酸性,故D错误.
故选C.
点评: 本题考查元素周期律与元素周期表的综合应用,难度中等,注意从化合价的角度判断元素在周期表的位置,注意对元素周期律理解掌握.


 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案科目:高中化学 来源: 题型:
青苹果汁遇碘溶液显蓝色,熟苹果能还原银氨溶液。这说明( )
A.青苹果中只含淀粉不含糖类
B.熟苹果中只含糖类不含淀粉
C.苹果成熟时淀粉水解为单糖
D.苹果成熟时单糖聚合成淀粉
查看答案和解析>>
科目:高中化学 来源: 题型:
已知A、B、C、D和E五种分子所含原子的数目依次为1、2、3、4和6,且都含有18个电子,又知B、C和D由两种元素的原子组成,且D分子中两种原子个数比为1∶1。
(1)组成A分子的原子的核外电子排布式是________;
(2)B和C的分子式分别是________和________;C分子的立体结构呈
________形,该分子属于________分子(填“极性”或“非极性”);
(3)向D的稀溶液中加入少量氯化铁溶液现象是________________,该反应的
化学方程式为_____________________________________________________。
(4)若将1 mol E在氧气中完全燃烧,只生成1 mol CO2和2 mol H2O,则E的
分子式是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
关于工业生产的叙述,错误的是 ( )。
A.制普通玻璃的主要原料是纯碱、石灰石、石英
B.氨是制作氮肥、硝酸、铵盐的重要原料
C.将二氧化硫催化氧化生成三氧化硫后,在吸收塔内用水吸收制得浓硫酸
D.制造普通水泥的主要原料是黏土、石灰石
查看答案和解析>>
科目:高中化学 来源: 题型:
硅单质及其化合物应用很广。请回答下列问题:
(1)制备硅半导体材料必须先得到高纯硅。三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程示意图如下 :




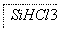

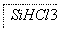


①写出由纯SiHCl3制备高纯硅的化学反应方程式____________________。
②整个制备过程必须严格控制无水、无氧。SiHCl3遇水剧烈反应生成H2SiO3、
HCl和另一种物质,写出配平的化学反应方程式____________________;H2
还原SiHCl3过程中若混有O2,可能引起的后果是____________________。
(2)下列有关硅材料的说法正确的是 ( )。
A.单质硅化学性质稳定,但可以被强碱溶液腐蚀
B.盐酸可以与硅反应,故采用盐酸为抛光液抛光单晶硅
C.普通玻璃是由纯碱、石灰石和石英砂制成的,其熔点很高
D.光导纤维的主要成分是SiO2
(3)硅酸钠水溶液俗称水玻璃。取少量硅酸钠溶液于试管中,逐滴加入盐酸,
振荡。写出实验现象并给予解释(用化学方程式说
明)____________________________________________________________。
(4)在人体器官受到损伤时,需要使用一种新型无机非金属材料来植入体内,
这种材料是________(填字母)。
A.高温结构陶瓷 B.生物陶瓷 C.导电陶瓷
查看答案和解析>>
科目:高中化学 来源: 题型:
根据所学的元素周期律知识,下列说法正确的是()
A. 碱金属元素从上到下随核电荷数的增加,单质的熔沸点逐渐升高
B. 第二周期元素(除稀有气体外)从左到右随核电荷数的增加,其最高正价从+1到+7
C. Se的氢化物应该比硫化氢稳定
D. Sr的碳酸盐应该难溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、R、Q是短周期元素,R、Q和X、Y分别处于同一周期,R、Y处于同一主族,Q2﹣和X2+具有相同的电子层结构,其中Q是地壳中含量最高的元素,R最外层电子数是次外层的2倍.下列说法正确的是()
A. 离子半径:Q2﹣>X2+
B. 原子序数:Y>R>Q
C. 简单气态氢化物的稳定性:R>Q>Y
D. 原子最外层电子数:X>Y>Q
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,反应X(g)+3Y(g)⇌2Z(g)达到化学平衡状态的标志是( )
|
| A. | X、Y、Z的分子数比为1:3:2 |
|
| B. | 单位时间生成amolX,同时生成3a molY |
|
| C. | X、Y、Z的浓度相等 |
|
| D. | 3v正(X)=v逆(Y) |
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下氨气和氧化铜可以发生如下反应:2NH3+3CuO 3Cu+N2+3H2O,下列对此反应的分析中合理的是()
3Cu+N2+3H2O,下列对此反应的分析中合理的是()
A. 该反应属于置换反应
B. CuO是氧化剂
C. 反应体现了金属铜的还原性
D. 每生成1molH2O就伴随着1mol电子转移
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com