
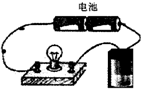
 用如图所示的装置分别进行如下实验,各离子方程式书写正确且各组物质反应后溶液的导电性变化不大
用如图所示的装置分别进行如下实验,各离子方程式书写正确且各组物质反应后溶液的导电性变化不大

 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案科目:高中化学 来源: 题型:
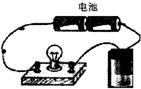
 某课外活动小组准备用如图所示的装置进行实验.现有甲、乙、丙三位同学分别选择了如下电极材料和电解质溶液:
某课外活动小组准备用如图所示的装置进行实验.现有甲、乙、丙三位同学分别选择了如下电极材料和电解质溶液:| A电极 | B电极 | X溶液 | |
| 甲 | Cu | Zn | H2SO4 |
| 乙 | Pt | Pt | CuCl2 |
| 丙 | Fe | Cu | ? |
| ||
| ||
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.向硝酸银溶液中通入少量氯化氢:Ag++HCl=AgCl↓+H+ |
| B.向亚硫酸溶液中通入氯气:H2SO3+Cl2+H2O=SO42-+4H++2Cl- |
| C.向FeI2溶液中通入少量氯气:2Fe2++Cl2=2Fe3++2Cl- |
| D.向NaOH溶液中通入少量氯气:2OH-+Cl2=Cl-+ClO-+H2O |
查看答案和解析>>
科目:高中化学 来源:2012-2013学年宁夏银川一中高三(上)期中化学试卷(解析版) 题型:选择题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com